21 oktober 2019: Zie ook dit artikel:
9 februari 2016: Bron: The Lancet
Het was al eerder bekend gemaakt maar nu nog eens bevestigd in The Lancet: wanneer prostaatkankerpatiënten met een Gleasonscore van 8 tot 10 bij de diagnose of een recidief of uitzaaiingen hebben na resistentie voor hormoontherapie standaard docetaxel krijgen naast hormoontherapie dan stijgt hun levensduur mediaan met ca. 10 maanden op 5 jaar (8%) in vergelijking met beste zorg = hormoontherapie. Maar de bijwerkingen zijn dusdanig slechter (plus 20%) voor docetaxel dat je je kunt afvragen of dat de moeite waard is. Misschien wel voor die patiënten die al uitzaaiingen hebben bij de eerste diagnose: want bij die patiënten die al uitzaaiingen hadden bij de eerste diagnose bleek het verschil in overall overleving 15 maanden tussen docetaxel en hormoontherapie, 45 versus 60 maanden.Maar ook hier veel meer bijwerkingen en veel slechtere kwaliteit van leven. Ook in hun conclusie schrijven de onderzoekers dat alleen mannen met een goede lichamelijke en psychische conditie chemo zou kunnen worden aangeboden.
Hierbij ook de kanttekening dat dit een studie is die is uitgevoerd voordat Abiraterone en enzalutamide hun intrede deden. En dan praten we nog niet over immuuntherapie met prostvac. Wel werden over alle patiëntengroepen verdeeld waar nodig radiotherapie - bestraling toegepast.
Bovendien is de groep patiënten die een lagere Gleasonscore hadden nog niet meegenomen in de analyse van de overall overleving.
Studieresultaten:
In de open-label studie namen 2,962 mannen deel met nieuw gediagnosteerde prostaatkanker uitgezaaide, lymfklier positieve of hoog risico gevorderde ziekte (Gleasonscore van 8 tot 10) deel. De studie loopt over de periode oktober 2005 tot maart 2013. De patienten kwamen uit 100 verschillende ziekenhuizen in Zwitserland en Engeland. Zij kregen als standaard behandeling langdurige hormoontherapie. Daarnaast werden de volgende groepen gerandomiseerd ingedeeld op basis van een 2:1:1:1 verdelingsschema:
- standaard hormoon therapie voor ≥ 2 jaar (n = 1,184),(controlegroep)
- standaard hormoontherapie plus zoledronic acid (Zometa) (n = 593),
- standaard hormoontherapie plus docetaxel (n = 592),
- standaard hormoontherapie met zowel zoledronic acid (Zometa) en docetaxel (n = 593).
Daarnaast werd radiotherapie toegepast waar nodig in alle groepen.
Patiënten hadden een mediane leeftijd van 65 jaar. Overall, 94% van de patiënten waren nieuw gediagnosteerd, 1,738 (62%) van de 2797 nieuw gediagnosteerden en 79 (48%) van de 165 patiënten met recidief hadden uitzaaiingen bij start van de studie (61% overall); 448 (15%) had N+/X, M0 ziekte, en 697 (24%) had N0, M0 ziekte. *(NO = lymfklieren wel of niet aangetast. MO is aantal uitzaaiingen)
Mediane PSA waarde was 65 ng/mL, 71% van de patiënten had een Gleason score tussen 8 en 10, en 6% had eerder een lokale behandeling gehad. Radiotherapie - bestraling was toegepast bij 25% tot 27% van de patiënten, inclusief bij 57% tot 63% van degenen met geen uitgezaaide ziekte.
Overall overleving:
Mediane follow-up was 43 maanden (interquartile range = 30–60 maanden). Er waren 415 sterfgevallen in de controle groep, met 347 (84%) gerelateerd aan prostaatkanker.
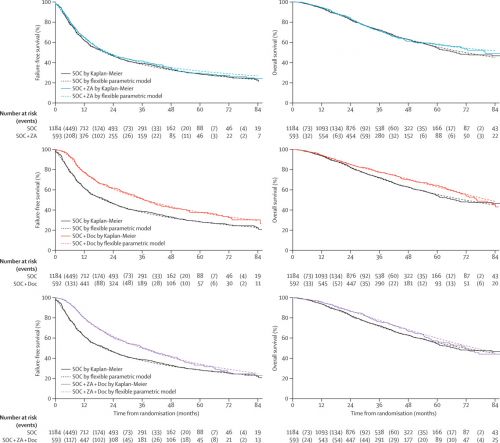
- Mediane overall overleving was 71 maanden (IQR = 32 maanden tot niet bereikt) in de controlegroep = standaard hormoontherapiegroep.
- Mediane overall overleving is nog niet bereikt (IQR = 32 maanden tot niet bereikt) in de zoledronic acid groep (HR = 0.94, 95% confidence interval = 0.79–1.11, P = .450),
- Mediane overall overleving is 81 maanden (IQR = 41 maanden tot nog niet bereikt) in de docetaxel groep (HR = 0.78, 95% CI = 0.66–0.93, P = .006),
- Mediane overall overleving is 76 maanden (IQR = 39 maanden tot nog niet bereikt) in de zoledronic acid plus docetaxel groep (HR = 0.82, 95% CI = 0.69–0.97, P = .022).
- 5-jaars overleving was respectievelijk 55% (controlegroep), 57% (zoledronic acid groep), 63% (docetaxelgroep) en 60% (docetaxel plus Zoledronic Acid groep)
- Onder de patiënten met uitgezaaide ziekte bij de diagnose was de mediane overall overleving 45 maanden in de controlegroep, 46 maanden (HR = 0.93, P = .416) in de zoledronic acid groep, 60 maanden (HR = 0.76, P = .005) in de docetaxel groep en 55 maanden (HR = 0.79, P = .015) in de zoledronic acid plus docetaxel groep.
- 5-jaars overleving was 39% (controlegroep), 43% (zoledronic acid groep), 50% (docetaxel groep), en 46%, (docetaxel plus zoledronic acid groep). Data voor de groep met niet uitgezaaide ziekte was op moment van opmaken van deze resultaten nog niet voorhanden omdat einddoel in deze groep nog niet bereikt was.
Ziektevrije tijd en sterfte aan prostaatkanker:
Mediane ziektevrije tijd was 20 maanden in de controlegroep (alleen hormoontherapie) versus 22 maanden in de zoledronic acid groep (HR = 0.92, P = .198), 37 maanden in de docetaxel groep (HR = 0.61, P = .413 × 10-13), en 36 maanden in de zoledronic acid plus docetaxel groep (HR = 0.62, P = .134 × 10-12).
5-jaars ziektevrije tijd was respectievelijk 28% (controlegroep), 31% (zoledronic acid groep), 38% (docetaxelgroep), en 34% (docetaxel plus zoledronic acid groep).
Op het moment van de analyse 978 mannen waren overleden, 809 (83%) gerelateerd aan prostaatkanker; onmder de mannen die overleden was de reden van overlijden bij 86% van de mannen die bij aanvang al uitgezaaide ziekte hadden en 68% bij niet uitgezaaide ziekte. vergeleken met de controlegroep was de kans te overlijden aan prostaatkanker minder in de docetaxel groep (HR = 0.79, P = .019) en de zoledronic acid plus docetaxel groep (HR = 0.78, P = .013) maar niet in de groep van alleen zoledronic acid. (HR = 0.95, P = .613).
Bijwerkingen:
Grade ≥ 3 bijwerkingen traden op bij 32% van de patiënten in de controlegroep (met hormonale klachten 12%, als meest voorkomend), 32% in de zoledronic acid groep (hormonale klachten12%), 52% in de docetaxel groep (febrile neutropenia in 15%, neutropenia in 12%, hormonale kalchten in 10%), en 52% in de zoledronic acid plus docetaxel groep (febrile neutropenia in 14%, neutropenia in 12%, hormonale kalchten in 12%, algemene klachten bv., lethargie, koorts, enz. in 11%). Botafbraak van de kaak kwam voor bij 2% van de patienten uit de zoledronic acid groep en bij 4% in de zoledronic acid plus docetaxel groep.
Van 8 sterfgevallen lijkt dit gerelateerd aan de bijwerkingen rechtstreeks verband houdende met de behandelingen (7 in de docetaxel plus zoledronic acidgroep en 1 in de docetaxelgroep.)
Conclusie van de onderzoekers:
“Zoledronic acid toont geen bewijs van overlevingswinst en zou geen deel moeten uitmaken van de behandeling voor deze groep van patienten. Chemo met Docetaxel gegeven naast langdurige hormoontherapie geeft wel overlevingswinst t.o.v. alleen hormoontherapie, maar geeft ook beduidend meer bijwerkingen. Docetaxel zou onderdeel uit kunnen maken van een behandleing voor mannen die lichamelijk en psychisch nog in goede conditie zijn en nog moeten starten met hormoontherapie”
Hier het abstract van de studie
Zoledronic acid showed no evidence of survival improvement and should not be part of standard of care for this population. Docetaxel chemotherapy, given at the time of long-term hormone therapy initiation, showed evidence of improved survival accompanied by an increase in adverse events. Docetaxel treatment should become part of standard of care for adequately fit men commencing long-term hormone therapy.
Addition of docetaxel, zoledronic acid, or both to first-line long-term hormone therapy in prostate cancer (STAMPEDE): survival results from an adaptive, multiarm, multistage, platform randomised controlled trial
Open access funded by Cancer Research UK
Summary
Background
Long-term hormone therapy has been the standard of care for advanced prostate cancer since the 1940s. STAMPEDE is a randomised controlled trial using a multiarm, multistage platform design. It recruits men with high-risk, locally advanced, metastatic or recurrent prostate cancer who are starting first-line long-term hormone therapy. We report primary survival results for three research comparisons testing the addition of zoledronic acid, docetaxel, or their combination to standard of care versus standard of care alone.
Methods
Standard of care was hormone therapy for at least 2 years; radiotherapy was encouraged for men with N0M0 disease to November, 2011, then mandated; radiotherapy was optional for men with node-positive non-metastatic (N+M0) disease. Stratified randomisation (via minimisation) allocated men 2:1:1:1 to standard of care only (SOC-only; control), standard of care plus zoledronic acid (SOC + ZA), standard of care plus docetaxel (SOC + Doc), or standard of care with both zoledronic acid and docetaxel (SOC + ZA + Doc). Zoledronic acid (4 mg) was given for six 3-weekly cycles, then 4-weekly until 2 years, and docetaxel (75 mg/m2) for six 3-weekly cycles with prednisolone 10 mg daily. There was no blinding to treatment allocation. The primary outcome measure was overall survival. Pairwise comparisons of research versus control had 90% power at 2·5% one-sided α for hazard ratio (HR) 0·75, requiring roughly 400 control arm deaths. Statistical analyses were undertaken with standard log-rank-type methods for time-to-event data, with hazard ratios (HRs) and 95% CIs derived from adjusted Cox models. This trial is registered at ClinicalTrials.gov (NCT00268476) and ControlledTrials.com (ISRCTN78818544).
Findings
2962 men were randomly assigned to four groups between Oct 5, 2005, and March 31, 2013. Median age was 65 years (IQR 60–71). 1817 (61%) men had M+ disease, 448 (15%) had N+/X M0, and 697 (24%) had N0M0. 165 (6%) men were previously treated with local therapy, and median prostate-specific antigen was 65 ng/mL (IQR 23–184). Median follow-up was 43 months (IQR 30–60). There were 415 deaths in the control group (347 [84%] prostate cancer). Median overall survival was 71 months (IQR 32 to not reached) for SOC-only, not reached (32 to not reached) for SOC + ZA (HR 0·94, 95% CI 0·79–1·11; p=0·450), 81 months (41 to not reached) for SOC + Doc (0·78, 0·66–0·93; p=0·006), and 76 months (39 to not reached) for SOC + ZA + Doc (0·82, 0·69–0·97; p=0·022). There was no evidence of heterogeneity in treatment effect (for any of the treatments) across prespecified subsets. Grade 3–5 adverse events were reported for 399 (32%) patients receiving SOC, 197 (32%) receiving SOC + ZA, 288 (52%) receiving SOC + Doc, and 269 (52%) receiving SOC + ZA + Doc.
Interpretation
Zoledronic acid showed no evidence of survival improvement and should not be part of standard of care for this population. Docetaxel chemotherapy, given at the time of long-term hormone therapy initiation, showed evidence of improved survival accompanied by an increase in adverse events. Docetaxel treatment should become part of standard of care for adequately fit men commencing long-term hormone therapy.
Funding
Cancer Research UK, Medical Research Council, Novartis, Sanofi-Aventis, Pfizer, Janssen, Astellas, NIHR Clinical Research Network, Swiss Group for Clinical Cancer Research.
Gerelateerde artikelen
- Docetaxel zou altijd gegeven moeten worden naast hormoontherapie bij reeds uitgezaaide prostaatkanker blijkt uit Stampede studie. Na 6 jaar was er een betere overall overleving en progressievrije ziekte dan alleen hormoontherapie.
- Docetaxel geeft naast hormoontherapie betere overleving bij hoog risico of uitgezaaide prostaatkanker met Gleasonscore van 8 tot 10 bij diagnose maar wel ten koste van kwaliteit van leven door bijwerkingen
- Bloedverdunners naast chemo verlengt leven van patienten met vergevorderde prostaatkanker met gemiddeld vier maanden
- Chemo: REVLIMID - lenalidomide fase 3 studie bij hormoonresistente prostaatkanker onder de naam Actimid - wordt stopgezet wegens geen resultaat.
- Chemo: Taxotere tegenover Mitoxantrone in combinatie met prednison - verlengt leven van prostaatkankerpatiënten met gemiddeld drie maanden, maar chemo bij prostaatkanker is geen effectieve behandeling



Plaats een reactie ...
Reageer op "Docetaxel geeft naast hormoontherapie betere overleving bij hoog risico of uitgezaaide prostaatkanker met Gleasonscore van 8 tot 10 bij diagnose maar wel ten koste van kwaliteit van leven door bijwerkingen"