Aan dit artikel is vele uren gewerkt. Opzoeken, vertalen, op de website plaatsen enz. Als u ons wilt ondersteunen dan kan dat via een al of niet anonieme donatie. Elk bedrag is welkom hoe klein ook. Klik hier als u ons wilt helpen kanker-actueel online te houden. Wij zijn een ANBI organisatie en dus is uw donatie in principe aftrekbaar voor de belasting.
3 september 2017: Bron: Clinical Cancer Research
Immuuntherapie met dendritische cellen en een speciaal daarvoor geprepareerd vacin, VACCELL genoemd geeft uitstekende resultaten op overall overleving en progressievrije ziekte bij patiënten met inoperabele gevorderde alvleesklierkanker. Wanneer aan die behandeling ook nog extra verschillende WT peptides (WT = Wilms tumor) worden toegevoegd worden de resultaten nog beter. Uit de laatste studie met 10 patiënten met inoperabele uitgezaaide alvleesklierkanker stadium IV en 1 patiënt met in lever uitgezaaide galwegenkanker bereikten 7 van de 11 een remissie en maar liefst drie patiënten een duurzame complete remissie (klinisch kankervrij) van mediaan 717 dagen = 6 jaar). En niet toevallig alle drie de patiënten hadden een sterk verhoogde huidreactie na de injecties met het vaccin. De patienten waren geselecteerd uit een grotere studie.
De gegevens komen uit een reviewstudie: Dendritic cell-based vaccine for pancreatic cancer in Japan die als volledig studierapport in deze PDF gratis is te lezen:
Onder schema meer informatie over de studies bij alvleesklierkanker:
Figure 1. Induction of WT1-specific CD4+ and CD8+ T cell responses by dendritic cells pulsed with MHC class I/II restricted multiple WT1 peptides.......
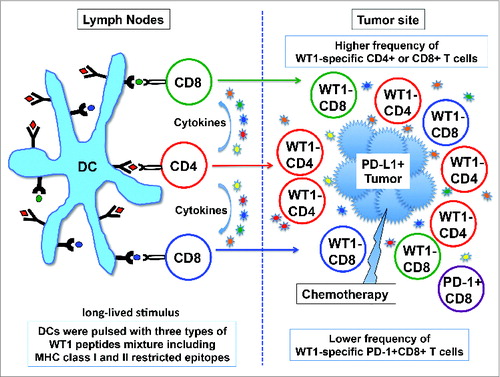 Figure 1
Figure 1
Vaccell is een vaccin gemaakt van dendritische cellen gehaald uit de monocyten van het bloed van de patiënt plus OK-432 toegevoegd in het laboratorium. Wanneer deze dendritische cellen dan als vaccin worden teruggebracht bij de patiënten worden er verschillende extra immuunstimulerende peptides, in dit geval WT - Wilms tumor peptides, aan toegevoegd om zo te komen tot een optimaal werkend vaccin:
Onder het plaatje een uitleg wat “optimized” betekent?
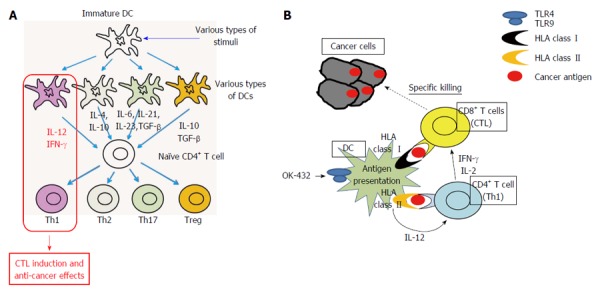
The DCs play central roles in deciding the direction of host immune reactions as well as antigen presentation. The DCs are “headquarters” of antigen-specific host immune responses[10,11]. The antigen presentation have to be done under the helper T-cell 1 (Th1) condition that is interferon (IFN)- and interleukin (IL)-12-rich condition for inducing antigen-specific cytotoxic T lymphocytes (CTLs) and eliciting anti-cancer effects (Figure (Figure1A),1A), however it is difficult to predict what kinds of immune responses, e.g., Th1, Th2, Th17 and regulatory T cells (Treg), will be induced by the dendritic cells in patients’ bodies. This is the serious problem of the conventional cancer vaccines which are the methods only using cancer antigens such as peptides, proteins and whole cells without DCs. The strategy to perform “optimization” of DCs in Th1-inducing type by processing DCs ex vivo should be reasonable.
De resultaten uit de eerste studie bij 49 patiënten waarbij dendritische celtherapie werd gecombineerd met S-1 een vorm van chemo vergelijkbaar met xeloda - capecitabine en LAK behandeling ( = lymphokine-activated killer): Clinical and immunologic evaluation of dendritic cell-based immunotherapy in combination with gemcitabine and/or S-1 in patients with advanced pancreatic carcinoma:
Resultaten:
Van de 49 patiënten (allemaal voorbehandeld met chemo en in vergevorderd stadium, bereikten alsnog 2 patiënten een CR = Complete Remissie (klinisch kankervrij), 5 bereikten een gedeeltelijke remissie (PR = Partial Remission = 50% of meer vermindering in tumor aantal en omvang) en 10 patiënten bereikten stabiele ziekte (SD). Levensverlenging in de groep van de dendritische cellen was veel beter (mediane overleving 3 jaar) in vergelijking met de controlegroep van alleen standaard behandeling. Overleving van patiënten die naast chemo en dendritische cellen ook nog aanvullend op de dendritische cellen een LAK behandeling (LAK = lymphokine-activated killer) kregen was langer dan zonder LAK behandeling. Geen van de patiënten ervaarde bijwerkingen met een graad 3 of ernstiger. (volledige abstract staat onder artikel).
De resultaten uit deze recente studie waarin 11 patiënten werden behandeld met een zo optimaal mogelijk geprepareerd vaccin: Treatment with Chemotherapy and Dendritic Cells Pulsed with Multiple Wilms' Tumor 1 (WT1)–Specific MHC Class I/II–Restricted Epitopes for Pancreatic Cancer zijn nog indrukwekkender.
Uit de resultaten geciteerd:
De combinatie behandeling werd goed verdragen....... De WT1-specifieke DTH-positieve patiënten (delayed-type hypersensitivity) toonden een statistisch significante betere overall overleving (OS) en progressie-vrije overleving (PFS) vergeleken met de patiënten met een negatieve DTH. In het bijzonder alle drie de patiënten met een sterke DTH bereikten een mediane overall overleving (OS) van 717 dagen.
Hier de karakteristieken van de deelnemende patienten:
Patient characteristics
| WT1 peptide–specific DTH | |||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| A*02:01 | A*24:02 | DRB1/DPB1 | |||||||||||||||||||||||||||
| HLA genotype | Vaccine times | Vaccine times | Vaccine times | ||||||||||||||||||||||||||
| Patient | Sex | Age, y | UICC stage | Location | Metastases | Prior systemic treatment | HLA-A | DRB1 | DPB1 | Vaccine | Times | 0 | 2 | 4 | 6 | 8 | 0 | 2 | 4 | 6 | 8 | 0 | 2 | 4 | 6 | 8 | |||
| PDA-01 | M | 41 | IV | PDA (body–tail) | Bone, LN | No | 02:01 | — | 08:03 | 12:01 | 02:02 | 15:01 | DC/WT1-I | 19 | − | − | − | − | − | − | − | − | − | − | − | − | − | − | − |
| PDA-02 | M | 69 | IV | PDA (body–tail) | Lung, peritonitis, LN | No | 24:02 | 26:01 | 12:01 | 15:02 | 05:01 | 09:01 | DC/WT1-I | 11 | − | − | − | − | − | − | − | − | − | − | − | − | − | − | − |
| PDA-03 | M | 73 | IV | PDA (head) | Peritonitis | No | 26:03 | 33:03 | 08:02 | 08:03 | 02:02 | 05:01 | DC/WT1-II | 13 | − | − | − | − | − | − | − | − | − | − | − | − | − | − | − |
| ICC-01 | F | 58 | IV | ICC | Peritonitis, LN | No | 02:01 | 24:02 | 04:05 | 15:02 | 09:01 | — | DC/WT1-I | 15 | − | + | + | + | + | − | + | ++ | ++ | ++ | − | − | − | − | − |
| PDA-04 | M | 70 | IV | PDA (body) | Peritonitis | No | 02:01 | 24:02 | 04:05 | 15:02 | 05:01 | 09:01 | DC/WT1-I/II | 35 | − | + | ++ | ++ | ++ | − | + | ++ | ++ | ++ | − | + | ++ | ++ | ++ |
| PDA-05 | M | 68 | IV | PDA (body) | Liver, LN | Ope, Cx | 24:02 | 33:03 | 08:03 | 13:02 | 02:02 | 04:01 | DC/WT1-I/II | 46 | − | − | − | − | − | − | + | ++ | ++ | ++ | − | + | ++ | ++ | ++ |
| PDA-06 | F | 49 | IV | PDA (head) | Liver, peritonitis, LN | No | 02:01 | 24:02 | 04:05 | 09:01 | 02:02 | 05:01 | DC/WT1-I/II | 7 | − | − | − | − | N.D. | − | − | − | − | N.D. | − | − | − | − | N.D. |
| PDA-07 | M | 35 | IV | PDA (body) | Liver, LN | No | 02:01 | — | 09:01 | 15:01 | 02:01 | 05:01 | DC/WT1-I/II | 6 | − | − | − | − | N.D. | − | − | − | − | N.D. | − | − | − | − | N.D. |
| PDA-08 | F | 72 | IV | PDA (body) | Peritonitis, LN | No | 02:06 | 24:02 | 08:02 | 12:01 | 02:01 | 05:01 | DC/WT1-I/II | 14 | − | − | − | − | − | − | − | − | − | − | − | − | − | − | − |
| PDA-09 | F | 69 | IV | PDA (body–tail) | LN | No | 24:02 | 33:03 | 13:02 | 15:01 | 04:01 | 13:01 | DC/WT1-I/II | 44+ | − | − | − | − | − | − | + | ++ | ++ | ++ | − | + | ++ | ++ | ++ |
| PDA-10 | M | 39 | IV | PDA (head–body) | Peritonitis | Ope | 02:10 | 24:02 | 15:01 | 15:02 | 02:02 | 09:01 | DC/WT1-I/II | 20 | − | − | − | − | − | − | − | + | + | + | − | − | + | + | + |
Abbreviations: Cx, chemotherapy; DTH -, erythema <1 mm; DTH +, erythema 2- 5 mm; DTH ++, erythema > 5 mm; LN, lymph nodes; N.D., not done; Ope, operation.
Het abstract van bovenstaande studie staat onderaan dit artikel.
Beide studies komen uit een reviewstudie: Dendritic cell-based vaccine for pancreatic cancer in Japan die als volledig studierapport in deze PDF gratis is te lezen.
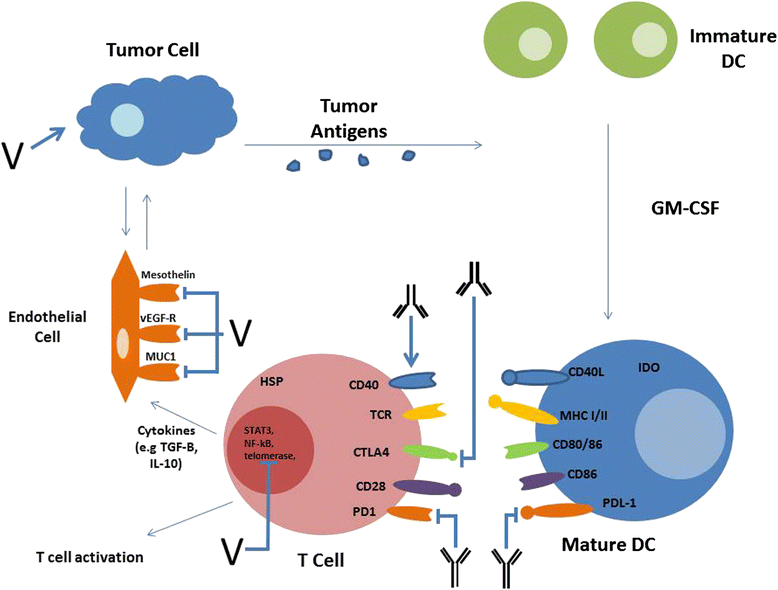
Een ander interessant studierapport over immuuntherapie bij alvleesklierkanker waaruit bovenstaand schema komt is dit studierapport: From bench to bedside a comprehensive review of pancreatic cancer immunotherapy. Gratis in te zien.
De beschrijvingen in de studierapporten zijn in voor mij te ingewikkeld medisch Engels uitgelegd en ik ga me dan ook maar niet wagen aan vertalingen. Ik denk wel dat als u de studierapporten mee neemt naar uw behandelend arts deze er zeker uitleg over kan geven.
Of print alleen de referentielijst uit die onderaan abstract en artikel staat.
Dendritic cell vaccine-based immunotherapy combined with chemotherapy was shown to be safe and possibly effective in patients with advanced pancreatic cancer refractory to standard treatment.
Clinical and immunologic evaluation of dendritic cell-based immunotherapy in combination with gemcitabine and/or S-1 in patients with advanced pancreatic carcinoma.
Abstract
OBJECTIVES:
In the current study, we have evaluated the clinical and immunological responses in patients with advanced pancreatic carcinoma who received dendritic cell (DC)-based immunotherapy in combination with gemcitabine and/or S-1.
METHODS:
Dendritic cell-based immunotherapy (DC vaccine alone or DC vaccine plus lymphokine-activated killer cell therapy) in combination with gemcitabine and/or S-1 has been carried out in 49 patients with inoperable pancreatic carcinoma refractory to standard treatment.
RESULTS:
Of 49 patients, 2 patients had complete remission, 5 had partial remission, and 10 had stable disease. Prolongation of survival in this cohort was highly likely (median survival, 360 days). Survival of patients receiving DC vaccine and chemotherapy plus LAK cell therapy was longer than those receiving DC vaccine in combination with chemotherapy but no LAK cells. Increased numbers of cancer antigen-specific cytotoxic T cells and decreased regulatory T cells were observed in several patients on immunotherapy, but increased overall survival time tended to be associated only with the latter. None of the patients experienced grade 3 or worse adverse events during the treatment period.
CONCLUSIONS:
Dendritic cell vaccine-based immunotherapy combined with chemotherapy was shown to be safe and possibly effective in patients with advanced pancreatic cancer refractory to standard treatment.
- PMID:
- 21792083
- DOI:
- 10.1097/MPA.0b013e31822398c6
- [Indexed for MEDLINE]
Plaats een reactie ...
2 Reacties op "Dendritische celtherapie naast chemo met Vaccell vaccin en aanvullende WT peptides geeft veel betere overleving en progressievrije tijd bij alvleesklierkankerpatienten"
Gerelateerde artikelen
- Eerste patient met alvleesklierkanker met immuuntherapie via Car-T cellen behandeld.
- Immuuntherapie met CAN-2409, een gemodiciceerd herpes simplex virus plus valaciclovir naast chemoradiotherapie geeft betere ziektevrije overleving na alsnog operatie bij patienten met alvleesklierkanker
- Casper van Eyck roemt vogelgriepvirus - New Castle disease virus in de documentaire Tegengif en gaat dit verder onderzoeken bij alvleesklierkanker
- KRAS gemuteerde tumoren: Kankervaccin ELI-002 2P stimuleerde hoge T-celreacties bij patiënten met voor immuuntherapie ongevoelige KRAS-gemuteerde tumoren en verbeterde de ziekteprogressieve tijd bij patienten met alvleesklierkanker en darmkanker copy 1
- mRNA vaccin met autogene cevumeran naast atezolizumab en mFolferinox geeft veelbelovende resultaten bij operabele niet uitgezaaide alvleesklierkanker.
- Advexin, een vorm van gentherapie geeft opvallend positieve resultaten bij patiënten met vergevorderde alvleesklierkanker. Artikel geplaatst 24 mei 2006
- Combinatie van chemo - gemcitabine en nab-paclitaxel met CD40 anti lichaam APX005M en immuuntherapie met anti-PD medicijn nivolumab slaat uitstekend aan bij nog niet behandelde alvleesklierkankerpatienten.
- Dendritische celtherapie naast chemo met Vaccell vaccin en aanvullende WT peptides geeft veel betere overleving en progressievrije tijd bij alvleesklierkankerpatienten
- Herceptin - trastuzumab: Laboratorium studies en dierstudies geven goed effect van Herceptin in combinatie met gemcitabine en/of docetaxel bij inoperabele alvleesklierkanker copy 1
- Immuuntherapie met gemoduleerde T-cellen gericht op specifiek eiwit heeft succes bij vrouw met uitgezaaide alvleesklierkanker en remissie duurt al drie jaar.
- Interferon toegevoegd aan chemo en bestraling verlengt leven van geselecteerde patienten met alvleesklierkanker
- PEGPH20 eiwit - hyaluron en gemcitabine zorgt voor veel langere progressievrije ziekte en een verdriedubbeling - 175 vs 529 dagen - van mediane overleving bij uitgezaaide alvleesklierkanker met hoge niveaus van hyaluronzuur
- Immuuntherapie bij alvleesklierkanker: een overzicht



Bedankt
Will
Mijn mama heeft pancreaskanker met uitzaaiingen in de lever.
(Sinds eind juli)
Bij wie kan ze terecht voor deze behandeling?
Kan er iemand mij hierbij helpen aub?
Alvast bedankt!
Gitte Cuvillier
Gitte.cuvillier@hotmail.com