Mocht u kanker-actueel de moeite waard vinden en ons willen ondersteunen om kanker-actueel online te houden dan kunt u ons machtigen voor een periodieke donatie via donaties: https://kanker-actueel.nl/NL/donaties.html of doneer al of niet anoniem op - rekeningnummer NL79 RABO 0372931138 t.n.v. Stichting Gezondheid Actueel in Amersfoort. Onze IBANcode is NL79 RABO 0372 9311 38
Elk bedrag is welkom. En we zijn een ANBI instelling dus uw donatie of gift is in principe aftrekbaar voor de belasting.
En als donateur kunt u ook korting krijgen bij verschillende bedrijven:
16 januari 2018: Lees ook dit artikel
12 mei 2016: lees ook dit artikel die de resultaten uit onderstaande studies bevestigt:
19 april 2016: Bron: American Association for Cancer Research (AACR) 2016
Immuuntherapie met nivolumab en ipilimumab, maar ook immuuntherapie met alleen nivolumab geeft onvoorstelbaar goede resultaten op 5-jaars overleving. Deze resultaten komen uit verschillende fase II studies die allemaal nagenoeg dezelfde resultaten laten zien. Een verdubbeling van mediaan 34% van mensen die met uitgezaaide vergevorderde melanomen alsnog of een combinatie van ipilimumab plus nivolumab kregen of een behandeling met alleen nivoilumab - soms was maar 1 behandeling met nivolumab nodig!. Let wel dit zijn allemaal patienten die al vele andere behandelingen hebben gehad voordat zij nivolumab kregen aangeboden.
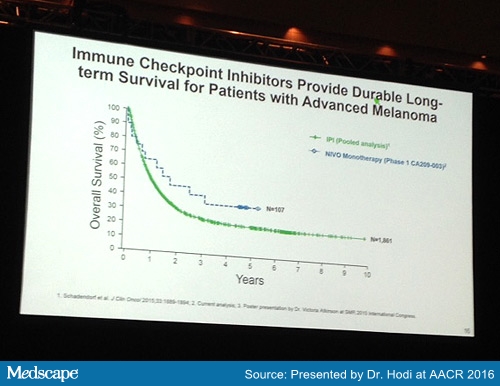
The 5-year OS rate of 34% with nivolumab is more than double what can be expected in this patient population ― data from the National Cancer Institute's SEER database show a 5-year OS rate of 16.6% for patients with metastatic melanoma diagnosed from 2005 to 2011.
Onderaan dit artikel staan de abstracten die op de AACR werden gepresenteerd afgelopen week. Waarvan 1 abstract geeft de resultaten van de studie zoals hieronder beschreven uit mei 2013
These data come from the phase 2 checkmate 069 trial, in which 95 patients received the combination, and 47 received nivolumab alone. Previously, superior response rates and progression-free survival had been reported for the combination. Now, OS has also been shown to be superior.
An exploratory analysis shows the OS rate at 2 years to be 69% with the combination vs 53% with nivolumab alone in patients with BRAF wild-type melanoma.
Discussing the presentation, Padmanee Sharma, MD, from the University of Texas MD Anderson Cancer Center, in Hosuton, compared this 2-year OS of 69% achieved with the combination therapy against data from previous studies, which showed a 2-year OS of 54% with ipilimumab alone and of 57% with nivolumab alone.
However, she noted that with the combination, the rate of adverse events was higher, with grade 3/4 toxicity reported in 55% of patients receiving the combination vs 22% receiving nivolumab alone.
| NIVO 3 mg/kg (n=17) |
All Patients (N=107) |
|
| OS rate, % (95% CI)* | ||
| 12-month | 64.7 (37.7-82.3) | 62.7 (52.6-71.2) |
| 24-month | 47.1 (23.0-68.0) | 48.0 (38.1-57.2) |
| 36-month | 41.2 (18.6-62.6) | 42.1 (32.4-51.4) |
| 48-month | 35.3 (14.5-57.0) | 34.8 (25.7-44.1) |
| 60-month | 35.3 (14.5-57.0) | 33.6 (24.6-42.9) |
| Median OS, months (95% CI) | 20.3 (7.2-NR) | 17.3 (12.5-37.8) |
| *Based on Kaplan-Meier estimates. NR, not reached. |
16 mei 2013: Bron: ASCO 2013
Een combinatie van twee immuuntherapeutische medicijnen - behandelingen met ipilimumab (Yervoy) en nivolumab (Bristol-Myers Squibb), gelijktijdig gegeven, geeft spectaculaire resultaten in een fase I studie bij melanoompatiënten met vergevorderde, uitgezaaide en vooraf intensief behandelde ziekte.
Bij circa de helft (17 patiënten) van de totaal 86 deelnemende patiënten aan deze fase I studie met verschillende groepen, die de gelijktijdige behandeling kregen en de hoogste dosis, werden de tumoren significant verkleind (tumorreductie van minimaal 80 procent) en die respons duurde ook de hele studietijd. Daarmee lijkt een nieuwe optie te komen voor de behandeling van uitgezaaide melanomen, aldus hoofdauteur Jedd Wolchok, MD, PhD, van het Memorial Sloan-Kettering Cancer Center, in New York op een pers bijeenkomst voorafgaande aan ASCO 2013 dat 2 juni a.s. van start gaat.
De objectieve respons bij het gelijktijdig gebruik van de 2 immuuntherapeutische behandelingen was significant hoger dan de respons wanneer de afzonderlijke medicijnen alleen als immuunbehandeling werden ingezet. In de nieuwe fase I studie, om de dosis en de veiligheid vast te stellen, werden maximale doses van ipilimumab (3 mg / kg per dag) en nivolumab (1 mg / kg per dag) gebruikt, indien zij gelijktijdig werden gegeven en deze maximale dosis leverde een objectieve respons - de medicijnen gaven een therapeutisch effect - op van 53% bij 17 patiënten. In eerder gepubliceerde studies, werd een objectieve respons gezien van 11% voor ipilimumab en 41% voor nivolumab.
De combinatie van ipilimumab / nivolumab gelijktijdige te geven zal nu worden getest in fase III studies als eerstelijns behandeling voor patiënten met uitgezaaide melanoom, te beginnen in juni 2013, aldus Dr Wolchok.
Totaal 52 van de 86 patiënten in de fase 1 studie kregen deze combinatie behandeling in verschillende groepen met verschillende doses. 90% van deze patiënten blijken vanaf februari 2013 met een voortdurende respons te reageren op de combinatiebehandeling met maximale dosis. Alle patiënten in deze studie hebben een inoperabel stadium III en stadium IV (gemetastaseerd) melanoom en hadden vooraf aan deze studie minimaal 3 voorafgaande behandelingen met chemo ondergaan.
De maximale dosering van deze combinatie behandeling produceert "snelle en vergaande" resultaten, zegt Dr Wolchok. 7 van de 17 patiënten (41%) van deze patiënten had meer dan een 80% tumor reductie binnen 3 maanden. Dus ongeveer een derde van alle patiënten in de studiegroep van de gelijktijdig gegeven combinatiebehandeling met ipilimumab (Yervoy) en nivolumab (Bristol-Myers Squibb), hadden minimaal een 80% tumorreductie."
"Dit is echt opmerkelijk. Dit soort reactie is nog niet eerder gezien met immuuntherapie voor melanomen," zegt Sandra Swain, MD, voorzitter van ASCO, die niet was betrokken bij de studie, maar wel als commentator optrad op de persbriefing. Ze is werkzaam in het Washington Cancer Institute, in Washington, DC.
"Deze studie is een bewijs van het principe dat gelijktijdig gebruik van 2 immuuntherapeutische middelen bepaalde antistoffen bevat die als voorbeeld aanpak kunnen dienen voor een behandeling van gevorderde melanoom. Dit is heel spannend," aldus Sandra Swain, MD.
Beide medicijnen behoren tot een nieuwe klasse van geneesmiddelen de zogeheten "immune checkpoint blokkade", wat betekent dat ze gericht worden op de poortwachters van het immuunsysteem, op receptoren van de immuuncellen en "verlaagt de remkracht" van het menselijke afweersysteem om actief kankercellen aan te vallen, zegt Dr Wolchok. Ipilimumab blokkeert de CTLA-4, terwijl nivolumab zich richt op het eiwit PD-1. "Door zowel het blokkeren van CDLA-4 als PD-1 zorgen deze voor een verbeterde activatie van de immuuncel," aldus Dr. Wolchock.
De volledige respons was 17% bij de patiënten die de ipilimumab / nivolumab gelijktijdig als behandeling kregen bij de maximale doseringen. Echter, onder alle patiënten in de studie, met inbegrip van degenen die de medicijnen niet gelijktijdig maar opeenvolgend kregen, bleek de volledige respons ongeveer 10% te zijn, aldus dr. Wolchock. In beide gevallen bleek de volledige respons ca. 3% beter voor gelijktijdig geven dan als de 2 medicijnen alleen werden ingezet (dit gold voor zowel ipilimumab als nivolumab met ca. 3% verschil), aldus Dr Wolchok. (Red: bedenk hierbij dat alle patiënten vergevorderde intensief vooraf behandelde uitgezaaide melanoom hadden)
Omdat er nog niet genoeg recidieven of stoppen met de behandeling te melden zijn, is er nog geen mediane tijd tot een recidief in de fase 1 studie vast gesteld. Geen van de patiënten die deze immuuntherapie ondergaan ervaren een vorm van resistentie tot nu toe door deze nieuwe gerichte therapieën voor melanoom zoals bij vemurafenib wel wordt gezien, aldus Dr Wolchok. De combinatie van ipilimumab en nivolumab wordt ook getest en onderzocht bij niet kleincellige longkanker en niercelcarcinoom.
Bijwerkingen zijn beheersbaar:
Voor alle doses gold een studieprotocol voor de patiënten die de medicijnen nivolumab en ipilimumab gelijktijdig zouden krijgen van elke 3 weken 4 doses van beide medicijnen, gevolgd door alleen nivolumab elke 3 weken met 4 doses. Dan vanaf week 24, wordt een gelijktijdige combinatie behandeling toegediend om de 3 maanden.
Graad 3-4 bijwerkingen als gevolg van behandeling traden op bij 28 van de 53 patiënten (53%) bij de groepen die een gelijktijdige behandeling kregen. De bijwerkingen waren meestal gerelateerd aan immuunreactie gerelateerde ontstekingen. De meest voorkomende asymptomatisch laboratorium afwijkingen waren: verhogingen in het bloed van lipase (13%) en de leverenzymen AST (13%) en ALT (11%).
In de groepen die een gefaseerde behandeling kregen, was de toxiciteit minder ernstig. Graad 3-4 bijwerkingen als gevolg van behandeling traden op bij 6 van de 33 patiënten (18%). De meest voorkomende was asymptomatische verhoging van lipase (6%).
(Red: Wat is lipase? Lipase wordt door de alvleesklier (pancreas) gemaakt en wordt via de alvleesklierbuis naar de twaalfvingerige darm vervoerd. Lipase is een enzym. Een enzym is een eiwit dat een bepaalde stof kan omzetten in een andere stof. In de darm helpt lipase bij de omzetting van vet uit het voedsel, zodat de opname makkelijker wordt. Lipase komt normaal in kleine hoeveelheden voor in het bloed. Wanneer de alvleesklier beschadigd is of de alvleesklierbuis verstopt is, zal de hoeveelheid lipase in het bloed toenemen)
De bijwerkingen bij zowel de gelijktijdige als gefaseerde behandeling waren beheersbaar met behulp van standaard aanpak, aldus Dr Wolchok. Er waren geen behandelings gerelateerde sterfgevallen.
Dr Wolchok: "We waren niet verrast door de ernst van de bijwerkingen of door iets nieuws, de bijwerkingen waren niet slechter, niet frequenter dan wanneer de geneesmiddelen alleen worden gegeven."
De studie werd uitgevoerd met financiële stuen van Bristol-Myers Squibb. Dr Wolchok meldt dat hij als adviseur is verbonden aan Bristol-Meyers Squibb. Mede auteurs zijn eveneens werknemers van het bedrijf.
Het abstract van bovengenoemde studie: Safety and clinical activity of nivolumab (anti-PD-1, BMS-936558, ONO-4538) in combination with ipilimumab in patients (pts) with advanced melanoma (MEL) kunt u vinden op de website van de American Society of Clinical Oncology (ASCO) 2013. Maar staat ook hieronder:
Combination immunotherapy with ipilimumab and the antibody drug nivolumab has broken new ground in the treatment of metastatic melanoma, producing durable tumor shrinkage >80% - in about half of patients.
Source: ASCO 2013:
Safety and clinical activity of nivolumab (anti-PD-1, BMS-936558, ONO-4538) in combination with ipilimumab in patients (pts) with advanced melanoma (MEL).
Citation:
J Clin Oncol 31, 2013 (suppl; abstr 9012^)
Author(s): Jedd D. Wolchok, Harriet M. Kluger, Margaret K. Callahan, Michael Andrew Postow, Ruth Ann Gordon, Neil Howard Segal, Naiyer A. Rizvi, Alexander M. Lesokhin, Kathleen Reed, Matthew M. Burke, Anne Caldwell, Stephanie Anne Kronenberg, Blessing Agunwamba, William Feely, Quan Hong, Christine E. Horak, Alan J. Korman, Jon M. Wigginton, Ashok Kumar Gupta, Mario Sznol; Memorial Sloan-Kettering Cancer Center, New York, NY; Yale School of Medicine; Yale Cancer Center, New Haven, CT; Memorial-Sloan Kettering Cancer Center, New York, NY; Bristol-Myers Squibb, Princeton, NJ; Bristol-Myers Squibb, Redwood City, CA
Abstract:
Background: CTLA-4 and PD-1 are critical immune checkpoint receptors. In MEL pts, ipilimumab (anti-CTLA-4) prolonged survival in two phase III trials, and nivolumab (anti-PD-1) produced an objective response rate (ORR) of 31% (n=106) in a phase I trial. PD-1 is induced by CTLA-4 blockade, and combined blockade of CTLA-4/PD-1 showed enhanced antitumor activity in murine models. Thus, we initiated the first phase 1 study to evaluate nivolumab/ipilimumab combination therapy.
Methods: MEL pts with ≤3 prior therapies received IV nivolumab and ipilimumab concurrently, q3 wk × 4 doses, followed by nivolumab alone q3 wk × 4 (Table). At wk 24, combined treatment was continued q12 wk × 8 in pts with disease control and no DLT. In two sequenced-regimen cohorts, pts with prior standard ipilimumab therapy were treated with nivolumab (q2 wk × 48).
Results: As of Dec. 6, 2012, 69 pts were treated. We report efficacy data on 37 pts with concurrent therapy in completed cohorts 1-3 (Table); ORR was 38% (95% CI: 23-55). In cohort 2 (MTD), ORR was 47% and 41% of pts had ≥80% tumor reduction at 12 wk (Table) with some pts showing rapid responses, prompt symptom resolution, and durable CRs. Related adverse events (rAEs) for concurrent therapy were similar in nature with some higher in frequency than those typically seen for the monotherapies and were generally manageable using immunosuppressants. Cohort 3 exceeded the MTD (DLT: gr 3-4 ↑ lipase). At the MTD, gr 3-4 rAEs occurred in 59% of pts and included uveitis/choroiditis, colitis, and reversible lab abnormalities.
Conclusions: Nivolumab and ipilimumab can be combined with a manageable safety profile. Clinical activity for concurrent therapy appears to exceed that of published monotherapy data, with rapid and deep tumor responses (≥80% tumor reduction at 12 wk) in 30% (11/37) of pts. A phase III trial is planned to compare concurrent combination dosing with each monotherapy. Clinical trial information: NCT01024231.
| Cohort | Ipilimumab (mg/kg) + nivolumab (mg/kg) | na | CRb (n) | PRb (n) | ORR (%) [95% CI] | ≥80% Tumor reduction at 12 wk (%) |
|---|---|---|---|---|---|---|
| 1 | 3 + 0.3 | 14 | 1 | 2 | 21 [5-51] | 4/14 (29) |
| 2 | 3 + 1 | 17 | 3 | 5 | 47 [23-72] | 7/17 (41) |
| 3 | 3 + 3 | 6 | 0 | 3 | 50 [12-88] | 0/6 (0) |
| 2a | 1 + 3 | 12 | Ongoing | |||
| 6 | Prior + 1 | 14 | Ongoing | |||
| 7 | Prior + 3 | 6 | Ongoing | |||
Total treated; bmWHO criteria.
Initial report of overall survival rates from a randomized phase II trial evaluating the combination of nivolumab (NIVO) and ipilimumab (IPI) in patients with advanced melanoma (MEL)
| Abstract Number: | CT002 |
| Presentation Title: | Initial report of overall survival rates from a randomized phase II trial evaluating the combination of nivolumab (NIVO) and ipilimumab (IPI) in patients with advanced melanoma (MEL) |
| Presentation Time: | Sunday, Apr 17, 2016, 2:15 PM - 2:35 PM |
| Location: | La Nouvelle Orleans Ballroom, Morial Convention Center |
| Webcast Status: | Webcast Available |
| Webcast Permission: | Agree to participate including all slides |
| Author Block: | Michael Postow1, Jason Chesney2, Anna Pavlick3, Caroline Robert4, Kenneth Grossmann5, David McDermott6, Gerald Linette7, Nicolas Meyer8, Jeffrey Giguere9, Sanjiv Agarwala10, Montaser Shaheen11, Marc Ernstoff12, David Minor13, April Salama14, Matthew Taylor15, Patrick Ott16, Joel Jiang17, Christine Horak17, Paul Gagnier17, Jedd Wolchok1, F. Stephen Hodi16. 1Memorial Sloan Kettering Cancer Center, New York, NY; 2J. Graham Brown Cancer Center, University of Louisville, Louisville, KY; 3Laura and Isaac Perlmutter Cancer Center, NYU Langone Medical Center, New York, NY; 4Gustave Roussy and INSERM U981, Villejuif-Paris-Sud, France; 5Huntsman Cancer Institute, University of Utah, Salt Lake City, UT; 6Beth Israel Deaconess Medical Center, Boston, MA; 7Washington University School of Medicine, St. Louis, MO; 8Toulouse University Cancer Institute, Toulouse, France; 9Greenville Health System, Seneca, SC; 10St. Luke's University Health Network, Bethlehem, PA; 11University of New Mexico, Albuquerque, NM; 12Cleveland Clinic, Cleveland, OH; 13California Pacific Medical Center Research Institute, San Francisco, CA; 14Duke University, Durham, NC; 15Oregon Health & Science University, Portland, OR; 16Dana-Farber Cancer Institute, Boston, MA; 17Bristol-Myers Squibb, Princeton, NJ |
| Abstract Body: | Background: This phase II trial (CheckMate 069) demonstrated a statistically significant improvement in objective response rate (ORR) and progression-free survival (PFS) with the combination of NIVO+IPI vs. IPI alone in treatment-naïve patients (pts) with BRAF wild-type MEL (Postow et al. N Engl J Med 2015;372:2006). ORR was 61% for NIVO+IPI vs 11% for IPI alone (P<0.0001). Here, we report updated efficacy data and the first overall survival (OS) results from this study. Methods: Pts (N=142) were randomized 2:1 (with stratification by BRAF mutation status) to receive either NIVO 1 mg/kg + IPI 3 mg/kg or IPI 3 mg/kg + placebo every 3 weeks x 4 doses, followed by NIVO 3 mg/kg or placebo, respectively, every 2 weeks until disease progression or unacceptable toxicity. The primary endpoint was investigator-assessed ORR in pts with BRAF wild-type tumors. Secondary endpoints included PFS in pts with BRAF wild-type tumors, ORR in pts with BRAF V600 mutation-positive tumors, and safety. OS was an exploratory endpoint. The most recent database lock occurred in August of 2015, representing a minimum follow-up of 18 months. Results: In the current analysis, median PFS in BRAF wild-type pts had not yet been reached with the NIVO+IPI combination and was 4.3 months for IPI alone (hazard ratio : 0.34; 95% confidence interval : 0.20-0.57; P<0.0001). The 12- and 18-month PFS rates were, respectively, 55.1% and 53.4% for NIVO+IPI vs. 16.2% and 8.1% for IPI alone. At 18 months of follow-up, OS rates in BRAF wild-type pts were 73% for NIVO+IPI vs. 56% for IPI alone, and median OS had not been reached in either group (HR: 0.56; 95% CI: 0.29-1.10; P=0.089). While 26 of 46 pts (57%) randomized to the IPI group had crossed over to receive NIVO alone upon disease progression, sensitivity analyses showed similar OS results when these pts were censored. In all randomized pts, median change from baseline in target lesions was a 70% reduction for NIVO+IPI vs. a 5% increase for IPI alone. Median duration of response was not reached in either group. Grade 3-4 treatment-related adverse events were reported more frequently with NIVO+IPI (55%) than with IPI alone (22%), and led to discontinuation in 30% and 9% of pts, respectively. Treatment-related select AEs in the combination arm were consistent with the initial report and most resolved with immune-modulating medications (>85% across organ categories). Conclusions: In this updated analysis, NIVO+IPI continued to show improved PFS vs. IPI alone, with an apparent plateau after 12 months in the combination group. At 18 months of follow-up, there was a trend toward higher OS rates in pts who received combination therapy. Further efficacy updates, including 2-year OS rates, will be presented according to BRAF mutation status and for all randomized pts. |
Durable, long-term survival in previously treated patients with advanced melanoma (MEL) who received nivolumab (NIVO) monotherapy in a phase I trial
| Abstract Number: | CT001 | |||||||||||||||||||||||||||
| Presentation Title: | Durable, long-term survival in previously treated patients with advanced melanoma (MEL) who received nivolumab (NIVO) monotherapy in a phase I trial | |||||||||||||||||||||||||||
| Presentation Time: | Sunday, Apr 17, 2016, 3:45 PM - 4:05 PM | |||||||||||||||||||||||||||
| Location: | La Nouvelle Orleans Ballroom, Morial Convention Center | |||||||||||||||||||||||||||
| Webcast Status: | Webcast Status Unknown | |||||||||||||||||||||||||||
| Author Block: | F. Stephen Hodi1, Harriet Kluger2, Mario Sznol2, Richard Carvajal3, Donald Lawrence4, Michael Atkins5, John Powderly6, William Sharfman7, Igor Puzanov8, David Smith9, Philip Leming10, Evan Lipson7, Janis Taube7, Robert Anders7, Christine Horak11, Joel Jiang11, David McDermott12, Jeffrey Sosman8, Julie Brahmer7, Drew Pardoll7, Suzanne Topalian7. 1Dana-Farber Cancer Institute, Boston, MA; 2Yale University School of Medicine and Smilow Cancer Center, Yale-New Haven Hospital, New Haven, CT; 3Columbia University Medical Center, New York, NY; 4Massachusetts General Hospital Cancer Center, Boston, MA; 5Georgetown-Lombardi Comprehensive Cancer Center, Washington, DC; 6Carolina BioOncology Institute, Huntersville, NC; 7The Sidney Kimmel Comprehensive Cancer Center at Johns Hopkins, Baltimore, MD; 8Vanderbilt University Medical Center, Nashville, TN; 9University of Michigan, Ann Arbor, MI; 10The Christ Hospital Cancer Center, Cincinnati, OH; 11Bristol-Myers Squibb, Princeton, NJ; 12Beth Israel Deaconess Medical Center, Boston, MA | |||||||||||||||||||||||||||
| Abstract Body: | Background: In previously treated MEL patients (pts), the results of an early phase I trial with NIVO monotherapy (CA209-003) demonstrated tumor responses that were durable even after treatment discontinuation (Topalian et al. J Clin Oncol 2014;32:1020). We report extended follow-up with 5-year overall survival (OS) data from this study. Methods: IPI-naïve pts (N=107) who had received 1-5 prior systemic therapies for MEL were treated with NIVO (0.1, 0.3, 1, 3, or 10 mg/kg) every 2 weeks for ≤96 weeks. Pts were followed for OS, progression-free survival (PFS), long-term safety, and response duration after discontinuing NIVO treatment. Pts began treatment in October 2008, and current data were analyzed in October 2015 with a minimum follow-up of 45 months (time from when the last pt received his or her first dose of NIVO). Results: Median age of the pts was 61 years, 67% were male, 97% had an ECOG performance status of 0 or 1, 62% had received ≥2 prior systemic therapies, and 36% had elevated lactate dehydrogenase levels at baseline. In all 107 pts, the 60-month OS rate was 34% (95% confidence interval : 25-43) and median OS was 17.3 months (95% CI: 12.5-37.8) (Table). OS rates appeared to plateau at ~48 months, although further follow-up is needed. Similar results were observed with NIVO at 3 mg/kg, the currently approved monotherapy dose (Table). At the last timepoint for tumor assessment, PFS rates at 30 months were 18.6% and 25.7% for all pts and those who received NIVO at 3 mg/kg, respectively. Conclusions: This analysis represents the longest survival follow-up of pts who received anti-PD-1 therapy in a clinical study. In this heavily pretreated population of MEL pts, these results suggest durable, long-term survival following NIVO monotherapy, with 34% of pts alive at 5 years. Characteristics of long-term survivors and updated safety data will also be presented.
|
|||||||||||||||||||||||||||
This analysis represents the longest survival follow-up of pts who received anti-PD-1 therapy in a clinical study. In this heavily pretreated population of Melanome patients, these results suggest durable, long-term survival following NIVO monotherapy, with 34% of patients alive at 5 years.
Source: ASCO 2016
| Abstract Number: | CT001 | |||||||||||||||||||||||||||
| Presentation Title: | Durable, long-term survival in previously treated patients with advanced melanoma (MEL) who received nivolumab (NIVO) monotherapy in a phase I trial | |||||||||||||||||||||||||||
| Presentation Time: | Sunday, Apr 17, 2016, 3:45 PM - 4:05 PM | |||||||||||||||||||||||||||
| Location: | La Nouvelle Orleans Ballroom, Morial Convention Center | |||||||||||||||||||||||||||
| Webcast Status: | Webcast Status Unknown | |||||||||||||||||||||||||||
| Author Block: | F. Stephen Hodi1, Harriet Kluger2, Mario Sznol2, Richard Carvajal3, Donald Lawrence4, Michael Atkins5, John Powderly6, William Sharfman7, Igor Puzanov8, David Smith9, Philip Leming10, Evan Lipson7, Janis Taube7, Robert Anders7, Christine Horak11, Joel Jiang11, David McDermott12, Jeffrey Sosman8, Julie Brahmer7, Drew Pardoll7, Suzanne Topalian7. 1Dana-Farber Cancer Institute, Boston, MA; 2Yale University School of Medicine and Smilow Cancer Center, Yale-New Haven Hospital, New Haven, CT; 3Columbia University Medical Center, New York, NY; 4Massachusetts General Hospital Cancer Center, Boston, MA; 5Georgetown-Lombardi Comprehensive Cancer Center, Washington, DC; 6Carolina BioOncology Institute, Huntersville, NC; 7The Sidney Kimmel Comprehensive Cancer Center at Johns Hopkins, Baltimore, MD; 8Vanderbilt University Medical Center, Nashville, TN; 9University of Michigan, Ann Arbor, MI; 10The Christ Hospital Cancer Center, Cincinnati, OH; 11Bristol-Myers Squibb, Princeton, NJ; 12Beth Israel Deaconess Medical Center, Boston, MA | |||||||||||||||||||||||||||
| Abstract Body: |
Background: In previously treated MEL patients (pts), the results of an early phase I trial with NIVO monotherapy (CA209-003) demonstrated tumor responses that were durable even after treatment discontinuation (Topalian et al. J Clin Oncol 2014;32:1020). We report extended follow-up with 5-year overall survival (OS) data from this study. Methods: IPI-naïve pts (N=107) who had received 1-5 prior systemic therapies for MEL were treated with NIVO (0.1, 0.3, 1, 3, or 10 mg/kg) every 2 weeks for ≤96 weeks. Pts were followed for OS, progression-free survival (PFS), long-term safety, and response duration after discontinuing NIVO treatment. Pts began treatment in October 2008, and current data were analyzed in October 2015 with a minimum follow-up of 45 months (time from when the last pt received his or her first dose of NIVO). Results: Median age of the pts was 61 years, 67% were male, 97% had an ECOG performance status of 0 or 1, 62% had received ≥2 prior systemic therapies, and 36% had elevated lactate dehydrogenase levels at baseline. In all 107 pts, the 60-month OS rate was 34% (95% confidence interval : 25-43) and median OS was 17.3 months (95% CI: 12.5-37.8) (Table). OS rates appeared to plateau at ~48 months, although further follow-up is needed. Similar results were observed with NIVO at 3 mg/kg, the currently approved monotherapy dose (Table). At the last timepoint for tumor assessment, PFS rates at 30 months were 18.6% and 25.7% for all pts and those who received NIVO at 3 mg/kg, respectively. Conclusions: This analysis represents the longest survival follow-up of pts who received anti-PD-1 therapy in a clinical study. In this heavily pretreated population of MEL pts, these results suggest durable, long-term survival following NIVO monotherapy, with 34% of pts alive at 5 years. Characteristics of long-term survivors and updated safety data will also be presented.
|
|||||||||||||||||||||||||||
Plaats een reactie ...
6 Reacties op "Immuuntherapeutische behandelingen met ipilimumab en nivolumab, gelijktijdig gegeven, geeft spectaculaire resultaten - 80 procent tumorreductie - bij melanoompatiënten met uitgezaaide vergevorderde vooraf intensief behandelde ziekte."
Gerelateerde artikelen
- Immuuntherapeutische behandelingen met ipilimumab en nivolumab, gelijktijdig gegeven, geeft spectaculaire resultaten - 80 procent tumorreductie - bij melanoompatiënten met uitgezaaide vergevorderde vooraf intensief behandelde ziekte.
- Immuuntherapie met Ipilimumab plus Nivolumab samen gegeven geeft uitstekende resultaten bij melanomen stadium 3 / 4 op 2 jaars overleving en verdubbelt complete remissies in vergelijking met alleen ipilimumab copy 1
- Nivolumab als enige behandeling geeft 34 procent 5 jaars overleving bij zwaar voorbehandelde melanoompatienten



Of ook oogmelanoom uitzaaiingen?
Een klein onderzoek heeft uitgewezen dat ipilimumab niet werkt bij een oogmelanoom, zie http://kanker-actueel.nl/NL/ipilimumab-geeft-geen-enkel-effect-bij-een-oogmelanoom.html maar het onderzoek was heel klein en er was van tevoren geen test gedaan op receptoren en mutaties dus volgens mij is het niet zeker dat ipilimumab niet ook bij een bepaalde groep van patiënten met een oogmelanoom werkzaam zou kunnen zijn. Informeer anders bij dr. Haanen in het AvL - Amsterdam?
Kees Braam
webmaster www.kanker-actueel.nl
Maar tegenwoordig kun je ook een melanoomtumor hebben in je darmen. Maar dat wordt dan bepaald door de DNA mutaties en receptorenexpressie. Vraag je behandelend arts hoe zo'n receptoren en DNA onderzoek aan te vragen.