12 september 2016: lees ook dit artikel: want wat zou er gebeuren als beide behandelingen van immuuntherapie, zie hieronder artikel van 4 augustus 2015, plus hyperthermie zouden worden gecombineerd?
4 augustus 2015: lees ook dit artikel:
4 augustus 2015: Bron: Exp Ther Med. 2015 Mar; 9(3): 1063–1067. Published online 2015 Jan 26. doi: 10.3892/etm.2015.2217
Wanneer patiënten met baarmoederhalskanker naast de standaard chemo ook dendritische celtherapie krijgen met aanvullende zogeheten DC-CIK - dendritische killercells dan hebben deze patiënten veel minder kans op een recidief en een veel grotere kans na drie jaar nog te leven te zijn in vergelijking met de patiënten die alleen chemo kregen.
Dit blijkt uit een gerandomiseeerde fase II studie bij totaal 79 patiënten met baarmoederhalskanker. 39 patiënten in de controlegroep en 40 patiënten in de studiegroep.
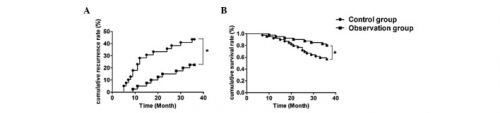
De cijfers van een optredend recidief waren in de controlegroep respectievelijk na 1 jaar 28,2% - 11 patiënten, na 2 jaar 35.9% - 14 patiënten en na drie jaar 46.2% - 18 patiënten.
In de studiegroep met de immuuntherapie waren deze cijfers respectievelijk: na 1 jaar 5% - 2 patiënten, na 2 jaar 15% (6 patiënten) en na drie jaar 22.5% - 9 patiënten.
De cijfers van de overall overleving waren: na 1 jaar 92.31% vs 97,25%, na 2 jaar 76.92 vs 90% en na drie jaar 56.41% vs 80%, respectieveljik voor controlegroep en studiegroep. Dit is statistisch significant: (P<0.05)
Een heel mooi resultaat dus, bij de huidige aanpak overleeft maar 20% tot maximaal 30% de 5 jaar,volgens statistische gegevens en het verbaast mij dat deze studie niet in een van de grote medische tijdschriften is gepubliceerd maar in het veel kleinere Experimental and Therapeutic Medicine. Terwijl de resultaten superieur zijn aan welke studie dan ook met welke chemo dan ook van de laatste 20 jaar. Alleen de immuuntherapeutische studie met een HPV gerelateerd vaccin, zie ander studie onder immuuntherapie in gerelateerde artikelen, geeft vergelijkbare resultaten.
En de patiëntenpopulatie uit beide groepen verschilde niet in leeftijd, stadium van de ziekte of anderszins. Dus een kwalitatief heel goed opgezette studie zo ver ik dat als leek kan beoordelen.
In de controlegroep waren 39 patiënten (leeftijd mediaan 51.9 met ±16.8 jaar verschillen) bij loting terecht gekomen: 30 patiënten hadden een type plaveisel carcinoom en negen patiënten had een type adenocarcinoma. Volgens de stadia classificaties van de International Federation of Gynecology and Obstetrics (FIGO) hadden 16 patiënten stadium IIa, 11 patiënten stadium IIb, 7 patiënten stadium IIIa, 4 patiënten stadium IIIb, en 1 patiënt met stadium IV.
De studiegroep bevatte na loting 40 patiënten (mediane leeftijd 52.4 met ±17.1 jaar verschillen), 31 patiënten hadden type plaveiselcarcinoom, 9 patiënten hadden type adenocarcinoom. Volgens de stadia classificaties van de International Federation of Gynecology and Obstetrics (FIGO) hadden 15 patiënten stadium IIa, 12 patiënten stadium IIb, 8 patiënten stadium IIIa, 4 patiënten stadium IIIb en 1 patiënt stadioum IV. er waren dus geen statische verschillen tussen de patiënten uit beide groepen in leeftijd, stadium van de ziekte of de mate van tumoraanwezigheid c.q. uitzaaiingen. (P>0.05).
Conclusie:
De onderzoekers concluderen dan ook: deze studie bevestigt de effectiviteit van biologische immuuntherapie, speciaal biologische immuuntherapie met chemotherapie in de behandeling van kwaadaardige tumoren en bewijst verder de noodzaak voor klinische toepassing van dendritische killercells bij de behandeling van specifiek baarmoederhalskanker.
Het volledige studierapport: Effectiveness of immune therapy combined with chemotherapy on the immune function and recurrence rate of cervical cancer is gratis in te zien. Met duidelijke heldere studieomschrijving en grafieken en mooie referentielijst.
Mocht u kanker-actueel de moeite waard vinden en ons willen ondersteunen om kanker-actueel online te houden dan kunt u ons machtigen voor een periodieke donatie via donaties: https://kanker-actueel.nl/NL/donaties.html of doneer al of niet anoniem op - rekeningnummer NL79 RABO 0372931138 t.n.v. Stichting Gezondheid Actueel in Amersfoort. Onze IBANcode is NL79 RABO 0372 9311 38
Elk bedrag is welkom. En we zijn een ANBI instelling dus uw donatie of gift is in principe aftrekbaar voor de belasting.
En als donateur kunt u ook korting krijgen bij verschillende bedrijven:
Hier het abstract van de studie:
This study confirmed the effectiveness of biological immune treatment, particularly biological immune treatment combined with chemotherapy, in the treatment of tumors, and provides further evidence to support its clinical application in the treatment of cervical cancer.
Effectiveness of immune therapy combined with chemotherapy on the immune function and recurrence rate of cervical cancer.
Abstract
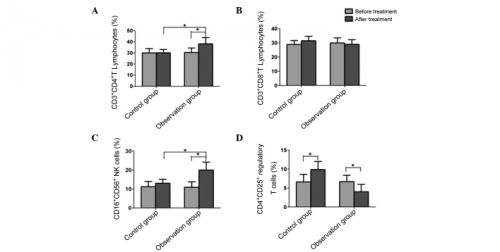
The aim of this study was to compare the immune function of patients with cervical cancer and the cancer recurrence rate in patients treated with biological immune therapy combined with chemotherapy or with chemotherapy only. A total of 79 postoperative patients with cervical cancer participated in the present study. They were randomly divided into a control group and an experimental group. Patients in the control group were treated with cisplatin chemotherapy. Patients in the experimental group were treated with dendritic cell-cytokine-induced killer (DC-CIK) cells combined with cisplatin chemotherapy. The CD3+, CD4+, CD8+, CD16+, CD56+ and CD4+CD25+ cell ratios in peripheral blood, and the expression levels of perforin, granzyme B (GraB) and CD107a of peripheral blood mononuclear cells (PBMCs) in all patients prior to and following treatment were observed. The changes of immune function and recurrence rate between these two groups prior to and following treatment were compared. Prior to treatment, the lymphocyte ratio had no significant difference between the two groups (P>0.05). Following treatment, the lymphocyte ratio in the experimental group was significantly higher than that in the control group (P<0.05). The positive expression levels of perforin, GraB and CD107a of PBMCs in the experimental group following treatment were significantly higher than those prior to treatment and those of the control group (P<0.05). The cumulative recurrence rate in the experimental group was significantly lower than that in the control group (P<0.05).
In conclusion, in postoperative patients with cervical cancer, treatment with DC-CIK cells combined with cisplatin chemotherapy significantly improved the immune function, reduced the recurrence rate and prolonged the survival time of the patients.
- PMID:
- 25667679
- PMCID:
- PMC4316956
-
References
1. Bynum SA, Brandt HM, Sharpe PA, Williams MS, Kerr JC. Working to close the gap: identifying predictors of HPV vaccine uptake among young African American women. J Health Care Poor Underserved. 2011;22:549–561. doi: 10.1353/hpu.2011.0060. [PubMed] [Cross Ref]2. Wang XC, Wu MY. Guangdong Yao Xue Yuan Xue Bao. Vol. 29. Progress; 2013. on DC-CIK-based adoptive cellular immunotherapy for uterine cervical neoplasm; pp. 575–579. (In Chinese)3. Tewari KS, Monk BJ. New strategies in advanced cervical cancer: from angiogenesis blockade to immunotherapy. Clin Cancer Res. 2014;20:5349–5358. doi: 10.1158/1078-0432.CCR-14-1099. [PubMed] [Cross Ref]4. Wang FS, Liu MX, Zhang B, et al. Antitumor activities of human autologous cytokine-induced killer (CIK) cells against hepatocellular carcinoma cells in vitro and in vivo. World J Gastroenterol. 2002;8:464–468. [PubMed]5. Itsumi M, Tatsugami K. Immunotherapy for renal cell carcinoma. Clin Dev Immunol. 2010;2010:284581. doi: 10.1155/2010/284581. [PMC free article] [PubMed] [Cross Ref]6. Kim HM, Lim J, Kang JS, et al. Inhibition of human cervical carcinoma growth by cytokine-induced killer cells in nude mouse xenograft model. Int Immunopharmacol. 2009;9:375–380. doi: 10.1016/j.intimp.2008.12.001. [PubMed] [Cross Ref]7. Hontscha C, Borck Y, Zhou H, Messmer D, Schmidt-Wolf IG. Clinical trials on CIK cells: first report of the international registry on CIK cells (IRCC) J Cancer Res Clin Oncol. 2011;137:305–310. doi: 10.1007/s00432-010-0887-7. [PubMed] [Cross Ref]8. Palucka K, Banchereau J. Cancer immunotherapy via dendritic cells. Nat Rev Cancer. 2012;12:265–277. doi: 10.1038/nrc3258. [PMC free article] [PubMed] [Cross Ref]9. Bhargava A, Bunkar N, Khare NK, Mishra D, Mishra PK. Nanoengineered strategies to optimize dendritic cells for gastrointestinal tumor immunotherapy: from biology to translational medicine. Nanomedicine (Lond) 2014;9:2187–2202. doi: 10.2217/nnm.14.115. [PubMed] [Cross Ref]10. Siegel R, Naishadham D, Jemal A. Cancer statistics, 2012. CA Cancer J Clin. 2012;62:10–29. doi: 10.3322/caac.20138. [PubMed] [Cross Ref]11. Kastritis E, Bamias A, Bozas G, et al. The impact of age in the outcome of patients with advanced or recurrent cervical cancer after platinum-based chemotherapy. Gynecol Oncol. 2007;104:372–376. doi: 10.1016/j.ygyno.2006.08.042. [PubMed] [Cross Ref]12. Motz GT, Coukos G. Deciphering and reversing tumor immune suppression. Immunity. 2013;39:61–73. doi: 10.1016/j.immuni.2013.07.005. [PMC free article] [PubMed] [Cross Ref]13. Lindau D, Gielen P, Kroesen M, Wesseling P, Adema GJ. The immunosuppressive tumour network: myeloid-derived suppressor cells, regulatory T cells and natural killer T cells. Immunology. 2013;138:105–115. doi: 10.1111/imm.12036. [PMC free article] [PubMed] [Cross Ref]14. Hasan UA, Bates E, Takeshita F, et al. TLR9 expression and function is abolished by the cervical cancer-associated human papillomavirus type 16. J Immunol. 2007;178:3186–3197. doi: 10.4049/jimmunol.178.5.3186. [PubMed] [Cross Ref]15. Wang X, Yu W, Li H, Yu J, Zhang X, Ren X, Cao S. Can the dual-functional capability of CIK cells be used to improve antitumor effects? Cell Immunol. 2014;287:18–22. doi: 10.1016/j.cellimm.2013.11.009. [PubMed] [Cross Ref]16. Wang QJ, Wang H, Pan K, et al. Comparative study on anti-tumor immune response of autologous cytokine-induced killer (CIK) cells, dendritic cells-CIK (DC-CIK) and semi-allogeneic DC-CIK. Chin J Cancer. 29:641–648. 201. [PubMed]17. Zheng YW, Li RM, Zhang XW, Ren XB. Current adoptive immunotherapy in non-small cell lung cancer and potential influence of therapy outcome. Cancer Invest. 2013;31:197–205. doi: 10.3109/07357907.2013.775294. [PubMed] [Cross Ref]18. Ren J, Di L, Song G, Yu J, et al. Selections of appropriate regimen of high-dose chemotherapy combined with adoptive cellular therapy with dendritic and cytokine-induced killer cells improved progression-free and overall survival in patients with metastatic breast cancer: reargument of such contentious therapeutic preferences. Clin Transl Oncol. 2013;15:780–788. doi: 10.1007/s12094-013-1001-9. [PubMed] [Cross Ref]19. Yang HZ, Shi N, Li LN, Kang H, Yang LN. Clinical research of interventional treatment combined with CIK in patients with uterine cervix cancer. Haerbin Yi Ke Da Xue Xue Bao. 2010;44:263–266. (In Chinese)20. Zhu YH, Liu JQ, Cao H, et al. Clinical efficiency of radiotherapy combined with self-immune cell therapy for cervical carcinoma. Zhongguo Zhong Liu Sheng Wu Zhi Liao Za Zhi. 2012;19:421–427. (In Chinese)21. Laurin D, Marin V, Biagi E, et al. Exploration of the lysis mechanisms of leukaemic blasts by chimaeric T-cells. J Biomed Biotechnol. 2010;2010:234540. doi: 10.1155/2010/234540. [PMC free article] [PubMed] [Cross Ref]
Articles from Experimental and Therapeutic Medicine are provided here courtesy of Spandidos Publications
Gerelateerde artikelen
- Immuuntherapie met pembrolizumab plus radiotherapie plus 5 immuunstimulerende middelen waaronder curcumine, vitamine-D, endoxan en sedergine geopend voor patienten met baarmoederkanker en baarmoederhalskanker
- Pembrolizumab eerstelijns gegeven plus chemotherapie bij aanhoudende of recidief of uitgezaaide baarmoederhalskanker geeft betere ziektevrije en overall overleving (plus 33 procent) dan placebo
- Immuuntherapie met pembrolizumab geeft hoopvolle resultaten bij patienten met gevorderde baarmoederhalskanker met Pd-L1 positieve mutatie waar chemotherapie faalde
- Immuuntherapie met HPV - T-cellen geeft veelbelovende resultaten bij vergevorderde baarmoederhalskanker met twee duurzame complete remissies uit 9 patienten
- Immuuntherapie met combinatie van balstilimab en zalifrelimab - of alleen balstilimab geeft hoopgevende resultaten als tweedelijnsbehandeling van vergevorderde baarmoederhalskanker
- Lenvatinib plus Pembrolizumab bij patienten met gevorderde baarmoederkanker geeft hoopgevende resultaten met 40 procent remissies van 50 procent of meer.
- Immuuntherapie met anti-PD medicijn Cemiplimab plus het vaccin ISA101b gericht op het HPV16 virus of met nivolumab geeft veelbelovende resultaten voor vormen van kanker die HPV gerelateerd zijn copy 1 copy 1
- Immuuntherapie met dendritische killercells (DC-CIK) geeft veel minder kans op een recidief 22,5 vs 46,2 procent en vergroot significant overall overleving met 25 procent op drie jaars meting
- Immuntherapie bij baarmoederkanker en baarmoederhalskanker: een overzicht



Plaats een reactie ...
Reageer op "Immuuntherapie met dendritische killercells (DC-CIK) geeft veel minder kans op een recidief 22,5 vs 46,2 procent en vergroot significant overall overleving met 25 procent op drie jaars meting"