4 januari 2024: zie ook dit artikel: https://kanker-actueel.nl/atezolizumab-als-eerstelijnstherapie-voor-patienten-met-uitgezaaide-of-lokaal-gevorderde-urineleiderkanker-geeft-betere-overall-overleving-maar-niet-statistisch-significant-in-vergelijking-met-chemotherapie.html
19 april 2017: FDA geeft versnelde goedkeuring aan atezolizumab bij blaaskanker. Zie hieronder beschrijving van de studie waarop de goedkeuring is gebaseerd. Of lees deze PDF van de FDA maar is heel technisch medisch engels:
https://www.accessdata.fda.gov/drugsatfda_docs/nda/2016/761034orig1s000riskr.pdf
25 februari 2016: Bron: Genitourinary Cancers Symposium 2016
Atezolizumab een zogeheten anti-PD medicijn (zoals bv. ook nivolumab is) toont aan dat dit medicijn in de nabije toekomst de standaard behandeling tweede lijns of hopelijk eerste lijns kan worden voor uitgezaaide platina chemo resistente urineleiderkanker en blaaskanker. Uit de tussenevaluatie na twee jaar van een fase II studie bekend onder de naam: IMvigor 210 blijkt dat, ondanks dat de patienten zwaar voorbehandeld waren (minimaal drie chemokuren achter de rug) en in een fase 4 stadium waren voordat de studie startte, er maar liefst 11% nog een duurzame CR - totale remissie bewerkstelligde. CR - complete remissie betekent dat er klinisch geen tumoren meer worden gevonden op een scan. Hoewel de positieve expressie van de zogeheten PD-L1 een positieve prognose gaf, 11% CR, waren er ook bij weinig expressie van de PD-L1 nog 6% CR - complete remissies en bij geen PD-L1 expressie 5% CR - complete remissies. 61% van alle patienten (N- 310) verdeeld over 70 ziekenhuizen wereldwijd reageerden met op zijn minst een respons op de atezolizumab, wat betekent dat er minimaal een teruggang van aantal en omvang van de tumoren was te zien
Zo vertelde hoofd onderzoekster Jean Hoffman-Censits, MD, van The Sidney Kimmel Cancer Center, Thomas Jefferson University, Philadelphia, op het Genitourinary Cancers Symposium 2016.
“Atezolizumab heeft de potentie de standaard behandeling te worden voor uitgezaaide urineleiderkanker Response cijfers zijn veel hoger vergeleken met de 10% in eerdere controlestudies in de tweedelijns behandelingen. Hogere PD-L1 status was gerelateerd aan betere respons maar ook lagere PD-L1 expressie gaf geen contra indicatie op de respons. Mediane duur van de respons is nog niet bereikt in alle groepen van patienten, ook niet bij de zwakke PD-L1 expressie”. stelt dr. Hoffman-Censits. In het abstract kunt u ook klikken voor haar videopresentatie
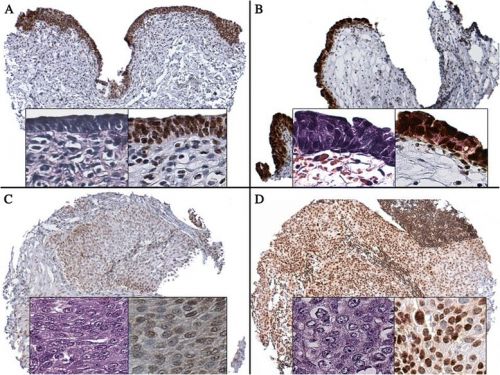
Foto: verschillende stadia van uritheelkanker
Studieopzet:
IMvigor 210 is een open-label, single-arm fase II studie uitgevoerd in 70 ziekenhuizen in Europa en Noord-Amerika. Alle patienten zijn in eerste instantie gescreend op PD-L1 en tumor infiltrating immuuncellen. Patiënten en onderzoekers wisten niet de resultaten daarvan.
Er waren twee studiegroepen van patiënten: In studiegroep 1 werden patiënten opgenomen die al resistent waren voor platina chemo en in studiegroep 2 patienten met ziekteprogressie of recidief na platina chemo. De resultaten van cohort 2 werd nu gepresenteerd, die van cohort 1 volgen later dit jaar.
Van de 486 gescreende patiënten kregen er uiteindelijk 310 een behandeling met atezolizumab met een dosis van 1,200 mg intraveneus elke drie weken tot er aantoonbaar geen effect meer was te zien.
PD-L1 expressie werd vastgesteld via de Ventana SP142 assay, met stratificatie van einddoelen door PD-L1 tumor-infiltrating immune cell (IC) status. Een score van IC 2/3 werd gezien als medium/hoog PD-L1 expressie, waar een score van IC 0/1 werd gezien als lage PD-L1 expressie.
Mediane leeftijd van de patiënten was 66 jaar en 78% waren man. Bjna 3/4 van de patiënten had ook blaaskanker en meer dan 40% hadden drie of meer chemokuren achter de rug.
Resultaten:
Overall response was 26% in IC 2/3 patiënten (dus met medium/hoge PD-L1 espressie) en 18% bij patiënten met enige maar lage expressie van PD-L1; overall response rate was 15% bij alle patiënten in een intent-to-treat analyse. Complete remissies werden gezien bij respectievelijk 11%, 6% en 5%.
Bij IC 2/3 patiënten bereikte 61% een vermindering van de tumorlast, 45% bij de IC 1 patiënten en 30% bij IC 0 patiënten.
Responses waren duurzaam. Mediane duur van de response was in nog geen enkele groep bereikt. Zelfs niet in de subgroup van geen of weinig expressie van de PD-L1. “84% van de patiënten die met een respons reageerden waren nog steeds in respons na 11,7 maanden,” aldus Dr. Hoffman-Censits.
In een subgroep analyse, de zwaarste voorbehandelde patiënten (10% van alle patiënten) hadden vier of meer chemokuren achter de rug. De overall response in deze groep patiënten was 20% bij IC 2/3 patiënten, met een complete remissie van 10%; bij alle patiënten uit deze subgroep was de overall response 8% en de complete remissie 4%.
Bijwerkingen profiel was redelijk tot goed behandelbaar. 5% ervaarde serieuze bijwerkingen graad 3 of erger. Vermoeidheid was de meest gehoorde bijwerking.
| n (%) | IRF ORR, % (95% CI) | CR, % | |
|---|---|---|---|
| PD-L1 status | |||
| IC2/3 | 100 (32) | 27 (19, 37)a | 8 |
| IC1/2/3 | 208 (67) | 18 (13, 24)a | 5 |
| All | 311 (100) | 15 (11, 20)a | 4 |
| Poor prognostic factors | |||
| Visceral mets | 243 (78) | 10 (7, 15) | 1 |
| Liver mets | 97 (31) | 6 (2, 13) | 0 |
| ECOG PS 1 | 193 (62) | 10 (6, 15) | 2 |
| Hb < 10 g/dL | 68 (22) | 9 (3, 18) | 0 |
aP < .01
Conclusie:
■ Atezolizumab had bemoedigende resultaten in responses en duurzame complete remissies bij gevorderde uitgezaaide uritheelkanker dat progressie van de ziekte liet zien tijdens of na platina chemokuren en bij primaire blaaskanker. De duurzame responses werden gezien bij alle vormen van PD-L1 expressie. Atezolizumab kan een verandering geven in de tweede lijnsbehandeling maar daarvoor zijn nog wel fase III studies nodig die kinmiddels al lopen.Disclosure: The study was sponsored by F. Hoffman-La Roche Ltd. Dr. Hoffman-Censits has received honoraria from and consulted for Roche/Genentech and received research funding from Sanofi.
Reference
- Hoffman-Censits JH, Grivas P, Van Der Heijden MS, et al: IMvigor 210, a phase II trial of atezolizumab (MPDL3280A) in platinum-treated locally advanced or metastatic urothelial carcinoma. 2016 Genitourinary Cancers Symposium. Abstract 355. Presented January 8, 2016.
Hier het abstract zoals gepresenteerd op het Genitourinary Cancers Symposium 2016
The first Phase 2 study targeting PD-L1/PD-1 in metastised Uritheal Carcinoma / bladder cancer , demonstrated significantly improved ORR vs historic controls. Responses were durable and associated with higher PD-L1 IC expression; poor prognostic factors did not preclude response.
IMvigor 210, a phase II trial of atezolizumab (MPDL3280A) in platinum-treated locally advanced or metastatic urothelial carcinoma (mUC).
Poster Session B: Prostate Cancer; Urothelial Carcinoma; Penile, Urethral, and Testicular Cancers
355
Background: The ORR and survival of mUC patients (pts) who progress after platinum-based chemotherapy (pctx) are poor. Atezolizumab (atezo) reinvigorates antitumor immunity by targeting PD-L1 and has shown promising Ph 1 activity in mUC.
Methods: IMvigor 210 cohort 2 (NCT02108652) enrolled 316 mUC pts who progressed during or following pctx. Pts received atezo at 1200 mg IV q3w until loss of clinical benefit. The SP142 IHC assay centrally assessed PD-L1 expression. Pts/investigators were blinded to PD-L1 status. Co-primary endpoints were confirmed ORR by RECIST v1.1 per central review (IRF) and modified (m) RECIST per investigator, which were met if null hypothesis (ORR = 10%) was rejected (α = 5%). ORR endpoints were stratified by PD-L1 tumor-infiltrating immune cell (IC) status: IC2/3, IC1/2/3, all comers.
Results: Efficacy/safety-evaluable pts (N = 311) had a median age of 66 y, CrCl < 60 mL/min (35%) and ≥ 2 prior regimens for mUC (40%). Many had poor prognostic factors (Table). At 5/5/15 data cutoff (follow up ≥ 24 w), 43/47 responding pts had ongoing responses. Both IRF (Table) and mRECIST ORR correlated with IC status. Durable responses were seen including poor prognostic subgroups (Table). mDOR was not reached in any PD-L1 or prognostic subgroup. mPFS was 2.1 mo in all PD-L1 subgroups. Median treatment duration was 12 w (range 0-46). Treatment-related AEs (most commonly fatigue) occurred in 66% of pts (all Grade); 15% had G3-4 related AE and 4% had G3-4 immune-mediated AE. 27% of AEs led to dose interruption and 3% led to withdrawal. No renal toxicity was seen.
Conclusions: IMvigor 210, the first Ph 2 study targeting PD-L1/PD-1 in mUC, demonstrated significantly improved ORR vs historic controls. Responses were durable and associated with higher PD-L1 IC expression; poor prognostic factors did not preclude response. Atezo was well tolerated, and a randomized Ph 3 study vs ctx is ongoing (IMvigor 211; NCT02302807). Clinical trial information: NCT02108652
| n (%) | IRF ORR, % (95% CI) | CR, % | |
|---|---|---|---|
| PD-L1 status | |||
| IC2/3 | 100 (32) | 27 (19, 37)a | 8 |
| IC1/2/3 | 208 (67) | 18 (13, 24)a | 5 |
| All | 311 (100) | 15 (11, 20)a | 4 |
| Poor prognostic factors | |||
| Visceral mets | 243 (78) | 10 (7, 15) | 1 |
| Liver mets | 97 (31) | 6 (2, 13) | 0 |
| ECOG PS 1 | 193 (62) | 10 (6, 15) | 2 |
| Hb < 10 g/dL | 68 (22) | 9 (3, 18) | 0 |
aP < .01
Gerelateerde artikelen
- ctDNA hulpmiddel Signatera CDx goedgekeurd door FDA om patiënten met spierinvasieve blaaskanker met restziekte na operatie te selecteren voor immuuntherapie met atezolizumab
- Anktiva = interleukine-15 samen met bacillus Calmette-Guérin (BCG) geeft op 3 jaar uitstekende ziekteprogressievrije overleving bij patiënten met BCG ongevoelige, hooggradige, papillaire, niet-spierinvasieve blaaskanker
- Atezolizumab als eerstelijnstherapie voor patiënten met uitgezaaide of lokaal gevorderde urineleiderkanker geeft betere overall overleving maar niet statistisch significant in vergelijking met chemotherapie
- Atezolizumab, een anti-PD medicijn geeft uitstekende resultaten bij uitgezaaide en zwaar voorbehandelde patienten met urineleiderkanker en blaaskanker
- nivolumab plus gemcitabine en cisplatine verbetert overall overleving van patienten met blaaskanker blijkt uit de checkmate 901 studie
- Immuuntherapie met Tislelizumab gecombineerd met Nab-Paclitaxel voor niet-spierinvasief urnieleider - blaaskanker met hoog risico geeft bijzonder goede resultaten
- C-reactief proteïne bloedwaarden (CRP) heeft betere voorspellende waarde voor aanslaan van immuuntherapie dan PD-L1 expressie bij patiënten met uitgezaaide urineleiderkanker - blaaskanker
- Immuuntherapie met maandelijkse vaste dosis durvalumab geeft duurzame remissies bij eerder met chemotherapie behandelde patiënten met gevorderde blaaskanker - urineleiderkanker
- Immuuntherapie met nivolumab geeft uitstekende resultaten bij gevorderde uitgezaaide blaaskanker - urineleiderkanker
- Circulerend tumor-DNA voorspelt respons op immuuntherapie met anti-PD medicijn Atezolizumab bij spierinvasieve urineleiderkanker en blaaskanker
- Hoe eerder na chemo gestart met Avelumab, een immuuntherapeutisch medicijn als onderhoudsbehandeling,hoe beter de resultaten op ziektevrije tijd en overall overleving bij patienten met inoperabele blaaskanker en urineleiderkanker
- Immuuntherapie met gemoduleerd verkoudheidsvirus (Coxsackievirus A21) vooraf aan operatie van blaaskanker is succesvol
- Pembrolizumab - Keytruda - anti PD medicijn - geeft uitstekende resultaten bij gevorderde blaaskanker blijkt uit follow-up gegevens van eerder wegens succes stopgezette studie.
- Avelumab, een anti-PD medicijn door FDA goedgekeurd voor gebruik na falende chemo bij gevorderde urineleiderkanker - blaaskanker stadium 4
- Immuuntherapie met nivolumab en ipilimumab samen geeft hoopgevende resultaten bij zwaar voorbehandelde gevorderde uitgezaaide blaaskanker
- BCG - Bacillus Calmette-Guerin bij blaaskanker: Hier een mini overzicht gepubliceerd van wetenschappelijke studies en bewijzen over het gebruik van BCG - Bacillus Calmette-Gue´rin - als succesvolle immuuntherapie bij blaaskanker. Update 23 februari 2010
- Immuuntherapie bij blaaskanker: een overzicht inclusief immuuntherapie met anti-PD medicijnen - checkpointremmers



Plaats een reactie ...
Reageer op "Atezolizumab, een anti-PD medicijn geeft uitstekende resultaten bij uitgezaaide en zwaar voorbehandelde patienten met urineleiderkanker en blaaskanker"