Mocht u de artikelen op kanker-actueel.nl waarderen dan wilt u misschien donateur worden? En als donateur kunt u naast toegang tot bepaalde artikelen alleen voor donateurs ook korting krijgen bij verschillende bedrijven.
28 januari 2026: zie ook dit artikel: https://kanker-actueel.nl/NL/daratumumab-en-hyaluronidase-fihj-samen-met-bortezomib-lenalidomide-en-dexamethason-geeft-uitstekende-resultaten-bij-patienten-met-nieuwe-diagnose-van-multiple-myeloma-die-niet-in-aanmerking-komen-voor-stamceltransplantatie.html
13 januari 2025: zie ook dit artikel: https://kanker-actueel.nl/daratumumab-alleen-gegeven-geeft-uitstekende-resultaten-bij-patienten-met-actieve-sluimerende-multiple-myeloma-in-vergelijking-met-actief-monitoren.html
3 oktober 2018: lees ook dit artikel:
5 september 2016: Deze studie: Adding Daratumumab to Bortezomib/Dexamethasone Improves Progression-Free Survival in Relapsed/Refractory Multiple Myeloma is inmiddels ook gepubliceerd in Clinical Oncology:. zie verder hieronder meer gegevens over deze studie.
De European Medicines Agency (EMA)heeft al in 2015 daratumumab (DARZALEX) goedgekeurd als behandeling voor vooraf zwaar behandelde patienten met ziekte van Kahler - Multiple Myeloma. Hier het persbericht van vorig jaar van de producent.Janssen’s daratumumab accepted for treatment of European patients with heavily pre-treated multiple myeloma
22 juni 2016: Bron: ASCO 2016 - J Clin Oncol 34, 2016 (suppl; abstr LBA4)
Wanneer patienten met botkanker - multiple myeloma (Kahler) na minimaal 1 keer behandeld te zijn met bortezomib - velcade en dexamethasone en daarna bij een recidief worden behandeld met daratumumab toegevoegd aan bortezomib - velcade en dexamethason dan blijken de resultaten zo goed te zijn (mediaan 61 procent minder kans op recidief op 1 jaars meting) dat de fase III studie (CASTOR) al na 7,5 maand is gestopt om de patienten uit de controlegroep ook daratumab te kunnen geven. Al na drie maanden ontstonden grote verschillen in response.
Opvallende constatering is dat de patiënten die slechts 1 chemokuur vooraf hadden gehad nog beter reageerden dan patienten die 2 of meer chemokuren hadden gehad.
Deze gaf 69% minder risico op een recidief en 1-jaarsprogressie-vrije overleving van 77.5% vs 29.4% zonder daratumumab.
Hieronder een grafiek van de resultaten van de gerandomiseerde fase III studie (CASTOR) (N = 498) zoals gepresenteerd op ASCO 2016
De mediane overall overleving is nog lang niet bereikt maar op basis van de tussenresultaten zal deze ongetwijfeld statistische significantie bereiken. De onderzoekers stellen dan ook dat daratumumab als aanvulling op bortezomib - Velcade en dexamethason standaard behandeling moet worden bij eerste recidief van multiple myeloma - ziekte van Kahler.
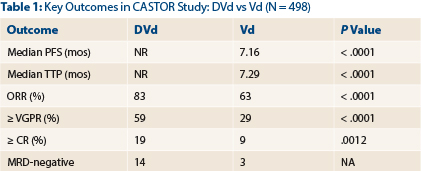
CR = complete response; DVd = daratumumab, bortezomib, dexamethasone; MRD = minimal residual disease; NR = not reached; ORR = overall response rate; PFS = progression-free survival; TTP = time to tumor progression; Vd = bortezomib, dexamethasone; VGFR = very good partial response.
Kernpunten uit de studie:
New Standard of Care in Multiple Myeloma?
- For relapsed/refractory multiple myeloma, daratumumab plus bortezomib/dexamethasone, vs bortezomib/dexamethasone, significantly improved multiple outcomes in patients with one or more previous lines of therapy.
- Risk of progression was reduced by 61% (P < .0001) with the daratumumab used earlier than its FDA indication (ie, after three or more prior treatments).
De studie Phase III randomized controlled study of daratumumab, bortezomib, and dexamethasone (DVd) versus bortezomib and dexamethasone (Vd) in patients (pts) with relapsed or refractory multiple myeloma (RRMM): CASTOR study. is gepresenteerd op ASCO 2016
De European Medicines Agency (EMA)heeft al in 2015 daratumumab goedgekeurd als behandeling voor vooraf zwaar behandelde patienten met ziekte van Kahler - Multiple Myeloma. Hier het persbericht van vorig jaar van de producent.Janssen’s daratumumab accepted for treatment of European patients with heavily pre-treated multiple myeloma
Hieronder het abstract van de nieuwste studie:
daratumumab 16 mg/kg monotherapy demonstrated rapid, deep, and durable responses, with a clinical benefit that extended to patients with stable disease or better.
Source: ASCO 2016
2016 ASCO Annual Meeting
Hematologic Malignancies—Plasma Cell Dyscrasia
LBA4
Background: Daratumumab (D), a human anti-CD38 IgGκ mAb, induces deep and durable responses with a favorable safety profile in RRMM pts. We report a pre-specified interim analysis of the first randomized controlled study of D (CASTOR; NCT02136134).
Methods: Pts with ≥1 prior line of therapy were randomized (1:1) to 8 cycles (q3w) of bortezomib (V)/dexamethasone (d) (V: 1.3 mg/m2sc on Days 1, 4, 8, 11; d: 20 mg po on Days 1, 2, 4, 5, 8, 9, 11, 12) ± D (16 mg/kg iv qw in Cycles 1-3, Day 1 of Cycles 4-8, then q4w until progression). Primary endpoint was PFS.
Results: 498 pts (DVd, 251; Vd, 247) were randomized. Baseline demographics and disease characteristics were well balanced. Pts received a median of 2 prior lines of therapy (range 1-10). 66% received prior V; 76% received prior IMiD; 48% received prior PI and IMiD; 33% were IMiD-refractory; 32% were refractory to last line of prior therapy. With median follow-up of 7.4 months, D significantly improved median PFS (61% reduction in risk of progression) and TTP for DVd vs Vd (Table). D significantly increased ORR (83% vs 63%, P<0.0001), and doubled rates of ≥VGPR (59% vs 29%, P<0.0001), and ≥CR (19% vs 9%, P= 0.0012) for DVd vs Vd, respectively; median duration of response was NR vs 7.9 months, respectively. Most common (>25%) AEs (DVd/Vd) were thrombocytopenia (59%/44%), peripheral sensory neuropathy (47%/ 38%), diarrhea (32%/22%) and anemia (26%/31%). Most common grade 3/4 AEs (>10%) were thrombocytopenia (45%/33%), anemia (14%/16%), neutropenia (13%/4%). 7%/9% of pts discontinued due to a TEAE. D-associated infusion-related reactions (45% of pts) mostly occurred during the first infusion; most were grade 1/2 (grade 3/4, 9%/0%).
Conclusions: Daratumab significantly improved PFS, TTP, and ORR in combination with Velcade vs Velcade alone. DVd doubled both VGPR and sCR/CR rates vs Vd alone. Safety of DVd is consistent with the known safety profile of D and Vd. The addition of D to Vd should be considered a new standard of care for RRMM pts currently receiving Vd alone. Clinical trial information: NCT02136134
| DVd | Vd | |
|---|---|---|
| PFS | ||
| Median, mo | NE | 7.16 |
| HR (95% CI) | 0.39 (0.28, 0.53) | |
| P | <0.0001 | |
| TTP | ||
| Median, mo | NE | 7.29 |
| HR (95% CI) | 0.30 (0.21, 0.43) | |
| P | <0.0001 | |
Gerelateerde artikelen
- Daratumumab en hyaluronidase-fihj samen met bortezomib, lenalidomide en dexamethason geeft uitstekende resultaten bij patiënten met nieuwe diagnose van multiple myeloma die niet in aanmerking komen voor stamceltransplantatie.
- Daratumumab toegevoegd aan een (VCd)-kuur (bortezomib, cyclofosfamide en dexamethason) geeft betere effectiviteit en meer patiënten bereikten een duurzame gedeeltelijke remissie in vergelijking met alleen VCd-kuur bij patienten met light chain amyloidosis
- Daratumumab (Darzalex) in combinatie met bortezomib (Velcade) en dexamethason voor eerder behandelde Multiple myeloma - Kahler vermindert kans op recidief op 1 jaar met 61 procent
- Daratumumab alleen gegeven geeft uitstekende resultaten bij patienten met actieve sluimerende Multiple Myeloma in vergelijking met actief monitoren




Plaats een reactie ...
Reageer op "Daratumumab (Darzalex) in combinatie met bortezomib (Velcade) en dexamethason voor eerder behandelde Multiple myeloma - Kahler vermindert kans op recidief op 1 jaar met 61 procent"