Mocht u de informatie op onze website kanker-actueel.nl waarderen dan wilt u ons misschien ondersteunen met een donatie?
Ons rekeningnummer is: RABO 37.29.31.138 t.n.v. Stichting Gezondheid Actueel in Terneuzen.
Onze IBANcode is NL79 RABO 0372 9311 38
Als donateur kunt u ook korting krijgen bij verschillende bedrijven. En we hebben een ANBI status
3 oktober 2019: Bron ESMO 2019
Galwegenkanker, zeker als het is uitgezaaid en inoperabel, is heel moeilijk te behandelen. De prognose voor deze groep van patienten is heel slecht. Nu lijkt een medicijn ivosidenib, een medicijn dat specifiek is gericht op de isocitrate dehydrogenase 1 (IDH1) mutatie toch hoop te geven. Onderzoekers hebben een gerandomiseerd placebo gecontroleerd onderzoek gedaan bij totaal 185 patienten met uitgezaaide vergevorderde inoperabele galwegenkanker die allemaal die specifieke IDH1 mutatie hadden.
Van de groep patienten die ivosidenib hadden gehad blijkt 53 procent (66 patienten) een stabiele ziekte te hebben bereikt, met zelfs ook 3 gedeeltelijke remissies (50 procent of meer tumorvermindering). Tegenover 0 remissies in de placebogroep en slechts 27,9 procent bereikte een stabiele ziekte. Echter in de placebogroep bereikte geen van de patienten op 6 maanden stabiele ziekte tegenover 32 procent uit de ivosidenibgroep. Daarbij aangetekend dat patienten uit de placebogroep ook nog konden overstappen. Dus resultaten zijn daar ook nog door beinvloed.
Hier een grafiek van de resultaten:
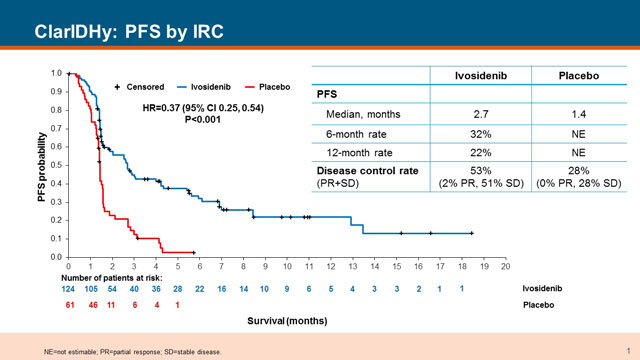
De resutlaten zoals gepresenteerd op ESMO 2019 in dit persbericht / presentatie: Ivosidenib Provides Prolonged Progression-Free Survival in Patients with Cholangiocarcinoma and IDH1 Mutation
ClarIDHy enrolled 185 patients with advanced cholangiocarcinoma and IDH1 mutation who were randomly assigned 2:1 to ivosidenib at 500 mg once daily or matched placebo and stratified by the number of prior systemic therapies (1 versus 2). The patients had a median age of 62 years, 117 were female, and 91% had intrahepatic disease. All patients had advanced unresectable cholangiocarcinoma and IDH1 mutation based on central testing, ECOG performance status 0–1, and measurable disease per RECIST v1.1. Overall, 92% of patients had metastatic disease, and 43% had received 2 prior therapies.
The primary endpoint was PFS by central review and secondary endpoints included safety, objective response rate (ORR), PFS by local investigator review, and overall survival (OS) in the intent-to-treat population (ITT). Crossover from placebo to ivosidenib was permitted upon radiographic disease progression (PD) and the crossover-adjusted OS was derived using rank preserved structural failure time (RPSFT).
The study primary endpoint of PFS by central review was met
Ivosidenib improved PFS over placebo; median PFS was 2.7 months in the 124 patients treated with ivosidenib compared to 1.4 months in the 61 patients receiving placebo (hazard ratio 0.37; 95% confidence interval , 0.25, 0.54; p < 0.001). The 6- and 12-month PFS rates were 32.0% and 21.9% with ivosidenib; however, no patients on placebo were progression-free for 6 months or more at data cut-off.
The ORR for ivosidenib was 2.4%, which consisted of 3 partial responses, and 63 patients (50.8%) achieved stable disease (SD). With placebo, the ORR was 0% and 27.9% (17 patients) achieved SD.
According to the ITT analysis, median OS was 10.8 months with ivosidenib compared to 9.7 months with placebo (HR 0.69; one-sided p = 0.06) with 57% crossover from placebo. Therefore, the RPSFT-adjusted median OS was 6 months with placebo (HR 0.46; p = 0.0008). PFS by local review (HR 0.47; p < 0.001).
Treatment-related adverse events (AEs) occurring in more than 15% of patients on ivosidenib included nausea (32.1%), diarrhoea (28.8%), fatigue (23.7%), cough (19.2%), abdominal pain (18.6%), ascites (18.6%), decreased appetite (17.3%), anaemia (16.0%), and vomiting (16.0%). Grade ≥3 AEs were reported in 46% of ivosidenib patients compared to 36% of patients on placebo. No treatment-related deaths occurred.
Conclusions
According to the authors, ivosidenib provided significant improvement in PFS and a trend towards favourable OS compared to placebo in patients with advanced cholangiocarcinoma and an IDH1 mutation. This is the first, pivotal study demonstrating the clinical benefit of targeting IDH1 mutation in this patient population.
Gerelateerde artikelen
- ASCO 2024: abstracten van ASCO 2024 gerelateerd aan alvleesklierkanker en galwegenkanker
- Chemo (oxaliplatin plus gemcitabine) na operatie bij galwegkanker geeft 25 maanden extra overall overleving (50 vs 75 maanden ) maar wordt afgedaan als zou chemo zinloos zijn copy 1
- Durvalumab gegeven naast gemcitabine plus cisplatine geeft betere overall overleving voor nieuw gediagnosticeerde gevorderde galwegkanker
- Galwegstents via de buikwand en HAIP - intra-arteriële chemotherapie voorkomen minder complicaties en verlengen overall overleving bij patienten met gevorderde en inoperabele galwegenkanker
- Immuuntherapie met pertuzumab plus trastuzumab (herceptin) geeft hoopvolle resultaten bij patiënten met gevorderde uitgezaaide galwegkanker met HER2-mutatie en overexpressie
- ivosidenib, een medicijn gericht op de IDH1 mutatie geeft hoopvolle resultaten bij zwaar voorbehandelde patienten met uitgezaaide galwegenkanker
- Panitumumab in combinatie met cisplatin en gemcitabine geeft beduidend minder overall overleving (13 vs 20 maanden) bij galwegkanker met KRAS wild-type
- PDT - Photo Dynamische Therapie als palliatieve behandeling van inoperabele galwegenkanker verlengt hoog significant mediane overleving bij inoperabele uitgezaaide galwegkanker blijkt uit gerandomiseerde studies. Artikel update 6 februari 2010
- Pemigatinib, een FGFR remmer, voor patiënten met eerder behandelde galwegenkanker geeft bij patienten met een FGFR2-mutatie uitstekende resultaten met een objectieve respons van 35 procent.versus 0 procent bij wie geen FGFR2 mutatie had
- Personalised medicine op basis van DNA en RNA mutaties voor bv. immuuntherapie met anti-PD en gerichte behandelingen lijkt voor galwegenkanker zeker zinvol aldus overzichtsstudie
- Specifieke bloedwaarden en biomarkers die wijzen op veroudering van immuunsysteem (immunosenescentie-biomarkers) plus basale EGF-concentratie in bloed resulteerden in goede voorspellers van het succes van het CIMAvax-EGF vaccin bij gevorderde longkanker c
- TACE - Trans Arteriele Chemo Embolisatie met gemcitabine plus cisplatin geeft bij uitgezaaide galwegkanker significant langere levensduur dan TACE met alleen gemcitabine. d.d. 6 februari 2010
- TAS-120 geeft uitstekende resultaten bij verschillende studies met solide tumoren waaronder galwegkanker
- TAS-120 - futibatinib geeft veelbelovende resultaten bij patienten met in lever uitgezaaide galwegenkanker met fibroblast growth factor receptor 2 (FGFR2) en T53 mutaties copy 1



Plaats een reactie ...
Reageer op "ivosidenib, een medicijn gericht op de IDH1 mutatie geeft hoopvolle resultaten bij zwaar voorbehandelde patienten met uitgezaaide galwegenkanker"