Aan dit artikel is vele uren gewerkt. Opzoeken, vertalen, op de website plaatsen enz. Als u ons wilt ondersteunen dan kan dat via een al of niet anonieme donatie. Elk bedrag is welkom hoe klein ook. Klik hier als u ons wilt helpen kanker-actueel online te houden Wij zijn een ANBI organisatie en dus is uw donatie in principe aftrekbaar voor de belasting
14 oktober 2014: Bron: NEJM 2014 Doi: 10.1056/NEJMoa1408868
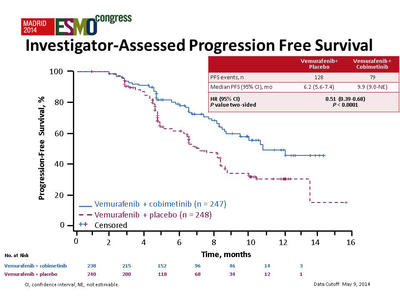
Cobimetinib in combinatie met vemurafenib verbetert significant progressievrije ziekte (PFS) met 49% en kans op overlijden met 35% (na 9 maanden) bij patiënten met melanomen met de mutatie BRAFV600 in vergelijking met alleen vemarufanib. Dit blijkt uit de gerandomiseerde fase III studie, de coBRIM studie, bij totaal 495 patiënten in een periode van slechts 1 jaar, van januari 2013 tot januari 2014.
Een erg goed resultaat. Zo ook zijn er bij andere vormen van kanker waarbij sprake is van BRAF en MEK mutaties, bv. bij vormen van spijsverteringskanker waaronder darmkanker waar een combinatie van BRAF en MEK remmers ook erg goede resultaten geven. Daarmee worden dan weer andere combinaties van BRAF en MEK remmers getest.
Punt van kritiek: in slechts enkele jaren en enkele laboratoriumstudies, dierstudies en een enkele patiënten studie verder komen dit soort nieuwe medicijjnen al na enkele jaren van onderzoek op de markt. Maar wel tegen een extreem hoge prijs als je dat afzet tegen de relatief geringe kosten die deze vorm van onderzoek vergt. Zou minister Schippers hier ook van op de hoogte zijn? Ongetwijfeld maar zoals ook de ziekenhuizen en de meeste betrokken oncologen doen ze er niets aan en feiteljk gezien ten koste van de kankerpatiënt
Studieresultaten:
Prof. McArthur, studieleider van de studie uitgevoerd aan het Peter MacCallum Cancer Centre, Melbourne, Australia presenteerde de resultaten op ESMO 2014.
Deze gerandomiseerde placebo gecontroleerde fase III studie (coBRIM studie) evalueerde de combinatie van de BRAF remmer vemurafenib en de MEK remmer cobimetinib. Cobimetinib is een oraal in te nemen, zogeheten kleine molecule, hoog selectieve, allosterische MEK-remmer.
Tussen januari 2013 en januari 2014, werden 495 patiënten met melanomen met de bewezen mutatie BRAFv600 gerandomiseerd ingedeeld (1 op 1) om of de combinatiebehandeling van vemurafenib + cobimetinib (N=247) te krijgen of alleen vemurafenib + placebo (N=248). In een cyclus van 28 dagen werd een behandeling gegeven van vemurafenib 960 mg twee keer per dag vanaf dag 1 tot dag 28 en cobimetinib of de placebo 60 mg dageljks vanaf dag 1 tot dag 21.
D patiënten hadden allemaal inoperabele lokaal gevorderde of uitgezaaide melanomen met een positieve BRAFV600 mutatie vastgesteld door de cobas® 4800 test. Een goed elichameljke gesateldheid en organenfunctie en waren nog neit eerder behandeld voor gevorderde ziekte. Doelen van de studie waren: progressievrije tijd, tijd van stabiele ziekte, overall overleving en bijwerkingenprofiel De patiënten werden verder geevalueerd naar plaats en stadium van de ziekte (M1c versus andere stadium).
Mediane progressievrije tijd (PFS) was 9.9 maanden voor de combinatiebehandeling versus 6.2 maanden voor de controlegroep met alleen vemurafenib (HR 0.51; p < 0.0001). Progressievrije tijd gebaseerd op sleutelgegevens als plaats en stadium van de ziekte bleek nog betere resultaten te geven: 11.3 maanden versus 6.0 mmaanden respectievelijk. (HR 0.60, p = 0.0003).
Complete regressie en gedeeltelijke regressie was 68% in de combinatiegroep en 45% in de vemurafenib groep (p < 0.0001), inclusief complete regressie bij 10% van de patienten behandeld met de combintairtebehandeling en 4% bij patiënten in de vemurafenib groep.
Overall overleving (OS) was op de 9 maanden meting 81.1% in de combinatie groep versus 72.5% in de vemurafenib groep (HR 0.65, p= 0.046).
De Vemurafenib/cobimetinib combinatie gaf vergeleken met alleen vemurafenib, meerdere bijekringen van graad 3 of hoger (65% vs 59%). Echter er was geen verschil in bijwerkingenprofiel bij de patiënten die met de behandeling door konden gaan en er hoefden ook geen patiënten te stoppen met de behandeling.
Conclusie:
Prof. McArthur concludeert namens de onderzoekers dat de coBRIM studie duidelijk en definitief bewijst dat de combinatie van BRAF en MEK remmers resulteert in significant betere klinische resultaten. 49% langere progresseivrije tijd en 35% minder kans op overlijden. De studie loopt nog door om volwaardige statistische significante overall overlevingscijfers te kunnen geven.
De studie is geljktijdig met de presentatie op eSMO 2014 gepubliceerd in de NEJM: Combined Vemurafenib and Cobimetinib in BRAF-Mutated Melanoma.
Het volledige studierapport is gratis in te zien. Hier het abstract van de studie:
The addition of cobimetinib to vemurafenib was associated with a significant improvement in progression-free survival among patients with BRAF V600–mutated metastatic melanoma, at the cost of some increase in toxicity
Combined Vemurafenib and Cobimetinib in BRAF-Mutated Melanoma
September 29, 2014DOI: 10.1056/NEJMoa1408868
Background
The combined inhibition of BRAF and MEK is hypothesized to improve clinical outcomes in patients with melanoma by preventing or delaying the onset of resistance observed with BRAF inhibitors alone. This randomized phase 3 study evaluated the combination of the BRAF inhibitor vemurafenib and the MEK inhibitor cobimetinib.
Methods
We randomly assigned 495 patients with previously untreated unresectable locally advanced or metastatic BRAF V600 mutation–positive melanoma to receive vemurafenib and cobimetinib (combination group) or vemurafenib and placebo (control group). The primary end point was investigator-assessed progression-free survival.
Results
The median progression-free survival was 9.9 months in the combination group and 6.2 months in the control group (hazard ratio for death or disease progression, 0.51; 95% confidence interval , 0.39 to 0.68; P<0.001). The rate of complete or partial response in the combination group was 68%, as compared with 45% in the control group (P<0.001), including rates of complete response of 10% in the combination group and 4% in the control group. Progression-free survival as assessed by independent review was similar to investigator-assessed progression-free survival. Interim analyses of overall survival showed 9-month survival rates of 81% (95% CI, 75 to 87) in the combination group and 73% (95% CI, 65 to 80) in the control group. Vemurafenib and cobimetinib was associated with a nonsignificantly higher incidence of adverse events of grade 3 or higher, as compared with vemurafenib and placebo (65% vs. 59%), and there was no significant difference in the rate of study-drug discontinuation. The number of secondary cutaneous cancers decreased with the combination therapy.
Conclusions
The addition of cobimetinib to vemurafenib was associated with a significant improvement in progression-free survival among patients with BRAF V600–mutated metastatic melanoma, at the cost of some increase in toxicity. (Funded by F. Hoffmann–La Roche/Genentech; coBRIM ClinicalTrials.gov number, NCT01689519.)
Gerelateerde artikelen
- Vemurafenib is een heel gericht medicijn en blijkt ook in fase III studie voor goede resultaten te zorgen bij vergevorderde melanoompatienten met BRAF mutatie. FDA geeft per direct vemurafenib - zelboraf goedkeuring als officieel medicijn
- Personalised medicine en targeted therapy bij melanomen: een overzicht





Plaats een reactie ...
Reageer op "vemurafenib plus cobimetinib, een MEK en BRAf remmer, geeft samen 49 procent langere progressievrije tijd en 35 procent minder kans op overlijden bij melanomen."