3 december 2018: Lees ook dit artikel:
10 september 2015: Bron: N Engl J Med. 2015 Feb 12;372(7):621-30. doi: 10.1056/NEJMoa1406470.
Lenvatinib, een zogeheten multi tyrosine kinase remmer geeft bij patiënten met uitbehandelde uitgezaaide schildklierkanker een zeer goed resultaat op progressievrije ziekte en mediane overall overleving in vergelijking met placebo en beste zorg. De mediane overleving was na 2 jaar studie follow-up 18,3 maanden versus 3,6 maanden voor de placebogroep. En ziektevrije tijd was 44,3 % voor de patiënten uit de lenvatinib groep. De ziektevrije tijd voor de placebogroep kon niet worden gemeten omdat veel patiënten tijdens de studie overstapten naar lenvatinib.
Alle deelnemende patiënten waren resistent geworden voor een behandeling met radio-iodine-131, (een behandeling met radio-actieve jodium), dus in feite onbehandelbaar en ongeneeslijk. 4 patiënten uit de lenvatinib groep bewerkstelligden binnen 2 jaar een duurzame complete remissie dat betekent dus dat er geen kanker meer werd gezien op scans enz. na 2 jaar
Lenvatinib is een remmer van de zogeheten VEGR - vascular endothelial growth factor receptor (VEGFR) 1, 2, en 3, de fibroblast growth factor receptors 1 tot 4, en de platelet-derived growth factor receptoren α, RET, en KIT. Ook patiënten die al eerder een kinase remmer hadden gekregen reageerden nog goed op lenvatinib.
De bijwerkingen waren wel wat groter dan bij een placebo maar waren meestal wel goed behandelbaar en onder controle te houden. Echter in de lenvatinibgroep overleden 6 patienten (2,3%) gedurende de behandeling die toegeschreven worden aan de behandeling. Maar u moet zich hierbij wel bedenken dat alle patiënten in het eindstadium van hun ziekte verkeerden en in feite ongeneeslijk waren.
Deze fase III studie is gepubliceerd in The New England Journal of Medicine, en uitgevoerd door Martin Schlumberger, MD, en collega's van het Institut Gustave Roussy.
De conclusie van de onderzoekers was dan ook: de multikinase inhibitor lenvatinib (Lenvima) produceert een grote verbetering in progressievrije ziekte in vergelijking met een placebo bij patiënten met gevorderde en resistent voor radioactieve jodium (radioiodine) uitgezaaide schildklierkanker.
Deze studie dient als basis voor de goedkeuring van de FDA - Food and Drug Administration om lenvatinib voor deze vorm van kanker te gebruiken als officiële behandeling.
Foto: werkingsmechanisme van een tyrosine kinase remmer op de receptoren van de tumor
Studieopzet en resultaten
In deze dubbelblinde fase III studie werden totaal 392 patiënten opgenomen met gevorderde uitgezaaide en voor radioactieve jodium resistente schildklierkanker uitgevoerd in meerdere ziekenhuizen in Europa, Australië, Azië en Amerika in de periode tussen augustus 2011 en oktober 2012.
Patiënten werden gerandomiseerd ingedeeld op 2 : 1 basis om in een cylcus van 28 dagen 24 mg/d lenvatinib te krijgen (N = 261) of een placebo (n = 131). Patiënten in de placebo groep konden overstappen naar een open label behandeling met lenvatinib bij progressie van de ziekte. Het primaire doel was progressievrije overleving.
Deelnemers aan de lenvatinib en placebo groepen waren in het algemeen redelijk goed verdeeld naar leeftijd (mediaan, 64 en 61 jaar), regio (Europe voor 50% en 49%, North America voor 30% in beide groepen, andere regio voor 20% en 21%), Eastern Cooperative Oncology Group performance status van 0 of 1 (95% en 98%), 1 eerdere tyrosine kinase inhibitor behandeling (25% en 21%), histologisch subtype (papillary in 51% en 52%, slecht gedifferentieerd in 11% en 14%, follicular–non-Hürthle cell in 20% en 17%, Hürthle cell in 18% en 17%), en aanwezigheid van botuitzaaiingen (40% en 37%) en longuitzaaiingen (87% en 95%). In de placebogroep was een groter aantal patiënten man (57% versus 48%).
Progressievrije overleving:
- Op het moment van stoppen met de studie (November 2013), de mediane duur van de follow-up was 17.1 maanden in de lenvatinib groep en 17.4 maanden in de placebo groep; 130 patients ontvingen nog steeds een behandeling volgens het geblindeerde protocol: 122 patiënten in de lenvatinibgroep (47%) en 8 in de placebogroep (6%). Onder de 114 beschikbare patiënten uit de placebogroep ontvingen er 109 patiënten (96%) alsnog lenvatinib. 41 patiënten (16%)uit de lenvatinib groep kregen na progressie van hun ziekte alsnog andere behandelingen.
- Mediane progressie-vrije overleving was 18.3 maanden in de lenvatinib groep versus 3.6 maanden in de placebo groep (hazard ratio = 0.21, P < .001), waarbij voordeel werd gezien voor alle subgroepen van lenvatinib.
- Progressie-vrije overleving was 63.0% voor de lenvatinibgroep versus 10.5% voor placebogroep na 12 maanden en 44.3% versus nog niet bereikt op 24 maanden voor de lenvatinibgroep
Response cijfers en overall overleving.
- 64.8% in de lenvatinib groep reageerde goed op de behandeling (inclusief 4 complete remissies) versus 1.5% die goed reageerde in de placebo groep (odds ratio = 28.87, P < .001).
- Stabiele ziekte werd gezien bij 54.2% in de lenvatinibgroep en bij 23.0% in de placebogroep.
- Controle over de ziekte werd bereikt bij 87.7% voor lenvatinib versus 55.7% voor plecebogroep (OR = 5.05, P < 001). Mediane tijd tot er zich meetbaar een respons voordeed was 2 maanden in de lenvatinib groep.
- Mediane overall overleving (using rank-preserving structural failure time to adjust for potential crossover bias) is nog niet bereikt in de lenvatinib groep (95% confidence interval = 22.0 maanden tot nog niet bereikt) evenmin voor de placebo groep (95% CI = 14.3 maanden tot nog niet bereikt (HR = 0.62, P = .05).
- Overall overleving was 81.6% voor lenvatinib versus 70.0% voor placebo na 12 maanden en nog niet bereikt voor lenvatinibgroep versus 58.2% voor placebogroep op 24 maanden.
- Gelijke resultaten werden bereikt bij patiënten die nog niet eerder een kinaseremmer hadden gehad als voor diegenen die wel 1 behandeling hadden gehad met een anti-angiogenetische tyrosine kinase remmer.
Voor de bijwerkingen zie ook het volledige studierapport, ik heb dit niet vertaald omdat het heel veel tekst is,: Lenvatinib versus placebo in radioiodine-refractory thyroid cancer.
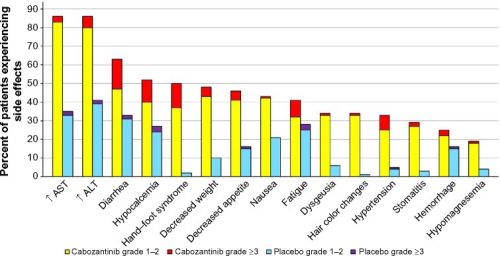
wel hier een grafiek van mogelijk optredende bijwerkingen bij toedienen van tyrosine kinase remmers. :
Foto: bijwerkingen profiel bij cabozantinib, een andere tyrosine kinase remmer
The median duration of treatment was 13.8 months among patients who received lenvatinib and 3.9 months among patients who received placebo. The incidence of treatment-related adverse effects (of all grades) as assessed by the investigator was 97.3% in the lenvatinib group and 59.5% in the placebo group, and the incidence of treatment-related adverse effects of grade 3 or higher was 75.9% in the lenvatinib group and 9.9% in the placebo group (Table 3)
Adverse Effects., and Table S2 in the Supplementary Appendix).
Adverse effects of special interest that developed in the lenvatinib group during treatment were hypertension (any grade, 69.3%; grade ≥3, 42.9%), proteinuria (any grade, 32.2%; grade ≥3, 10.0%), arterial thromboembolic effects (any grade, 5.4%; grade ≥3, 2.7%), venous thromboembolic effects (any grade, 5.4%; grade ≥3, 3.8%), renal failure, including acute renal failure (any grade, 4.2%; grade ≥3, 1.9%), hepatic failure (grade ≥3, 0.4%), gastrointestinal fistula (any grade, 1.5%; grade ≥3, 0.8%), corrected QT prolongation (any grade, 8%; grade ≥3, 1.5%), and the posterior reversible encephalopathy syndrome (any grade, 0.4%; grade ≥3, 0). In patients who received lenvatinib, the median serum thyrotropin levels increased from baseline levels in cycle 1 and peaked by cycle 2. The post-baseline levels of serum thyrotropin increased to more than 0.5 mIU per liter in 158 patients in the lenvatinib group (61.5%).
Conclusie:
“Lenvatinib vergeleken met placebo wordt geassocieerd met een significante verbetering van de progressievrije overleving en mate van kans van aanslaan van de behandeling bij patiënten met vergevorderde uitgezaaide schildklierkanker, resistent voor een radio actieve jodium behandeling - iodine-131. Patienten die lenvatinib kregen ervaarden wel meer bijwerkingen dan bij een placebo.”
Disclosure: This study was funded by Eisai. For full disclosures of the study authors, visit www.nejm.org.
Reference
1. Schlumberger M, Tahara M, Wirth LJ, et al: Lenvatinib versus placebo in radioiodine-refractory thyroid cancer. N Engl J Med 372:621-630, 2015.
Lori J. Wirth, MD, of Dana-Farber/Harvard Cancer Center, discusses treatment options for patients with radioiodine-refractory thyroid cancer.
Hier het abstract van de studie:
Lenvatinib, as compared with placebo, was associated with significant improvements in progression-free survival and the response rate among patients with iodine-131-refractory thyroid cancer. Patients who received lenvatinib had more adverse effects
Lenvatinib versus placebo in radioiodine-refractory thyroid cancer.
Abstract
BACKGROUND:
Lenvatinib, an oral inhibitor of vascular endothelial growth factor receptors 1, 2, and 3, fibroblast growth factor receptors 1 through 4, platelet-derived growth factor receptor α, RET, and KIT, showed clinical activity in a phase 2 study involving patients with differentiated thyroid cancer that was refractory to radioiodine (iodine-131).
METHODS:
In our phase 3, randomized, double-blind, multicenter study involving patients with progressive thyroid cancer that was refractory to iodine-131, we randomly assigned 261 patients to receive lenvatinib (at a daily dose of 24 mg per day in 28-day cycles) and 131 patients to receive placebo. At the time of disease progression, patients in the placebo group could receive open-label lenvatinib. The primary end point was progression-free survival. Secondary end points included the response rate, overall survival, and safety.
RESULTS:
The median progression-free survival was 18.3 months in the lenvatinib group and 3.6 months in the placebo group (hazard ratio for progression or death, 0.21; 99% confidence interval, 0.14 to 0.31; P<0.001). A progression-free survival benefit associated with lenvatinib was observed in all prespecified subgroups. The response rate was 64.8% in the lenvatinib group (4 complete responses and 165 partial responses) and 1.5% in the placebo group (P<0.001). The median overall survival was not reached in either group. Treatment-related adverse effects of any grade, which occurred in more than 40% of patients in the lenvatinib group, were hypertension (in 67.8% of the patients), diarrhea (in 59.4%), fatigue or asthenia (in 59.0%), decreased appetite (in 50.2%), decreased weight (in 46.4%), and nausea (in 41.0%). Discontinuations of the study drug because of adverse effects occurred in 37 patients who received lenvatinib (14.2%) and 3 patients who received placebo (2.3%). In the lenvatinib group, 6 of 20 deaths that occurred during the treatment period were considered to be drug-related.
CONCLUSIONS:
Lenvatinib, as compared with placebo, was associated with significant improvements in progression-free survival and the response rate among patients with iodine-131-refractory thyroid cancer. Patients who received lenvatinib had more adverse effects. (Funded by Eisai; SELECT ClinicalTrials.gov number, NCT01321554.).
Comment in
- Lenvatinib in radioiodine-refractory thyroid cancer. [N Engl J Med. 2015]
- Lenvatinib in radioiodine-refractory thyroid cancer. [N Engl J Med. 2015]
- Neuroendocrine cancer: SELECT—lenvatinib in thyroid cancer. [Nat Rev Clin Oncol. 2015]
- Therapy: Lenvatinib and radioiodine-refractory thyroid cancers. [Nat Rev Endocrinol. 2015]
- PMID:
- 25671254
- [PubMed - indexed for MEDLINE]
Gerelateerde artikelen
- Cryo-ablatie = bevriezing van kwaadaardig tumorweefsel blijkt succesvolle behandeling bij 2 patienten met schildklierkanker uitgevoerd in UMC Maastricht
- Immuuntherapie met Atezolizumab naast een gerichte behandeling met vemurafenib + cobimetinib verbetert sterk de overall overleving bij anaplastische schildklierkanker
- Theranostiek, succesvol bij prostaatkanker en schildklierkanker lijkt ook interessante behandeling voor borstkanker te kunnen zijn, aldus prof. dr. Dalm uit Erasmus MC copy 1
- [18F]FDG-PET/CT-gestuurde diagnose van verdachte schildklierknobbeltjes vermindert nutteloze operaties met 40 procent door goedaardig van kwaadaardig te onderscheiden.
- Schildklierkanker: Bestraling voor andere vormen van kanker veroorzaakt meer en ernstiger vorm van schildklierkanker.
- Selpercatinib (LOXO-292), geeft alsnog uitstekende resultaten (68 procent objectieve respons) met langdurende remissies bij zwaar voorbehandelde RET fusie-positieve niet-kleincellige longkanker met ook hersenuitzaaiingen copy 2
- Oudere patiënten (40 plus) met primaire papillaire schildklierkanker in een actief wait-and-see programma hebben een lager risico op tumorgroei en ziekteprogressie in vergelijking met jongere patienten
- Vier internationale medisch-specialistische verenigingen stellen zorgplan op voor optimale behandelingen voor patiënten met gedifferentieerde schildklierkanker (DTC)
- Anaplastische schildklierkanker (ATC) is een zeldzame vorm van kanker en heel moeilijk te behandelen maar immuuntherapie en gerichte behandelingen op mutaties en eiwitexpressie geven hoopvolle resultaten
- Schildklierkanker: Lenvatinib geeft zeer goede resultaten bij uitbehandelde gevorderde, uitgezaaide schildklierkanker waarbij mediane overleving stijgt van 3,5 naar 18,5 maanden binnen studie van 2 jaar. copy 1
- Wie als baby/kind bestraald is voor een vergrote schildklier loopt sterk vergroot risico op schildklierkanker. Dit risico blijft het hele leven bestaan blijkt uit studie na 50 jaar copy 1




Plaats een reactie ...
Reageer op "Schildklierkanker: Lenvatinib geeft zeer goede resultaten bij uitbehandelde gevorderde, uitgezaaide schildklierkanker waarbij mediane overleving stijgt van 3,5 naar 18,5 maanden binnen studie van 2 jaar. copy 1"