Aan dit artikel is enkele uren gewerkt. Mocht u ons willen helpen kanker-actueel online te houden dan kan dat met een machtiging of directe donatie via: http://kanker-actueel.nl/NL/donaties.html of al of niet anoniem op - rekeningnummer NL79 RABO 0372931138 t.n.v. Stichting Gezondheid Actueel in Terneuzen.
28 maart 2026: aanvullend op onderstaand onderzoek wil ik ook een ander onderzoek naar het onderwerp of studiepublicaties wel altijd correct zijn toevoegen van prof dr. John P. A. Ioannidis werkzaam aan de Stanford universiteit
Hij schrijft o.a. in het abstract: Simulaties tonen aan dat voor de meeste onderzoeksopzetten en -omstandigheden de kans groter is dat een onderzoeksbewering onjuist is dan waar.
De titel van zijn publicatie is:
Het abstract staat onderaan dit artikel. De correctie uit 2022 gaat alleen over een grafiek.
9 oktober 2017: Bron: BMJ 2017;359:j4530
Slechts de helft van de door de European Medicines Agency (EMA) officieel goedgekeurde nieuwe kankermedicijnen geven een mediane verbetering van de overall overleving. Maar die verbetering, als die er al is, blijkt marginaal met een mediane verbetering van overall overleving van 2,7 maanden. (variërend van 1 tot 5,8 maanden). Verbetering van kwaliteit van leven werd in de 23 studies waar dit ook als doel stond bereikt bij 48% (11 uit 23).
De Engelse onderzoekers, Courtney Davis en collega's zijn hard in hun conclusie: veel medicijnen worden beoordeeld en goedgekeurd op basis van ondeugdelijke resultaten of studiedoelen die geen goede voorspellers blijken voor de mate van overleving en/of kwaliteit van leven.
Conclusions: This systematic evaluation of oncology approvals by the EMA in 2009-13 shows that most drugs entered the market without evidence of benefit on survival or quality of life. At a minimum of 3.3 years after market entry, there was still no conclusive evidence that these drugs either extended or improved life for most cancer indications. When there were survival gains over existing treatment options or placebo, they were often marginal.
De studieresultaten zijn afgelopen week gepubliceerd in BMJ.
In de periode 2009 tot en met 2013 gaf de EMA goedkeuring aan 48 kankermedicijnen voor 68 indicaties. Bv. olaparib werd goegekeurd voor zowel borstkankerpatiënten als eierstokkankerpatiënten met een BRCA 1 / 2 mutatie. Bij 35 van de 68 indicaties bij een mediane follow-up van 5,4 jaar vonden de onderzoekers van deze nieuwe studie statistisch significante verbetering van de overleving of verbetering van de kwaliteit van leven. De medicatie voor de andere 33 indicaties liet geen verbetrring van de overall overleving zien en ook geen verbeterde kwaliteit van leven.
Hier een grafiek van de onderzochte medicijnen voor de 68 indicaties. Teskt gaat onder grafiek verder.
Table 1
Characteristics of approvals of cancer drug, 2009-13. Figures are numbers (percentage) of indications
| Characteristics | Solid tumours (n=51) | Haematological tumours (n=17) |
|---|
| Type of marketing authorisation: |
| First marketing authorisation |
24 (47) |
9 (53) |
| Extension |
27 (53) |
8 (47) |
| Pathway of first marketing authorisation: |
| Regular approval |
19 (79) |
4 (44) |
| Conditional approval |
5 (21) |
5 (56) |
| Orphan designation |
3 (6) |
8 (47) |
| Intent of treatment: |
| Curative |
6 (12) |
1 (6) |
| Non-curative |
45 (88) |
16 (94) |
Wat de onderzoekers vooral benadrukken in hun studie is dat geen enkele studie die beslissend was voor de offciële goedkeuring en dus toelating tot de klinische praktijk als doel had ‘kwaliteit van leven’, zelfs niet als het onderzochte middel vooral palliatief werd ingezet. In iets meer dan de helft van de indicaties was kwaliteit van leven een secundair doel van het onderzoek, maar de resultaten daarvan waren echt heel slecht: slechts in zeven studies was er sprake van een statistisch significante verbetering van de kwaliteit van leven.
Deze medicijnen gaven uiteindelijk een verbetering van kwaliteit van leven. Ik heb dit niet vertaald. Anders gebruik google translationknop rechtsboven dit artikel.
Box 2: Cancer drugs associated with benefit on health related quality of life (HRQoL)
Reported at time of market approval
-
Afatinib v pemetrexed/cisplatin (for the treatment of TKI-naive, EGFR mutation +ve, non-small cell lung cancer) significantly delayed the time to deterioration for cough and dyspnoea but not time to deterioration of pain. HRQoL was evaluated against prespecified components of the European Organisation for Research and Treatment of Cancer quality of life questionnaire C30 (EORTC QLQ-C30) questionnaire and lung cancer module QLQ-LC13. The study was open label43
-
Gefitnib (for the treatment of metastatic non-small cell lung cancer) showed significant benefits on quality of life compared with carboplatin plus paclitaxel, and with docetaxel on some measures, but not compared with placebo. HRQoL was assessed with the functional assessment of cancer therapy-lung (FACT-L), and trial outcome index (TOI), and symptom improvement by the lung cancer subscale (LCS). The active comparator trials were open label. The trial v placebo was double blind44
-
Tegafur, gimeracil, oteracil (S-1) (in combination with cisplatin for the treatment of advanced gastric cancer) showed a significant improvement over cisplatin/5-fluorouracil for only one of the subscales (physical wellbeing) of the functional assessment of cancer therapy-gastric (FACT-Ga) HRQOL instrument. The study was open label45
-
Vandetanib v placebo (for the treatment of metastatic medullary thyroid cancer) significantly improved “time to worsening of pain” (a composite endpoint based on patient reported analgesic use and responses to the brief pain inventory) but did not show a significant improvement for the functional assessment of cancer therapy-general (FACT-G) score. The study was double blind46
Reported in the postmarketing period
-
Crizotinib (for second line treatment of ALK mutation +ve advanced non-small cell lung cancer) showed significant improvements compared with pemetrexed across a range of HRQoL measures, including a significantly greater delay in time to worsening of symptoms. HRQoL was assessed with the European Organisation for Research and Treatment of Cancer quality of life questionnaire C30 (EORTC QLQ-C30) and the lung cancer module QLQ-LC13. The study was open label47
-
Erlotinib (for first line treatment of EGFR mutation +ve metastatic non-small cell lung cancer) showed clinically relevant and significant improvements compared with gemcitabine/carboplatin in total functional assessment of cancer therapy-lung (FACT-L), trial outcome index (TOI), and lung cancer subscale (LCS) scores. The study was open label48
-
Nilotinib v imatinib (for patients with newly diagnosed Ph+ chronic myeloid leukaemia) reported a significant quality of life improvement with respect to some categories of low grade adverse events. HRQoL was assessed with generic SF-36 and leukaemia specific functional assessment of cancer therapy-leukaemia (FACT-Leu) surveys. The study was open label42
-
Ofatumumab (in patients with chronic lymphocytic leukaemia refractory to fludarabine and alemtuzumab) showed significant improvements v “physician’s choice” with respect to fatigue but not side effects of treatment or effects of disease. HRQoL was evaluated according to three prespecified domains of the European Organisation for Research and Treatment of Cancer Quality of Life Questionnaire C30 (EORTC-C30) and the chronic lymphocytic leukaemia module QLQ-CLL16 (fatigue, side effects of treatment, and effects of disease). The study was open label49
-
Pazopanib (for first line treatment of advanced renal cell carcinoma) significantly improved HRQoL compared with sunitinib with respect to 11 of 14 HRQoL domains. HRQoL was assessed with the functional assessment of chronic illness therapy-fatigue (FACIT-F) questionnaire, the National Comprehensive Cancer Network/functional assessment of cancer therapy-kidney symptom index 19 (NCCN-FACT FKSI-19), and the cancer therapy satisfaction questionnaire. The study was open label50
Het overzicht van de belangrijkste onderzochte medicijnen, is wel klein maar hopelijk nog wel te lezen:
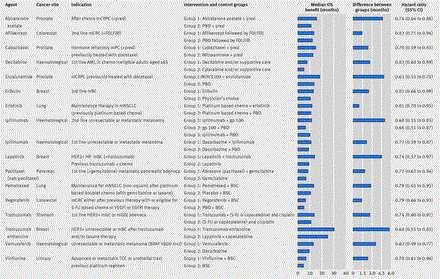
Fig 1 Magnitude of overall survival benefit at the time of EMA approval. Figure excludes seven indications for which median overall survival could not be estimated at time of marketing authorisation: mifamurtide for resectable non-metastatic osteosarcoma after complete resection (+chemo); pertuzumab for 1st line HER2+mBC; pomalidomide for 3rd line (+dexamethasone) relapsed and refractory multiple myeloma; rituximab for 1st line CLL (+chemo); trastuzumab for HER2+ BC (+taxane) after adjuvant chemo; trastuzumab for HER2+BC (+adjuvant chemo); and trastuzumab for HER2+locally advanced BC (+neoadjuvant chemo and as monotherapy adjuvantly). Box 1 shows abbreviations used
Hier een grafiek van de efectiviteit van de goedgekeurde medicijnen nadat zij op de markt kwamen:
Fig 2 Availability of benefits on overall survival and quality of life of cancer drugs approved 2009-13. Box 1 shows abbreviations used

Deborah Cohen, verbonden aan BMJ, heeft in de studies die zij beoordeelden een heleboel fouten geconstateerd, zoals methodologische fouten in het ontwerp, de uitvoering, de analyse en de verslaglegging. Die zijn volgens haar allemaal door de EMA over het hoofd gezien.
Dat medicijnen op ondeugdelijke gronden worden toegelaten, heeft volgens Deborah Cohen ernstige gevolgen. Zij geeft twee voorbeelden. De eerste: een publicatie met statistisch hoopgevende resultaten leidt tot onrealistische verwachtingen bij kankerpatiënten en ook bij oncologen. En het tweede uunt dat Deborah Cohen maakt: het ontbreken van een goed onderbouwd bewijs van de effectiviteit brengt de betalende instanties en regeringen in een moeilijk parket in hun onderhandelingen met de producenten van de medciijnen. Wat te doen met de financiering van deze dure geneesmiddelen?
Al met al dus een ontluisterend beeld. Dat alleen maar bevestigd dat de kankerpatient zelf totaal onbelangrijk is in het wetenschappelijke onderzoek
Het volledige studierapport: Availability of evidence of benefits on overall survival and quality of life of cancer drugs approved by European Medicines Agency: retrospective cohort study of drug approvals 2009-13 is gratis in te zien.
Hier het abstract met referentielijst:
This systematic evaluation of oncology approvals by the EMA in 2009-13 shows that most drugs entered the market without evidence of benefit on survival or quality of life. At a minimum of 3.3 years after market entry, there was still no conclusive evidence that these drugs either extended or improved life for most cancer indications. When there were survival gains over existing treatment options or placebo, they were often marginal.
Availability of evidence of benefits on overall survival and quality of life of cancer drugs approved by European Medicines Agency: retrospective cohort study of drug approvals 2009-13
BMJ 2017; 359 doi: https://doi.org/10.1136/bmj.j4530 (Published 04 October 2017) Cite this as: BMJ 2017;359:j4530
- Courtney Davis, senior lecturer1,
- Huseyin Naci, assistant professor of health policy2,
- Evrim Gurpinar, MSc candidate in international health policy 2,
- Elita Poplavska, assistant professor3,
- Ashlyn Pinto, MSc candidate in global health2,
- Ajay Aggarwal, academic clinical oncologist4 5
Author affiliations
- 1Department of Global Health and Social Medicine, King’s College London, London WC2R 2LS, UK
- 2LSE Health, Department of Health Policy, London School of Economics and Political Science, London, UK
- 3Faculty of Pharmacy, Riga Stradins University, Riga, Latvia
- 4Department of Health Services Research and Policy, London School of Hygiene and Tropical Medicine, London, UK
- 5Institute of Cancer Policy, King’s College London, London, UK
- Correspondence: C Davis courtney.davis@kcl.ac.uk
- Accepted 28 September 2017
Abstract
Objective To determine the availability of data on overall survival and quality of life benefits of cancer drugs approved in Europe.
Design Retrospective cohort study.
Setting Publicly accessible regulatory and scientific reports on cancer approvals by the European Medicines Agency (EMA) from 2009 to 2013.
Main outcome measures Pivotal and postmarketing trials of cancer drugs according to their design features (randomisation, crossover, blinding), comparators, and endpoints. Availability and magnitude of benefit on overall survival or quality of life determined at time of approval and after market entry. Validated European Society for Medical Oncology Magnitude of Clinical Benefit Scale (ESMO-MCBS) used to assess the clinical value of the reported gains in published studies of cancer drugs.
Results From 2009 to 2013, the EMA approved the use of 48 cancer drugs for 68 indications. Of these, eight indications (12%) were approved on the basis of a single arm study. At the time of market approval, there was significant prolongation of survival in 24 of the 68 (35%). The magnitude of the benefit on overall survival ranged from 1.0 to 5.8 months (median 2.7 months). At the time of market approval, there was an improvement in quality of life in seven of 68 indications (10%). Out of 44 indications for which there was no evidence of a survival gain at the time of market authorisation, in the subsequent postmarketing period there was evidence for extension of life in three (7%) and reported benefit on quality of life in five (11%). Of the 68 cancer indications with EMA approval, and with a median of 5.4 years’ follow-up (minimum 3.3 years, maximum 8.1 years), only 35 (51%) had shown a significant improvement in survival or quality of life, while 33 (49%) remained uncertain. Of 23 indications associated with a survival benefit that could be scored with the ESMO-MCBS tool, the benefit was judged to be clinically meaningful in less than half (11/23, 48%).
Conclusions This systematic evaluation of oncology approvals by the EMA in 2009-13 shows that most drugs entered the market without evidence of benefit on survival or quality of life. At a minimum of 3.3 years after market entry, there was still no conclusive evidence that these drugs either extended or improved life for most cancer indications. When there were survival gains over existing treatment options or placebo, they were often marginal.
This is an Open Access article distributed in accordance with the Creative Commons Attribution Non Commercial (CC BY-NC 4.0) license, which permits others to distribute, remix, adapt, build upon this work non-commercially, and license their derivative works on different terms, provided the original work is properly cited and the use is non-commercial. See: http://creativecommons.org/licenses/by-nc/4.0/.
References
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
Gutman SI, Piper M, Grant MD, et al. Progression-Free Survival: What Does It Mean for Psychological Well-Being or Quality of Life? Rockville (MD), 2013.
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
Official Journal of the European Union. Commission Regulation (EC) No. 507/2006, of 29 March 2006 on the conditional marketing authorisation for medicinal products for human use falling within the scope of Regulation (EC) No 726/2004 of the European Parliament and of the Council, 2006.
- ↵
Higgins JPT Green S. Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0 (updated March 2011). Cochrane Collaboration, 2011. 2011
- ↵
- ↵
- ↵
EMA. EMA/CHMP/815425/2010, 16 December 2010. 2010
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
- ↵
- ↵
- ↵
- ↵
European Medicines Agency. Appendix 2 to the guideline on the evaluation of anticancer medicinal products in man. The use of patient-reported outcome measures in oncology studies. EMA/CHMP/292464/2014, 2014.
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
EMA. EMA, EMEA/H/C/000795/II/0022 pp 47-48.
- ↵
- ↵
EMA. Guideline on the evaluation of anticancer medicinal products in man. EMA/CHMP/205/95/Rev4 13 December 2012 2012
- ↵
- ↵
- ↵
- ↵
- ↵
Simulations show that for most study designs and settings, it is more likely for a research claim to be false than true. Moreover, for many current scientific fields, claimed research findings may often be simply accurate measures of the prevailing bias. In this essay, I discuss the implications of these problems for the conduct and interpretation of research.
Published: August 30, 2005
Abstract
Summary
There is increasing concern that most current published research findings are false. The probability that a research claim is true may depend on study power and bias, the number of other studies on the same question, and, importantly, the ratio of true to no relationships among the relationships probed in each scientific field. In this framework, a research finding is less likely to be true when the studies conducted in a field are smaller; when effect sizes are smaller; when there is a greater number and lesser preselection of tested relationships; where there is greater flexibility in designs, definitions, outcomes, and analytical modes; when there is greater financial and other interest and prejudice; and when more teams are involved in a scientific field in chase of statistical significance. Simulations show that for most study designs and settings, it is more likely for a research claim to be false than true. Moreover, for many current scientific fields, claimed research findings may often be simply accurate measures of the prevailing bias. In this essay, I discuss the implications of these problems for the conduct and interpretation of research.
Citation: Ioannidis JPA (2005) Why Most Published Research Findings Are False. PLoS Med 2(8): e124. https://doi.org/10.1371/journal.pmed.0020124
Published: August 30, 2005
Copyright: © 2005 John P. A. Ioannidis. This is an open-access article distributed under the terms of the Creative Commons Attribution License, which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Competing interests: The author has declared that no competing interests exist.
References
- 1.Ioannidis JP, Haidich AB, Lau J (2001) Any casualties in the clash of randomised and observational evidence? BMJ 322: 879–880.
- 2.Lawlor DA, Davey Smith G, Kundu D, Bruckdorfer KR, Ebrahim S (2004) Those confounded vitamins: What can we learn from the differences between observational versus randomised trial evidence? Lancet 363: 1724–1727.
- 3.Vandenbroucke JP (2004) When are observational studies as credible as randomised trials? Lancet 363: 1728–1731.
- 4.Michiels S, Koscielny S, Hill C (2005) Prediction of cancer outcome with microarrays: A multiple random validation strategy. Lancet 365: 488–492.
- 5.Ioannidis JPA, Ntzani EE, Trikalinos TA, Contopoulos-Ioannidis DG (2001) Replication validity of genetic association studies. Nat Genet 29: 306–309.
- 6.Colhoun HM, McKeigue PM, Davey Smith G (2003) Problems of reporting genetic associations with complex outcomes. Lancet 361: 865–872.
- 7.Ioannidis JP (2003) Genetic associations: False or true? Trends Mol Med 9: 135–138.
- 8.Ioannidis JPA (2005) Microarrays and molecular research: Noise discovery? Lancet 365: 454–455.
- 9.Sterne JA, Davey Smith G (2001) Sifting the evidence—What's wrong with significance tests. BMJ 322: 226–231.
- 10.Wacholder S, Chanock S, Garcia-Closas M, Elghormli L, Rothman N (2004) Assessing the probability that a positive report is false: An approach for molecular epidemiology studies. J Natl Cancer Inst 96: 434–442.
- 11.Risch NJ (2000) Searching for genetic determinants in the new millennium. Nature 405: 847–856.
- 12.Kelsey JL, Whittemore AS, Evans AS, Thompson WD (1996) Methods in observational epidemiology, 2nd ed. New York: Oxford U Press. 432 p.
- 13.Topol EJ (2004) Failing the public health—Rofecoxib, Merck, and the FDA. N Engl J Med 351: 1707–1709.
- 14.Yusuf S, Collins R, Peto R (1984) Why do we need some large, simple randomized trials? Stat Med 3: 409–422.
- 15.Altman DG, Royston P (2000) What do we mean by validating a prognostic model? Stat Med 19: 453–473.
- 16.Taubes G (1995) Epidemiology faces its limits. Science 269: 164–169.
- 17.Golub TR, Slonim DK, Tamayo P, Huard C, Gaasenbeek M, et al. (1999) Molecular classification of cancer: Class discovery and class prediction by gene expression monitoring. Science 286: 531–537.
- 18.Moher D, Schulz KF, Altman DG (2001) The CONSORT statement: Revised recommendations for improving the quality of reports of parallel-group randomised trials. Lancet 357: 1191–1194.
- 19.Ioannidis JP, Evans SJ, Gotzsche PC, O'Neill RT, Altman DG, et al. (2004) Better reporting of harms in randomized trials: An extension of the CONSORT statement. Ann Intern Med 141: 781–788.
- 20.International Conference on Harmonisation E9 Expert Working Group (1999) ICH Harmonised Tripartite Guideline. Statistical principles for clinical trials. Stat Med 18: 1905–1942.
- 21.Moher D, Cook DJ, Eastwood S, Olkin I, Rennie D, et al. (1999) Improving the quality of reports of meta-analyses of randomised controlled trials: The QUOROM statement. Quality of Reporting of Meta-analyses. Lancet 354: 1896–1900.
- 22.Stroup DF, Berlin JA, Morton SC, Olkin I, Williamson GD, et al. (2000) Meta-analysis of observational studies in epidemiology: A proposal for reporting. Meta-analysis of Observational Studies in Epidemiology (MOOSE) group. JAMA 283: 2008–2012.
- 23.Marshall M, Lockwood A, Bradley C, Adams C, Joy C, et al. (2000) Unpublished rating scales: A major source of bias in randomised controlled trials of treatments for schizophrenia. Br J Psychiatry 176: 249–252.
- 24.Altman DG, Goodman SN (1994) Transfer of technology from statistical journals to the biomedical literature. Past trends and future predictions. JAMA 272: 129–132.
- 25.Chan AW, Hrobjartsson A, Haahr MT, Gotzsche PC, Altman DG (2004) Empirical evidence for selective reporting of outcomes in randomized trials: Comparison of protocols to published articles. JAMA 291: 2457–2465.
- 26.Krimsky S, Rothenberg LS, Stott P, Kyle G (1998) Scientific journals and their authors' financial interests: A pilot study. Psychother Psychosom 67: 194–201.
- 27.Papanikolaou GN, Baltogianni MS, Contopoulos-Ioannidis DG, Haidich AB, Giannakakis IA, et al. (2001) Reporting of conflicts of interest in guidelines of preventive and therapeutic interventions. BMC Med Res Methodol 1: 3.
- 28.Antman EM, Lau J, Kupelnick B, Mosteller F, Chalmers TC (1992) A comparison of results of meta-analyses of randomized control trials and recommendations of clinical experts. Treatments for myocardial infarction. JAMA 268: 240–248.
- 29.Ioannidis JP, Trikalinos TA (2005) Early extreme contradictory estimates may appear in published research: The Proteus phenomenon in molecular genetics research and randomized trials. J Clin Epidemiol 58: 543–549.
- 30.Ntzani EE, Ioannidis JP (2003) Predictive ability of DNA microarrays for cancer outcomes and correlates: An empirical assessment. Lancet 362: 1439–1444.
- 31.Ransohoff DF (2004) Rules of evidence for cancer molecular-marker discovery and validation. Nat Rev Cancer 4: 309–314.
- 32.Lindley DV (1957) A statistical paradox. Biometrika 44: 187–192.
- 33.Bartlett MS (1957) A comment on D.V. Lindley's statistical paradox. Biometrika 44: 533–534.
- 34.Senn SJ (2001) Two cheers for P-values. J Epidemiol Biostat 6: 193–204.
- 35.De Angelis C, Drazen JM, Frizelle FA, Haug C, Hoey J, et al. (2004) Clinical trial registration: A statement from the International Committee of Medical Journal Editors. N Engl J Med 351: 1250–1251.
- 36.Ioannidis JPA (2005) Contradicted and initially stronger effects in highly cited clinical research. JAMA 294: 218–228.
- 37.Hsueh HM, Chen JJ, Kodell RL (2003) Comparison of methods for estimating the number of true null hypotheses in multiplicity testing. J Biopharm Stat 13: 675–689.
DRUP studie, overzicht van personalised medicine, receptorenonderzoek, eiwitexpressie, DNA mutaties, prognosemodel, Personalized Cancer Treatment (CPCT), kwaliteit van leven
Gerelateerde artikelen
- Algemene artikelen die met kanker te maken hebben maar niet specifiek bij een vorm van kanker
- Aflibercept (Zaltrap) toegevoegd aan een chemo combinatie van fluorouracil - 5-FU, leucovorine en irinotecan (FOLFIRI) verbetert de overleving en progressievrije tijd met 1,5 maand
- Aprepitant - Emend is een geneesmiddel dat de bijwerkingen van chemokuren vermindert en inmiddels veelgebruikt middel om misselijkheid bij chemo tegen te gaan
- Avastin - Bevacizumab, een angiogenese remmer die bij een aantal vormen van kanker gebruikt wordt inmiddels: overzicht van een aantal studies en belangrijke artikelen
- BBBD-behandeling (Blood Brain Barrier Disruption) bij lymfomen (tumoren) van centrale zenuwstelsel succesvol en hoog significant aldus fase II studie.
- Bloedcellen: Onze longen ondersteunen ons beenmerg in het maken van rode bloedcellen, bloedplaatjes en immuuncellen.
- Beenmergtransplantaties en stamceltransplantaties: Studiepublicaties van niet-toxische middelen en behandelingen uit literatuurlijst van arts-bioloog drs. Engelbert Valstar naast beenmergtransplantaties en stamceltransplantaties
- Bloedarmoede (anemia) en ESA's : Medicijnen die de aanmaak van rode bloedlichaampjes stimuleren en vaak ingezet worden tegen bloedarmoede en moeheid geven een groter risico (17%) om te sterven tijdens de chemo en geeft kortere mediane overlevingstijd.
- Boekenlijst met daarop titels van boeken die op een of andere manier in relatie staan tot kanker en omgaan daarmee
- Celebrex - een zogeheten COX-2 remmer geeft 2,5 keer zo groot risico op ernstige hartklachten aldus gerandomiseerde dubbelblinde langjarige studie. Aandeel van producent Pfizer zakte 17% in waarde op 1 dag.
- Chemo en voedingsondersteuning: een overzicht van een aantal studies en opinies bij elkaar in 1 overzicht. Inclusief studielijst chemo en voedingstoffen
- Clolar - clofarabine plus busulfan geeft uitstekende resultaten bij ALL - Acute lymfatische Leukemie en stamceltransplantatie
- COBALT - Combination Bacteriolytic Therapy - chemo en bacteriën succesvol in dierproeven, maar wordt ook bekritiseerd door hoge toxiciteit
- Cryosurgery bij goedaardige en kleine kwaadaardige bottumoren - chondrosarcomen - wordt vaak succesvol en genezend toegepast.
- Da Vinci robot werkt effectief en nauwkeurig bij o.a. prostaatkanker
- Dendritische celtherapie informatie en studies enz. bij elkaar gezet in 1 artikelenreeks
- Denosumab geeft prostaatkankerpatienten met risico op recidief significant langere tijd tot zich botuitzaaiingen voordoen, maar geen verbetering van overall overleving
- Diagnose: Kanker zonder primaire oorsprong komt minder voor door betere diagnostiek, maar kans op overlijden blijft gelijk.
- Dolasetron, injectie om misselijkheid bij chemo tegen te gaan geeft vergroot risico op hartfalen, waarschuwt de FDA. Dolasetron mag niet meer gebruikt worden in hoge dosis.
- EGRF remmers zoals Tarceva - Erlotinib en Iressa - Gefitinib: een overzicht
- Epigenetische behandeling met Azacitidine en Entinostat blijkt succesvolle aanpak van niet-klein-cellige longkanker
- Erbitux - Cetuximab, een overzicht van belangrijke studies en recente ontwikkelingen..
- Everolimus vermindert sterk epileptische aanvallen bij patiënten met het tubereuze sclerose complex, goedaardige tumoren in de hersenen vanuit erfelijke oorsprong en verbetert kwaliteit van leven aanzienlijk.
- Gamma-Knife - Stereotactische bestraling - informatie bij elkaar gezet
- Gentherapie met p53 virus (gendicine) en hyperthermie zorgt voor spectaculaire verbeteringen bij patienten met vergevorderde kanker blijkt uit kleinschalige fase 2 studie.
- Gleevec - Imatinib: een overzicht van belangrijke studies en recente ontwikkelingen met dit medicijn
- Goedkeuring van nieuwe kankermedicijnen meestal gebaseerd op te weinig bewijs en geven in de praktijk slechts bij de helft kleine verbeteringen in mediane overleving.
- Heparine, laag moleculair gewicht, blijkt overlevingstijd van kankerpatiënten met solide tumoren en zonder uitzaaiïngen significant te beinvloeden, aldus Nederlandse studie
- Hersenmetastases: Hardnekkige misvattingen over behandelen van uitzaaiingen in de hersenen maken dat veel patiënten verkeerd worden behandeld en heeft grote gevolgen voor therapeutisch effect op ziektevrije tijd en overall overleving
- Herceptin - trastuzumab: een overzicht
- HPV test voor vrouwen goedgekeurd door FDA
- HYPEC - Hypertherme Intra Peritoneale Chemotherapie informatie
- Hyperthermie in combinatie met doelgerichte en immuuntherapeutische behandelingen is veel belovende combinatiebehandeling voor kankerpatienten, aldus artsen van ELMEDIX van de universiteit van Antwerpen
- Hyperthermie: Electromagnetische velden - TT fields therapie als aanvulling op andere behandelingen zorgen voor uitstekende resultaten bij o.a. borstkanker, hersentumoren en longtumoren, aldus verschillende studies.
- Hyperthermie: Informatie over hyperthermie bij elkaar gezet inclusief rapporten van aantal studies bij o.a. borstkanker, blaaskanker, hyperthermie als aanvulling op bestraling enz..
- HIFU = High Intensity Focused Ultrasound: Bottumoren verwijderen met HIFU = High Intensed Focused Ultrasound naast chemo geeft uitstekende resultaten ten opzichte van alleen chemo of aleen operatie. Artikel update 6 november 2010
- Hormoontherapie om bijwerkingen van overgang te verminderen heeft effect op structuur van hersenen en cognitieve functies blijkt uit placebo gecontroleerde studie
- Hyperbare zuurstof geeft uitstekende resultaten op het herstel van beschadigingen door bestralingen en geeft ook veel pijnverlichting. 76.7 tot 92.6 procent betere kwaliteit van leven
- IMRT - intensiteitsgemoduleerde radiotherapie
- INGN 241 , een nieuw virsuachtig medicijn dat direct in tumor moet worden ingespoten, geeft in fase I studie bij 22 kankerpatiënten 100% resultaat. Artikel geplaatst juni 2005
- Ipilimumab, een immuuntherapeutisch medicijn geeft hoopgevende resultaten op langere overleving bij patienten met een melanoom graad III en IV die al eerder intensief behandeld zijn. FDA keurt ipilimumab goed als medicijn bij gevorderde melanomen
- JAMA oncologie geeft een overzicht van de door hun geaccepteerde en goedgekeurde studieverslagen in het jaar 2025
- Lymfklierkanker: reviewstudie van 37 case studies met meerdere vormen van kanker uit een groep van 810 patiënten met lymfklierkanker en hoe bepaalde reguliere aanpak wel of niet werkte en deze studie geeft mooi inzicht in behandeling van lymfklierkanker
- Melanomen: overzicht van artikelen en studies binnen reguliere oncologie. Scroll in linkerkolom voor artikelen. Update 2 april 2010 copy 1
- Metformine: Kankerpatiënten met diabetes (type 2) die metformine gebruiken overleven langer en blijven langer zonder ziekteprogressie dan kankerpatienten plus suikerziekte die geen metaformine gebruiken. Zelfs beter dan kankerpatienten zonder diabetes
- Morfine: Obstipatie bij morfine en andere opioiden als pijnstiller wordt verlicht door Relistor is een officieel goedgekeurd medicijn tegen obstipatie bij o.a. morfinegebruik. Toegevoegd TNO rapport over obstipatie bij sterke pijnmedicatie via morfine
- Nanotechnologie - nanotherapie wordt als toepassing bij medicijnen steeds vaker gebruikt.
- Newcastle Disease Virus - NDV informatie
- NOVO TTF behandeling met electrische pulsen en thuis te gebruiken voor meerdere vormen van kanker
- Pijnbestrijding bij kanker: enkele opties bij elkaar gezet
- PIPAC - verneveling van chemotherapie toegediend via kijkoperatie in de buikholte voor met name buikvliestumoren geeft goede resultaten
- Probiotica - melkzuurbacterien: informatie over wat is probiotica en effecten van probiotica bij o.a. darmkanker en ziekte van Crohn copy 1
- Protonenbestraling
- Provenge als immuuntherapeutisch middel bij gevorderde prostaatkanker geeft significant meer overlevingen indien gegeven samen met dendritische celtherapie. Blijkt uit Fase III studie.
- RFA - Radio Frequency Ablation: een overzicht van recente ontwikkelingen
- Reolysin, een overzicht van recente ontwikkelingen en belangrijke studies met dit virus medicijn
- Sarcomas - Ewing sarcoma: klik hier voor meer artikelen over reguliere ontwikkelingen bij sarcomas en ewing sarcoma
- Scans en ook foto's bij de tandarts veroorzaken honderden nieuwe gevallen van kanker per jaar alleen al in Engeland en duizenden doden door kanker wereldwijd aldus studie aan universiteit van Oxfort
- TACE - Trans Arteriele Chemo Embolisatie en LITT - Laser Induced Interstitual Thermotherapy informatie
- Thalidomide: REVLIMID - lenalidomide studie bij hormoonresistente prostaatkanker wordt gestopt wegens geen resultaat. Bij andere vormen van kanker - CLL en non-Hodgkin gaan studies wel verder met tot nu toe goede resultaten
- Tyrosine-kinase remmers: waarschuwing voor interacties met andere medicijnen die werking van deze klasse van medicijnen kan verminderen of blokkeren stellen Nederlandse onderzoekers in The Lancet
- Ultra Sound = RFA naast TACE geeft hoog significant betere resultaten dan alleen TACE bij levertumoren met een gemiddelde grootte van 10,4 cm. !!!!!, aldus twee gerandomiseerde studies bij totaal 200 patiënten met levertumoren.
- Voeding en voedingstoffen en effect naast reguliere behandelingen: Onder onderzoek en voeding staan vele artikelen en studies die bewijzen dat aanvullende voeding en voedingsuppletie naast reguliere behandelingen vaak de effectiviteit van de behandeling v
- Yttrium-90: Embolisatie met microspheres (Yttrium-90) direct gevolgd door RFA blijkt voor inoperabele levertumoren succesvolle behandeling.
- Zometa - Zoledronic Acid informatie: recente ontwikkelingen en belangrijke studies bij elkaar gezet





Plaats een reactie ...
Reageer op "Goedkeuring van nieuwe kankermedicijnen meestal gebaseerd op te weinig bewijs en geven in de praktijk slechts bij de helft kleine verbeteringen in mediane overleving."