Helpt u ons aan 500 donateurs?
13 februari 2018: Lees ook dit artikel:
en dit artikel:
13 februari 2018: Bron ASCO GU 2018
Bij mannen met castratie-resistente prostaatkanker zonder zichtbare uitzaaiingen en snel stijgende PSA is een behandeling met enzalutamide bijzonder succesvol. Uit een placebo gecontroleerde fase III studie blijkt enzalutamide in vergelijking met placebo een statistisch significante vermindering van 71% te geven iop het risico van uitzaaiingen.
Dit bljkt uit de fase III PROSPER studie en gepresenteerd op het 2018 American Society of Clinical Oncology (ASCO) Genitourinary Cancers Symposium, from February 8 – 10 2018.
In totaal hebben 1401 mannen deelgenomen aan deze studie. De mediane leeftijd was 74 jaar in de enzalutamide-groep (n = 933). De mediane leeftijd was 73 jaar in de placebogroep (n = 468).
Enzalutamide verlengde de mediane uitzaaingsvrije overleving statistisch significant met 22,1 maanden (36,6 versus 14,7 maanden [P <.0001]), de tijd tot het eerste gebruik van een nieuwe behandeling met 21,9 maanden (39,6 versus 17,7 maanden [P <.0001]) en de tijd tot PSA-progressie met 33,3 maanden (37,2 versus 3,9 maanden [P <.0001]) allemaal in vergelijking met de placebogroep.
In de eerste tussentijdse analyse van de algehele overleving was er een trend naar betere oaveall overleving voor enzalutamide (hazard ratio 0,80; P = .1519). De mediane duur van de behandeling was 18,4 versus 11,1 maanden voor enzalutamide versus placebo.
Bijwerkingen waren hoger met enzalutamide dan met placebo (alle bijwerkingen 87% versus 77%, graad ≥3: 31% versus 23%, ernstige bijwerkingen: 24% versus 18%). Van de patiënten die enzalutamide kregen, stopte 10% de behandeling vanwege bijwerkingen versus 8% van degenen die placebo kregen.
Er is zover ik kan zien nog studierapport beschikbaar maar zal dat erbij plaatsen zodra dit wordt vrijgegeven.
4 september 2016: lees ook dit artikel:
10 januari 2016: lees ook dit artikel:
17 mei 2015: Lees ook deze twee artikelen:
en deze:
5 mei 2015: Bron The Lancet
In the Lancet zijn recente studieresultaten uit de PREVAIL studie, een placebo gecontroleerde gerandomiseerde fase III studie bij patiënten met hormoonresistente in de botten uitgezaaide prostaatkanker gepresenteerd die eerdere uitstekende tussenresultaten bevestigen. Enzalutamide geeft ook voor prostaatkankerpatiënten die nog geen chemo hebben gehad significant betere resultaten op pijn en op de tijd tot zich botprogressie / een botbreuk voordoet en heel belangrijk betere mediane progressievrije tijd. Mediane overall overleving is nog niet bekend omdat einddoel nog niet is bereikt maar zal ongetwijfeld beter zijn gezien de tussenresultaten.
 Zie hier het abstract van de studie uit The Lancet:
Zie hier het abstract van de studie uit The Lancet:
http://www.thelancet.com/journals/lanonc/article/PIIS1470-2045%2815%2970113-0/abstract en lees ook onderstaande informatie.
Maar op de website van de producent staat ook mooi overzicht van deze PREVAIL studie: https://www.xtandihcp.com/prevail-trial
27 oktober 2014: Bron: EMA / CHMP
Enzalutamide (XTANDI) wordt nu officieel ook aanbevolen voordat iemand met hormoonresistente prostaatkanker chemo heeft gehad. Tot nu toe werd enzalutamide officieel pas na chemo voorgeschreven maar mag dus nu ook voor chemo worden voorgeschreven. Zie hier het officiële document van de EMA / CHMP over enzalutamide:
http://www.ema.europa.eu/docs/en_GB/document_library/Summary_of_opinion/human/002639/WC500176322.pdf
15 augustus 2014: uit de AFFIRM fase III studie blijkt ook dat enzalutamide een significante verbetering gaf te zien van enzalutamide t.o.v. een placebo:
- de eerste problemen door bot metastases deden zich voor na 16.7 maanden vs 13.3 maanden in de placebogroep (hazard ratio = 0.69, P = .0001),
- na 1 jaar was er ook een significant verschil op vrij van problemen door botmetastases (62.0% vs 52.9%)
- Significant minder pijn. Meer pijn op meting via pijnscoretable in 13 weken deed zich voor bij 174 (28%) van de 625 evalueerbare patiënten die enzalutamide hadden gekregen vs 101 (39%) van de 259 patiënten die een placebo ontvingen (difference= −11.2%, P = .0018). Mediane tijd tot pijnprogressie is nog niet bereikt in de enzalutamidegroep vs 13.8 maanden (HR = 0.56, P = .0004) in de placebo groep.
- patiënten uit de Enzalutamide groep hadden significant betere resultaten op de toegenomen ernst van de pijn (vanaf de basismeting = −0.15 vs +0.50, P < .0001) en pijn pain interference (mean change in score from baseline = −0.01 vs +0.74, P < .0001). Pijnpallaitie (≥ 30% reductie in pijn scores zonder een begeleidende pijnstiller of ≥30% dosisstijging van bv. pijnstillers uit de morfinegroep) in week 13 werd gezien bij 22 (45%) van de 49 evalueerbare enzalutamide patienten uit de enzalutamidegroep vs 1 (7%) van de 15 patienten uit de placebogroep (P = .0079).
Significant betere kwaliteit van leven werd ook gezien, zie daarvoor onderaan het abstract van de publicatie. Ik heb namelijk de resultaten zoals die zijn gepubliceerd in The Lancet: Effect of enzalutamide on time to first skeletal-related event, pain, and quality of life in men with castration-resistant prostate cancer: results from the randomised, phase 3 AFFIRM trial onderaan dit artikel toegevoegd.
5 augustus 2014: Lees ook het artikel over bloedtest die biomarker AR-V7 kan aantonen via in bloed circulerende tumorcellen en van grote waarde blijkt voor prognose of Abiraterone en enzalutamide wel of niet zal aanslaan bij patiënten met uitgezaaide hormoonresistente prostaatkanker.
4 juli 2014: Het volledige studierapport: Enzalutamide in Metastatic Prostate Cancer before Chemotherapy is inmiddels gepubliceerd nadat het op ASCO 2014 is gepresenteerd en gratis in te zien. Enzalutamide blijkt dus superieure resultaten op te leveren. Hieronder heb ik Nederlandse vertaling gemaakt van de resultaten enz.
16 april 2014: Bron: 29th Annual EAU Congress
Ook op het Congres van Europese Association of Urology - EAU werd onderstaande studie gepresenteerd als een van de belangrijkste van afgelopen jaren voor uitgezaaide prostaatkanker. Lees hier maar het persbericht van de EAU.
29 januari 2014: Bron: Genitourirany Symposium 2014
Enzalutamide, een hormoon receptorblokker in tabletvorm, vertraagt progressie van uitgezaaide prostaatkanker in vergelijking met placebo met 81%. En progressie vrije tijd werd verlengd van 5,4 maanden naar 17,1 maanden.
Dit blijkt uit de tussenresultaten uit de PREVAIL studie. Een placebo gecontroleerde fase III studie (zie studieprotocol http://clinicaltrials.gov/show/NCT01212991) bij totaal 1717 mannen met hormoonresistente uitgezaaide prostaatkanker, maar die nog geen chemo hebben gehad. Deze studieresultaten werden gepresenteerd door Tomasz M. Beer, MD van het Oregon Health & Science University-Knight Cancer Institute, Portland op het Genitourirany Symposium 2014
Nu klinkt 81% spectaculairder dan het in werkelijkheid is want in deze studie is vergeleken met een placebo en niet met andere middelen zoals abiraterone bv. Echter het is toch wel een bijzonder resultaat want ook stopte of vertraagde enzalutamide de groei van kanker in zachte weefsel bij 59 % van de patiënten (20 % bereikten alsnog een complete remissie en 39 % een gedeeltelijke remissie) tegenover slechts 5 % van de patiënten uit placebogroep waarbij geen progressie verder werd gezien.
Voor alle duidelijkheid enzalutamine, voorheen bekend onder codenaam MDV3100)(Xtandi , Medivation / Astellas) is een medicijn dat getest is bij mannen waarbij de prostaatkanker al uitgezaaid is en waarvoor in principe als behandeling alleen nog een behandeling met chemo - docetaxel wordt voorgeschreven. Uiteindelijk blijkt de mediane overall overleving op dit moment nog niet zo heel veel te verschillen tussen de placebogroep en de enzalutamide groep hoewel hierover nog geen definitieve cijfers kunnen worden geven omdat het eindpunt wat dit studiedoel betreft nog niet is bereikt bij een deel van de deelnemers.
Enzalutamide is een zogeheten hormoon receptorblokker en werkt anders dan de gebruikelijke hormoonblokkers zoals bicalutamide, flutamide en nilutamide. Ook de FDA (zie http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm317838.htm) in 2012 en de EMU (zie http://www.ema.europa.eu/docs/en_GB/document_library/Summary_of_opinion_-_Initial_authorisation/human/002639/WC500142493.pdf ) in 2013 hebben enzalutamide goedgekeurd voor gebruik als tweede lijns behandeling na chemo maar er gaan nu stemmen op om enzalutamide juist voor de chemo als eerste lijns voor te schrijven. Zie ook voor meer inforamtie in gerelateerde artikelen hieronder of hiernaast.
Ik heb het abstract zo goed als mogelijk proberen te vertalen in het Nederlands:
Studieresultaten PREVAIL studie:
Achtergrond:
Enzalutamide een oraal toegediende androgene receptor remmer, verbeterde de algemene overleving ( OS ) bij mannen met mCRPC (uitgezaaide chemo hormoonresistente prostaatkanker) die een eerdere behandeling met docetaxel
( Scher et al. , NEJM 367:13 , 2012 ) hadden gekregen . Deze studie onderzocht of enzalutamide de algemene overleving OS en progressie vrije overleving ( RPFS ) kon verlengen van asymptomatische of mild symptomatische chemo-naieve mannen met mCRPC.
Methoden:
In deze gerandomiseerde, dubbelblinde, placebo-gecontroleerde, multinationale fase 3 studie ( Zie NCT01212991 ) , chemotherapie - naïeve patiënten met mCRPC werden gerandomiseerd 1:1 ingedeeld in een groep die tot 160 mg per dag enzalutamide of een placebo kregen toegediend. Algehele overleving (OS) en progressievrije tijd (RPFS) waren beide primaire einddoelen en geanalyseerd bij een intent-to-treat populatie.
Resultaten:
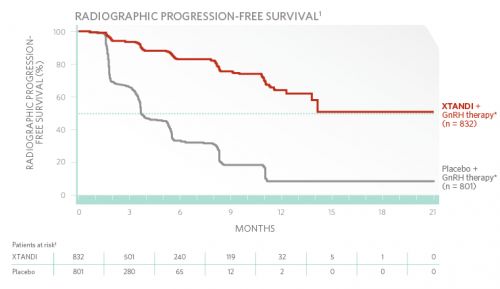
Een totaal van 1.717 mannen werden gerandomiseerd ingedeeld (1715 mannen daarvan zijn daadwerkelijk behandeld behandeld ) tussen september 2010 en september 2012. De tussentijdse analyse bij 539 sterfgevallen toonden een statistisch significant voordeel boven placebo van enzalutamide met een vermindering van 30 % in het risico op overlijden ( OS : HR 0.70 , 95% CI : 0,59-0,83 , p < 0,0001) en tot 81 % vermindering van het risico van radiografische vastgestelde progressie of overlijden ( RPFS : 00:19 HR , 95% CI : 0:15-00:23 , P < 0,0001) .
Op het moment van de analyse - studieduur tot dat moment - is 28 % van de patiënten uit de enzalutamide groep en 35 % van de placebo patiënten overleden. Geschatte mediane overleving (OS) zal ca. 32.4 maanden zijn in de enzalutamide groep ( 95% CI , 31.5 - bovengrens nog niet bereikt [ NYR ] ) versus 30,2 maanden (95 % CI , 28 - bovengrens nog niet bereikt (NYR) ) in de placebogroep. Voor de mediane progressie vrije tijd (RPFS) blijkt de bovengrens in de enzalutamide groep nog niet bereikt ( 95% CI : 13,8 - bovengrens nog niet bereikt - (NYR) )
versus 3,9 maanden ( 95%-BI : 3,7-5,4 ) in de placebogroep. In beide groepen overleed 1 patiënt aan een acute gebeurtenis. Beide patiënten hadden een geschiedenis van epilepsie.
The Independent Data Monitoring Committee overweegt aan de hand van een baten - risicoverhouding om een behandeling met enzalutamide te bevorderen en mannen uit de placebogroep te laten stoppen met de studie en een overstap aan te bieden naar enzalutamide. Secundaire eindpunten en veiligheids analyse zullen worden gepresenteerd.
Enzalutamide werd goed verdragen. 6 % van de patiënten in beide groepen stopten voortijdig de studie vanwege bijwerkingen. Er waren meer graad 3+ bijwerkingen met enzalutamide versus placebo ( 43 % versus 37 % ) De meest voorkomende bijwerkingen waren vermoeidheid ( 36 % vs 26% ) , constipatie ( 22 % vs 17% ) , rugpijn ( 27 % versus 22 % ) en gewrichtspijn ( 20 % vs 16 % ). De mediane tijd tot zich een ongewenste voorval voordeed was 17,1 maanden voor mannen uit de enzalutamide groep en 5,4 maanden voor mannen uit de placebogroep.
Conclusies:
Behandeling met enzalutamide verbetert statistisch significant algehele overleving (OS) en progressievrije tijd (RPFS) bij mannen met chemotherapie - naïeve uitgezaaide prostaatkanker (mCRPC)
De studie werd uitgevoerd in veel verschillende landen waaronder België, maar niet in Nederland, zie hier het originele abstract zoals dat werd gepresenteerd op het Genitourirany Symposium 2014
Treatment with enzalutamide significantly improves OS and rPFS in men with chemotherapy-naive mCRPC
Source: 2014 Genitourinary Cancers Symposium
Enzalutamide in men with chemotherapy-naive metastatic prostate cancer (mCRPC): Results of phase III PREVAIL study
Author(s): Tomasz M. Beer, Andrew J. Armstrong, Cora N. Sternberg, Celestia S. Higano, Peter Iversen, Yohann Loriot, Dana E. Rathkopf, Suman Bhattacharya, Joan Carles, Johann S. De Bono, Christopher P. Evans, Anthony M. Joshua, Choung-Soo Kim, Go Kimura, Paul N. Mainwaring, Harry H. Mansbach, Kurt Miller, Sarah B. Noonberg, Peter M. Venner, Bertrand Tombal; Oregon Health & Science University-Knight Cancer Institute, Portland, OR; Duke Cancer Institute and the Duke Prostate Center, Division of Medical Oncology and Urology, Duke University, Durham, NC; San Camillo and Forlanini Hospital, Rome, Italy; University of Washington/Seattle Cancer Care Alliance, Seattle, WA; Department of Urology, Rigshospitalet, University of Copenhagen, Copenhagen, Denmark; Department of Medical Oncology, Institut Gustave Roussy, Villejuif, France; Memorial Sloan-Kettering Cancer Center, New York, NY; Medivation, Inc., San Francisco, CA; Vall d'Hebron University Hospital, Barcelona, Spain; The Royal Marsden NHS Foundation Trust and The Institute of Cancer Research, Sutton, United Kingdom; UC Davis Comprehensive Cancer Center, Davis, CA; Princess Margaret Cancer Centre, Toronto, ON, Canada; Asan Medical Center, Seoul, South Korea; Nippon Medical School Hospital, Tokyo, Japan; Icon Cancer Care, South Brisbane, Australia; Charité-Universitätsmedizin Berlin, Berlin, Germany; Department of Oncology, University of Alberta, Edmonton, AB, Canada; Cliniques Universitaires Saint-Luc, Brussels, Belgium
Background: Enzalutamide, an orally administered androgen receptor inhibitor, improved overall survival (OS) in men with mCRPC who had received prior docetaxel therapy (Scher et al, NEJM 367:13, 2012). This study examined whether enzalutamide could prolong OS and radiographic progression-free survival (rPFS) in asymptomatic or mildly symptomatic chemotherapy-naive men with mCRPC.
Methods: In this randomized, double-blind, placebo-controlled, multinational phase 3 study (NCT01212991), chemotherapy-naive patients with mCRPC were stratified by site and randomized 1:1 to enzalutamide 160 mg/day or placebo. OS and rPFS were co-primary endpoints and analyzed for the intent-to-treat population. Planned sample size was 1,680 with 765 deaths to achieve 80% power to detect a target OS hazard ratio (HR) of 0.815 with a type I error rate of 0.049 and a single interim analysis at 516 (67%) deaths. The co-primary endpoint of rPFS had sufficient power to detect a target HR of 0.57 and a type I error rate of 0.001 with a minimum of 410 events.
Results: A total of 1,717 men were randomized (1,715 treated) between September 2010 and September 2012. The interim analysis at 539 deaths showed a statistically significant benefit of enzalutamide over placebo with a 30% reduction in risk of death (OS: HR 0.70; 95% CI: 0.59-0.83; P< 0.0001) and an 81% reduction in risk of radiographic progression or death (rPFS: HR 0.19; 95% CI: 0.15-0.23; P< 0.0001). At the time of the analysis, 28% of enzalutamide patients and 35% of placebo patients had died. Estimated median OS was 32.4 months (mo) (95% CI, 31.5–upper limit not yet reached ) in the enzalutamide arm vs 30.2 mo (95% CI, 28–upper limit NYR) in the placebo arm. Median rPFS was NYR (95% CI: 13.8–upper limit NYR) in the enzalutamide arm vs 3.9 mo (95% CI: 3.7-5.4) in the placebo arm. Seizure events were reported in two patients. The Independent Data Monitoring Committee considered the benefit-risk ratio to favor enzalutamide and recommended stopping the study and crossing placebo patients to enzalutamide. Secondary endpoints and safety analysis will be presented.
Conclusions: Treatment with enzalutamide significantly improves OS and rPFS in men with chemotherapy-naive mCRPC. Clinical trial information: NCT01212991.
Our results show that, in addition to improving overall survival, enzalutamide improves wellbeing and everyday functioning of patients with metastatic castration-resistant prostate cancer
doi:10.1016/S1470-2045(14)70303-1
Effect of enzalutamide on time to first skeletal-related event, pain, and quality of life in men with castration-resistant prostate cancer: results from the randomised, phase 3 AFFIRM trial
Summary
Background
Methods
Findings
Interpretation
Funding
Gerelateerde artikelen
- enzalutamide plus leuprolide - leuproreline (hormoontherapie) geeft langere ziektevrije tijd bij prostaatkankerpatienten met stijgende PSA waarden na operatie of bestraling
- Pembrolizumab plus olaparib geeft betere respons en ziekteprogressievrije overleving bij patiënten met eerder behandelde uitgezaaide prostaatkanker in vergelijking met abirateron of enzalutamide maar niet statistisch significant copy 1
- Behandeling met enzalutamide verminderde het risico op progressie van prostaatkanker met 46 procent in vergelijking met patienten in een wait-and-see beleid
- Seizure Rates in Enzalutamide-Treated Men With Metastatic Castration-Resistant Prostate Cancer and Risk of SeizureThe UPWARD Study
- Enzalutamide voorkomt met 71 procent uitzaaiingen bij patienten met hormoonresistente niet uitgezaaide prostaatkanker en oplopende PSA
- Enzalutamide is ook superieur aan bicalutamide - casodex bij prostaatkankerpatienten. Ziektevrije tijd stijgt mediaan van 5,8 naar 15,7 maanden. PSA stijging 2,8 maanden versus nog niet bereikt na 20 maanden
- Enzalutamide - XTANDI verhoogt algehele overleving met 30 procent bij hormoonresistente mannen met uitgezaaide prostaatkanker in vergelijking met placebo en progressie vrije tijd werd minimaal verlengd van 5,4 maanden naar 17,1 maanden
- MDV3100 en abiraterone lijken succesvolle medicijnen te kunnen zijn voor prostaatkankerpatienten waarbij de hormoontherapie niet meer werkt. Abiraterone is inmiddels goedgekeurd als officieel medicijn door FDA
- Enzalutamide - Xtandi bij prostaatkanker, een overzicht van publicaties






Plaats een reactie ...
1 Reactie op "Enzalutamide - XTANDI verhoogt algehele overleving met 30 procent bij hormoonresistente mannen met uitgezaaide prostaatkanker in vergelijking met placebo en progressie vrije tijd werd minimaal verlengd van 5,4 maanden naar 17,1 maanden"