Aan dit artikel is vele uren gewerkt. Opzoeken, vertalen, op de website plaatsen enz. Als u ons wilt ondersteunen dan kan dat via een al of niet anonieme donatie. Elk bedrag is welkom hoe klein ook. Klik hier als u ons wilt helpen kanker-actueel online te houden. Wij zijn een ANBI organisatie en dus is uw donatie in principe aftrekbaar voor de belasting.
15 februari 2015: Bron: Dixon JM, Turnbull AK, Fan C, et al: In-depth genomic analysis of ER+ breast cancers during development of endocrine resistance. 2014 San Antonio Breast Cancer Symposium. Abstract S1-05
Een test met een vier-genen-model - mRNA op 4 sleutel mutaties (Seriële sampling) kan binnen 14 dagen nauwkeurig voorspellen of patiënten met borstkanker wel of niet resistent zijn of worden voor een hormoonbehandeling, in deze studie met letrozole - femara. Maar zal waarschijnlijk gelden voor elke vorm van hormoonbehandeling gezien de mechanismes die hieronder liggen.
Wanneer voor aanvang van de hormoontherapie met letrozole - femara de mRNA waarde van IL6ST en een mRNA waarde van NGFRAP werden gemeten en na 14 dagen behandelen met letrozole - femara de mRNA waarden van MCM4 en ASPM, bleken de uitkomsten van deze vier mRNA's samen voorspellend of patiënten wel of niet resistent zouden worden voor hormoontherapie met letrozole - femara. Zelfs na drie jaar gebruik voorspelden deze vier waarden de uitkomsten.
Deze studie werd gepresenteerd op het San Antonio Breast Cancer Symposium 2014 door een onderzoeksteam onder leiding van Michael Dixon, MD, van het Western General Hospital in Edinburgh. Zij stellen dat een vier-genen RNA (mRNA) profiel de responskans - of de hormoonbehandeling wel of niet aanslaat - met een hoge mate van nauwkeurigheid - 83% tot 100% kan voorspellen.
Belangrijkste conclusies van dit onderzoek:
Gebaseerd op wat de onderzoekers waar hebben genomen met de seriële biopsieën en het moleculaire profiel, gaven zij deze belangrijkste conclusies:
- Moleculaire subtypes veranderen al naar gelang de reactie op de behandeling: nonresponders, dus patiënten die niet goed reageren op letrozole - femara hebben meer kans op een luminale B status bij de start van de behandeling of aan het eind van de behandeling hebben zij een luminale B-status ontwikkeld;
- responders, dus patiënten die goed reageerden op letrole - femara hebben meer kans om bij de start een status te hebben van luminaal A of hun status verandert in tijdens de duur van de behandeling in een luminale A. status.
- Responders, dus patiënten die goed reageeerden op letrole - femara tonen een verlies / verdwijnen van genetische mutaties tijdens de behandelingsperiode.
- Patiënten die nieuwe mutaties ontwikkelen reageren niet meer; Deze veranderingen suggereren dat tijdens de behandeling klonale selectie plaatsvindt.
- Een baseline analyse geeft onvoldoende inforamtie of patiënten wel of niet op een hormoonbehandeling - endocriene behandeling zullen reageren. Daarvoor is een seriële biopsie noodzakelijk.
- Een vier-gen-model kan de reactie op letrozol - femara met grote nauwkeurigheid voorspellen.
Studieopzet:
Mutaties in bepaalde genen hebben eerder aangetoond dat resistentie tegen aromataseremmers en bepaalde moleculaire subtypes, vooral waarden van luminale B-HER2-verrijkte, gerelateerd zijn aan een voorspelling van een slechte prognose. Om de resultaten voor patiënten die resistent zijn of worden tegen hormonale behandelingen te verbeteren, dachten wij dat het nuttig zou zijn om de belangrijkste mutaties te identificeren en hoe deze zich ontwikkelen binnen moleculaire subtypes. De dynamische profilering van dezelfde tumor, bij aanvang en gedurende de neoadjuvante hormonale behandeling, zou een unieke kans zijn om belangrijke genomische veranderingen te identificeren, aldus Dr. Dixon bij de presentatie van zijn studie.
Dr. Dixon en zijn team evalueerden in deze studie postmenopauzale vrouwen met oestrogeenreceptor positieve tumoren die behandeld werden met neoadjuvante letrozol - femara, waaronder 73 patiënten uit Edinburgh en 44 van het Royal Marsden Hospital in Londen. Vers weefsel werd genomen bij de start en 14 dagen later en weerd gebruikt om een voorspellende test op basis van mRNA-expressie te ontwikkelen. Om de resistentie tegen een hormoonbehandeling te analyseren hebben de onderzoekers 17 patiënten geëvalueerd. Een groep van patiënten die niet goed reageerden op de hormoonbehandeling en waarbij meerdere biopsieën zijn genomen. Bij de start, na 14 dagen en regelmatig gedurende een periode van 6 maanden tot drie jaar.
Seriële sampling betekent dat tumoren konden worden geëvalueerd of deze nog gevoelig waren voor een hormonale behandeling tijdens de hormonale therapie en wat pastte binnen bij de bestaande of verworven resistentie status. Dit geeft een dynamisch beeld van hoe de genetische samenstelling verandert als patiënten resistentie tegen een hormoontherapie ontwikkelen, aldus Dr. Dixon.
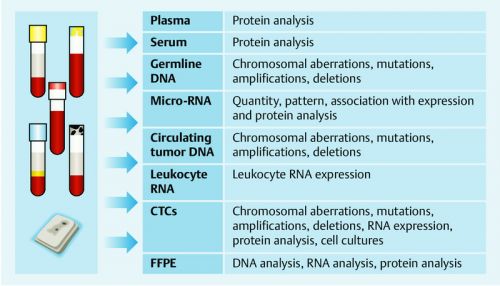
Beeld van op welke manieren een moleculair profiel kan worden vastgesteld uit de Praegnant studie, een andere biomoleculaire studie
Resultaten:
Van de 17 patiënten, reageerden er 13 in eerste instantie wel goed op de behandeling maar gedurende de behandeling ontstond resistentie. Terwijl 4 patiënten goed bleven reageren op de behandeling en geen resistentie ontwikkelden binnen de studieduur. De dynamische klinische respons werd geëvalueerd via driedimensionale ultrasone metingen verkregen tijdens de behandeling. Vers weefsel is genomen vóór de behandeling en bleek daarna resistentie te hebben ontwikkeld. RNA en DNA werden uit de tumor gehaald en normaal DNA werd verkregen uit het bloed of lymfatisch weefsel. De onderzoekers gebruikten UNCeqR, dat RNA en DNA-sequencing integreert, om mutatiedetectie te verbeteren. Deze technologie is bijzonder waardevol als er weinig tumorexpressie is of een lage variatie van allerlei gen-mutaties. Aldus de onderzoekers
De intrinsieke subtype analyse toonde aan dat sommige tumoren met een luminale B expressie bij aanvang van de behandeling waren veranderd in luminale A expressie op het moment van de laatste biopsie, terwijl sommige tumoren van luminale A naar luminale B veranderden en weer terug naar A intraluminaal, afhankelijk van de status van de reactie.
"We zagen dat non-responders veel heterogener waren in hun reacties dan responders, maar er was een tendens om hun luminale B status te behouden, hoewel sommige luminale B veranderen tijdens de behandeling," aldus dr. Dixon.
Er waren 12 patiënten met meerdere monsters en normale DNA, gebaseerd op de UNCeqR analyse. Somatische mutaties waren vergelijkbaar met die gevonden door de Cancer Genome Atlas, hoewel sommige genen vaker dan verwacht waren gemuteerd. Slechts twee genen waren significant op meerdere testen: GATA3 (een transcriptie factor in luminale epitheliale differentiatie) en SMCP (sperma mitochondriën-geassocieerde cysteïnerijke eiwit).
Door het tellen van de mutaties in de tumor en deze te koppelen aan de responsstatus, zagen de onderzoekers dat responders, dus de patiënten die goed reageerden op de hormoonbehandeling, een hoog aantal mutaties hadden bij de start, die dramatisch leek te dalen tijdens de behandeling. Nonresponders, dus patiënten die niet goed reageerden op de hormoonbehandeling, toonden geen duidelijk patroon. Het verlies van mutatie kon niet verklaard worden door de veranderingen in de tumor celeigenschappen. Genetische hot spots van de resistente patiënten toonden aan dat mutaties tijdens de behandeling aanwezig blijven, hoewel hun samenstelling en algehele frequentie in verloop van de tijd veranderen.
Vier-genen model:
Hoewel algemeen aangenomen is dat apoptose belangrijk is na de behandeling blijkt uit de studie dat de apoptotische genen bij de diagnose of de kanker op hormoontherapie met letrozol - femara zal reageren essentieel"
"In principe blijken al na 14 dagen de mRNA niveaus van deze proliferatie genen, de uitkomsten te kunnen voorspellen in de uitkomst. Tenzij letrozole - femara de proliferatie uitschakelt, hoeft een patient geen voordeel te krijgen op de lange termijn van een hormoontherapie. Als tumoren eenmaal de proliferatie uitschakelen dan blijft deze ook uit." Aldus dr. Dixon
"Met de toepassing van mRNA met dit vier-genen profiel, krijgt elke patiënt een indicatie via mRNA of ze zullen reageren of niet reageren op de behandeling."
De test was zeer nauwkeurig, zowel binnen de trainingset van 73 tumoren (96%) en de bevestigingset van 44 tumoren (93%). De toepassing ervan op de studiegroep van 17 patiënten liet een 100% nauwkeurighied zien in het voorspellen van patiënten die een snelle stabiele respons verkregen, zij die eerst stabiele ziekte en daarna progressie verkregen en zij die progressie vertoonden. De test was 83 % nauwkeurig in het voorspellen welke patiënten goed zouden reageren en daarna progressie, de test mistte één van deze zes patiënten.
"Bij onze 17 patiënten konden we na 14 dagen voorspellen welke het goed zouden doen en welke niet. We hadden er maar één verkeerd. Deze test lijkt in de klinische praktijk van nut te kunnen zijn." aldus dr. Dixon.
Dr. Dixon zegt nogmaals dat uit dit onderzoek blijkt dat een diagnosetest bij de start ontoereikend is om een respons op hormoontherapie of enige andere behandeling te voorspellen. "We moeten de status van de tumoren ook analyseren tijdens de behandeling, omdat deze status verandert door de behandeling. "
Disclosure: Dr. Dixon heeft geen potentiële belangenconflicten gemeld.
Reference
1. Dixon JM, Turnbull AK, Fan C, et al: In-depth genomic analysis of ER+ breast cancers during development of endocrine resistance. 2014 San Antonio Breast Cancer Symposium. Abstract S1-05. Presented December 10, 2014.
Hier het abstract van deze studie:
Four-Gene Panel Predicts Response to endocrine therapy with Letrozole - Femara within 14 days
[S1-05] In-depth genomic analysis of ER+ breast cancers during development of endocrine resistance
Dixon JM, Turnbull AK, Fan C, Parker JS, He X, Arthur L, Martinez-Perez C, Renshaw L, Perou C. University of Edinburgh, Edinburgh, United Kingdom; Comprehensive Cancer Centre, Chapel Hill, NC
Background: Aromatase inhibitors (AIs) have an established role in the treatment of estrogen receptor alpha positive (ER+) post-menopausal breast cancer. Response rates are only 50-70% in the neoadjuvant setting and up to 40-50% of all adjuvantly treated patients will eventually relapse. Mutations in certain genes have been previously shown to confer resistance to therapy, and molecular subtype has associations with poor outcome (i.e. LumB and HER2E). In order to improve the outcomes of non-responders or patients who become resistant to endocrine treatment, the identification of key mutations, and their interaction with subtype, is crucial. Dynamic profiling of the same tumour demonstrating de novo or developing resistance after responding to one or more lines of endocrine treatment in the neoadjuvant setting provides a unique opportunity to identify such genomic changes.
Methods: This series is unique in that it includes 17 post-menopausal women with ER+ breast cancer treated with neoadjuvant letrozole. 13 of these patients progressed on treatment or initially responded to treatment and then developed acquired resistance and 4 responded well. Dynamic clinical response was assessed for each patient using periodic 3D ultrasound measurements performed during treatment. Fresh tissue was taken before treatment and when the tumor was resistant to treatment (4 patients had 2 biopsies, 9 patients had 3 and 4 patients had 4 available biopsies taken). RNA and DNA were extracted from tumour and normal DNA obtained from either matched blood or normal lymphatic tissue. In total, 51 tumour samples were available and have completed RNA-Seq, with exome sequencing shortly to be completed.
Results: From the RNA-seq data, the intrinsic subtype distribution was 9 LumA, 7 LumB, and 1 HER2-enriched; when stratified according to response, the "progressors" were 7 LumB, 5 LumA and 1 HER2-enriched, while "responders" were 3 LumA and 1 LumB. When examined in an unsupervised hierarchical clustering analysis along with >800 TCGA Breast tumor samples, 13/17 patients had all of their samples grouped immediately together, suggesting that the overall tumor phenotype was maintained. Interestingly, the most dominant change in gene expression was the observation that there were 5 "progressor" patients where the pre-treatment sample was LumB and all subsequent samples were LumA; we only observed one instance of a patient starting as LumA and changing to a LumB, who was also labelled as a "progressor". Full exome sequencing is underway and these results will be presented.
Conclusion: Genomic analysis of progression suggests that an apparent "subtype shift" appears in a number of patients where a shift to LumA is seen; this apparent change may be reflective of decreased proliferation rates caused by therapy, or the acquisition of a true LumA phenotype. We cannot differentiate between these two hypotheses at this time, but expect that the exome sequencing will help to differentiate between these two hypotheses given the large number of mutations and copy number alterations that can differentiate between LumA vs. LumB.
Gerelateerde artikelen



Plaats een reactie ...
Reageer op "Genentest - mRNA test uitgevoerd op 4 sleutel gen-mutaties voorspelt binnen 14 dagen of patienten met borstkanker wel of niet resistent zullen worden voor letrozole - femara."