Abstract
BACKGROUND
Pembrolizumab has efficacy in programmed death ligand 1 (PD-L1)–positive metastatic or unresectable cervical cancer that has progressed during chemotherapy. We assessed the relative benefit of adding pembrolizumab to chemotherapy with or without bevacizumab.
METHODS
In a double-blind, phase 3 trial, we randomly assigned patients with persistent, recurrent, or metastatic cervical cancer in a 1:1 ratio to receive pembrolizumab (200 mg) or placebo every 3 weeks for up to 35 cycles plus platinum-based chemotherapy and, per investigator discretion, bevacizumab. The dual primary end points were progression-free survival and overall survival, each tested sequentially in patients with a PD-L1 combined positive score of 1 or more, in the intention-to-treat population, and in patients with a PD-L1 combined positive score of 10 or more. The combined positive score is defined as the number of PD-L1–staining cells divided by the total number of viable tumor cells, multiplied by 100. All results are from the protocol-specified first interim analysis.
RESULTS
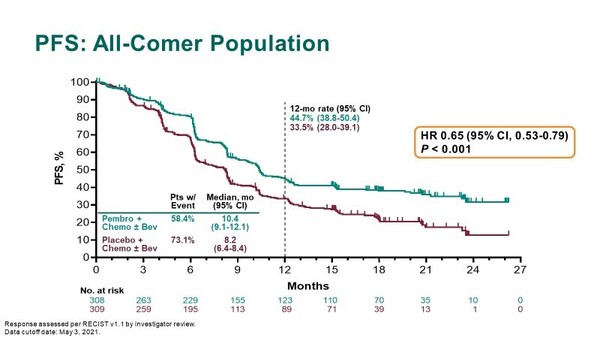
In 548 patients with a PD-L1 combined positive score of 1 or more, median progression-free survival was 10.4 months in the pembrolizumab group and 8.2 months in the placebo group (hazard ratio for disease progression or death, 0.62; 95% confidence interval , 0.50 to 0.77; P<0.001). In 617 patients in the intention-to-treat population, progression-free survival was 10.4 months and 8.2 months, respectively (hazard ratio, 0.65; 95% CI, 0.53 to 0.79; P<0.001). In 317 patients with a PD-L1 combined positive score of 10 or more, progression-free survival was 10.4 months and 8.1 months, respectively (hazard ratio, 0.58; 95% CI, 0.44 to 0.77; P<0.001). Overall survival at 24 months was 53.0% in the pembrolizumab group and 41.7% in the placebo group (hazard ratio for death, 0.64; 95% CI, 0.50 to 0.81; P<0.001), 50.4% and 40.4% (hazard ratio, 0.67; 95% CI, 0.54 to 0.84; P<0.001), and 54.4% and 44.6% (hazard ratio, 0.61; 95% CI, 0.44 to 0.84; P=0.001), respectively. The most common grade 3 to 5 adverse events were anemia (30.3% in the pembrolizumab group and 26.9% in the placebo group) and neutropenia (12.4% and 9.7%, respectively).
CONCLUSIONS
Progression-free and overall survival were significantly longer with pembrolizumab than with placebo among patients with persistent, recurrent, or metastatic cervical cancer who were also receiving chemotherapy with or without bevacizumab. (Funded by Merck Sharp and Dohme; KEYNOTE-826 ClinicalTrials.gov number, NCT03635567. opens in new tab.)



Plaats een reactie ...
Reageer op "Pembrolizumab eerstelijns gegeven plus chemotherapie bij aanhoudende of recidief of uitgezaaide baarmoederhalskanker geeft betere ziektevrije en overall overleving (plus 33 procent) dan placebo"