16 februari 2019: op de website van de Japanse Saisei-Mirai clinics , de enige betrouwbare producent van Gc-Maf, staan een aantal case studies bij individuele patienten met verschillende vormen van kanker. 1 casestudie bij man met longkanker is ook onder ervaringsverhalen te lezen.
Ook de andere case studies zijn zeker de moeite waard eens te lezen, klik op deze pagina.
Officiele studiepublicaties met Gc-Maf staan op deze pagina
Mocht iemand belangstelling hebben dan kunnen we u in contact brengen met een Nederlandse man die de GC-Maf second generation als injectie voor een sterk gereduceerde prijs kan leveren. En u kunt zelf deze injecties toedienen zoals maretakinjecties.
21 februari 2015: als ik in Pubmed zoek op Gc-Maf krijg ik, voor zover ik dat kan beoordelen als leek slechts 1 goed onderbouwde studie naar Gc-MF:
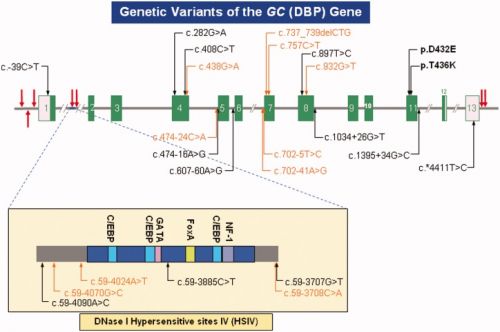
The vitamin D binding protein (DBP) is the major plasma carrier for vitamin D and its metabolites, but it is also an actin scavenger, and is the precursor to the immunomodulatory protein, Gc-MAF: Common variants of the vitamin D binding protein gene and adverse health outcomes
Misschien wel goed dit studierapport eens te lezen en eventueel met uw behandeld arts te bespreken mocht u toch Gc-Maf willen proberen. En lees aub alles hieronder en de artikelen in gerelateerde artikelen.
19 februari 2015: Bron: Antikankerfonds
Ik hoef denk ik aan onderstaande informatie en persbericht niets toe te voegen:
Enkele kernpunten uit het rapport waarom de Engelse autoriteiten het Gc-Maf laboratorium hebben gesloten.
- Er werd vastgesteld dat het bloedplasma dat gebruikt werd om GcMAF aan te maken uitdrukkelijk voorzien was van de volgende vermelding: "Niet toedienen aan mensen of aanwenden voor de productie van geneesmiddelen". Er werd ook bezorgdheid geuit over de steriliteit van het product. In hun reactie concludeerden de bevoegde instanties dat het middel niet volgens de vereiste goede productiepraktijken (GMP) geproduceerd werd.
- Voorts werd bij klanten de indruk gewekt dat ze, door het kopen van dit product, deelnamen aan een klinische studie – er werd hen onder meer gevraagd om de onderneming te informeren over de evolutie van hun ziekte - hoewel er geen spoor terug te vinden is van eender welke geregistreerde klinische studie door de onderneming. De wetenschappers die deelnamen aan deze operatie publiceerden hun zogenaamde resultaten voornamelijk in louter op verkoop gerichte tijdschriften, in zogenaamde “predatory journals”.
- Artikelen die over de resultaten van het onderzoek rapporteerden, werden sindsdien ingetrokken (verwijderd uit de tijdschriften waarin ze aanvankelijk gepubliceerd waren) omwille van onregelmatigheden met betrekking tot de goedkeuring door institutionele beoordelingsraden (IRB's - Institutional Review Boards). Zo ontkenden meerdere vermeende leden van deze IRB's ooit deel uitgemaakt te hebben van de raden in kwestie en wezen ze er bovendien op nooit betrokken te zijn geweest bij enig onderzoek naar GcMAF.
- Voorts werd door dezelfde groep bij de voorstelling van de “resultaten” op internationale conferenties valselijk beweerd dat het onderzoek met de medewerking van een erkende academische instelling en één van hun wetenschappers was gebeurd, terwijl het tegelijk verschillende beproefde beginselen in de oncologie tegensprak.
Zie onder deze grafiek volledige persbericht en eerdere berichten over Gc-Maf
Persbericht: Bevoegde medische autoriteiten in het Verenigd Koninkrijk sluiten GcMAF laboratorium
Het Medicine and Healthcare Products Regulatory Agency (MHRA), de medische toezichthouder in het Verenigd Koninkrijk, heeft een laboratorium gesloten waar GcMAF geproduceerd werd. Het laboratorium in kwestie behoort toe aan Immuno Biotech Ltd, een onderneming die de voorbije jaren agressief promotie voerde voor GcMAF en dit product online verkocht onder de merknaam First Immune. Naast het nu gesloten laboratorium heeft dit bedrijf nog medische centra in Zwitserland en Duitsland, waar heel wat aandoeningen met het product behandeld worden.
Het MHRA voerde een onaangekondigde inspectie uit op een productiesite in Milton, Cambridgeshire, nadat de toezichthouder voor geneesmiddelen in Guernsey een aantal ernstige bedenkingen had geuit met betrekking tot het product.
Er werd vastgesteld dat het bloedplasma dat gebruikt werd om GcMAF aan te maken uitdrukkelijk voorzien was van de volgende vermelding: "Niet toedienen aan mensen of aanwenden voor de productie van geneesmiddelen". Er werd ook bezorgdheid geuit over de steriliteit van het product. In hun reactie concludeerden de bevoegde instanties dat het middel niet volgens de vereiste goede productiepraktijken (GMP) geproduceerd werd. Naar schatting werden er in de gesloten faciliteit zo’n 10.000 flacons van het niet-goedgekeurde product gemaakt.
Voorts werd bij klanten de indruk gewekt dat ze, door het kopen van dit product, deelnamen aan een klinische studie – er werd hen onder meer gevraagd om de onderneming te informeren over de evolutie van hun ziekte - hoewel er geen spoor terug te vinden is van eender welke geregistreerde klinische studie door de onderneming. De wetenschappers die deelnamen aan deze operatie publiceerden hun zogenaamde resultaten voornamelijk in louter op verkoop gerichte tijdschriften, in zogenaamde “predatory journals”.
‘Predatory publishing’ is een exploiterend business model voor open-access publicaties waarbij er aan auteurs enkel een publicatievergoeding wordt gevraagd, zonder in de collegiale toetsings-, redactionele en andere publicatiediensten van legitieme tijdschriften te voorzien. Dergelijke rooftijdschriften publiceren eender welke nonsens van om het even welke auteur, zolang die auteur de gevraagde vergoeding maar betaalt. Dit alles terwijl Immuno Biotech Ltd op haar website naar diezelfde tijdschriften verwijst als zijnde ‘enkele van de meest toonaangevende wetenschappelijke tijdschriften ter wereld’. Voor een leek die niet vertrouwd is met wetenschappelijke publicaties zijn de tijdschriften dan ook bedoeld om legitiem over te komen, terwijl het in feite om boerenbedrog gaat.
De bevoegde instanties roepen patiënten, die GcMAF gebruikt hebben, op om zo snel mogelijk contact op te nemen met hun arts. Hoewel er door gebruikers tot nu toe geen bijwerkingen gemeld werden, werd echter evenmin het bewijs geleverd dat dit product niet gevaarlijk is voor de menselijke gezondheid. De vraag is ook of het überhaupt werkt. Bovendien werd het onderzoek dat aanvankelijk als bewijs werd aangevoerd voor de werkzaamheid van dit product tegen kanker en HIV inmiddels ernstig in twijfel getrokken door de wetenschappelijke gemeenschap die er vandaag van uitgaat dat de gegevens gewoonweg uit de lucht gegrepen zijn. Artikels die over de resultaten van het onderzoek rapporteerden, werden sindsdien ingetrokken (verwijderd uit de tijdschriften waarin ze aanvankelijk gepubliceerd waren) omwille van onregelmatigheden met betrekking tot de goedkeuring door institutionele beoordelingsraden (IRB's - Institutional Review Boards). Zo ontkenden meerdere vermeende leden van deze IRB's ooit deel uitgemaakt te hebben van de raden in kwestie en wezen ze er bovendien op nooit betrokken te zijn geweest bij enig onderzoek naar GcMAF.
Voorts werd door dezelfde groep bij de voorstelling van de “resultaten” op internationale conferenties valselijk beweerd dat het onderzoek met de medewerking van een erkende academische instelling en één van hun wetenschappers was gebeurd, terwijl het tegelijk verschillende beproefde beginselen in de oncologie tegensprak. Dit alles, in combinatie met de agressieve illegale marketing van het product, bracht onze organisatie ertoe om verder onderzoek te verrichten naar het product en wetenschappelijke en overheidsinstanties, alsook patiënten op bovenstaande malafide praktijken te wijzen.
Inmiddels werd ook de invoer van GcMAF verboden door de autoriteiten van Guernsey, terwijl consumenten per brief op de hoogte gebracht worden van het opgelegde verbod. Naar schatting zouden er wereldwijd nog zo'n 10 GcMAF-fabrieken bestaan.
25 juli 2014: Lees aub dit artikel voor u Gc-Maf gaat gebruiken:
26 mei 2012: enkele links en bepaalde informatie in onderstaande artikel is gecorrigeerd en waar nodig aangevuld. Onderaan staat een lange referentielijst van studies gedaan met Gc-Maf. In Nederland zijn ook enkele artsen al een tijdje bezig met Gc-Maf maar tot nu toe gebruiken zij niet de Gc-Maf van Dr. Yamamoto. Zie onze nieuwsbrieven. Er zijn inmiddels wel positieve ontwikkelingen maar zullen u daarvan op de hoogte stellen zodra we die mogen vrijgeven.
Klik hier voor video over hoe Gc-MAF injecties werken.
10 november 2011: afgelopen weken had ik een correspondentie met een orthomoleculaire arts die mij vertelde dat hij met enkele collega's bezig waren met Gc-MAF op basis van nagalase testen. Hij zou mij nog antwoorden over de uitkomsten van experimenten op een congres over Gc-MAF. Ik had hem vantevoren links gestuurd waaruit blijkt dat er nog steeds wel studies gedaan worden naar Gc-MAF.
Ook dr. Yamamoto heeft deze zomer nog gepubliceerd over Gc-Maf.
Maar of de Gc-MAF die in Nederland gebruikt wordt de juiste Gc-MAF is weet ik niet. Dr. Yamamoto heeft het octrooi op het maken van Gc-Maf en niemand anders mag zonder zijn toestemming de Gc-MAF mag gebruiken. Maar het ware weet ik niet hiervan.
19 juni 2010:
Afgelopen tijd krijgen we steeds meer vragen over Gc-Maf. Maar ik moet helaas zeggen dat wij hierop geen antwoord hebben. Wel wordt Gc-Maf aangeboden op internet maar naar onze mening is dit niet echt betrouwbaar. Achter deze website zitten dezelfde mensen van DCA en daar horen we toch ook weinig meer van. En nergens is ook maar enig bewijs geleverd dat de Gc-Maf die op internet wordt aangeboden ook de echte Gc-Maf is. En hoewel deze mensen erg goed weten hoe je op internet de publiciteit kunt verkrijgen is de manier waarop zij Gc-Maf aanbieden naar mijn mening dubieus. Ze schermen met op te zetten studies en wetenschappers en artsen maar in mailtjes aan patienten wordt nergens vermeld wie het protocol van de studie heeft opgezet, welke artsen er bij betrokken zijn en wat er gebeurt met de gegevens die patienten eventueel aanleveren. De patienten moeten wel tekenen dat de aanbieders hun aangeleverde gegevens mogen gebruiken voor promotie van hun activiteiten. Wel handig natuurlijk want dat verkoopt goed. Bovendien moeten de patienten alles zelf betalen wat niet gebruikelijk is bij een studie. En als het waar is dat deze mensen de echte Gc-Maf leveren schenden zij het octrooi dat dr. Yamamoto heeft op Gc-Maf injecties en zijn zij strafbaar.
Het is wel jammer dat dr. Yamamoto zo weinig van zich laat horen want Gc-Maf lijkt toch veelbelovend. Vorig jaar publiceerde Dr. Yamamoto nog een studie met Aidspatienten en als het waar is wat de onderzoekers beweren is dit echt goed nieuws. Achtereenvolgens de studie uit januari 2009 met Aidspatienten en daaronder de informatie over Gc-Maf studies bij kanker enz. Onderaan lijst van referenties van uitgevoerde studies met Gc-Maf.
Immunotherapy of HIV-infected patients with Gc protein-derived macrophage activating factor (GcMAF)
Immunotherapy of HIV-infected patients with Gc protein-derived macrophage activating factor (GcMAF).
Source
Division of Molecular Immunology and Immunotherapy, Socrates Institute for Therapeutic Immunology, Philadelphia, Pennsylvania 19126-3305, USA. nobutoyama@verizon.net
Abstract
Serum Gc protein (known as vitamin D3-binding protein) is the precursor for the principal macrophage activating factor (MAF). The MAF precursor activity of serum Gc protein of HIV-infected patients was lost or reduced because Gc protein is deglycosylated by alpha-N-acetylgalactosaminidase (Nagalase) secreted from HIV-infected cells. Therefore, macrophages of HIV-infected patients having deglycosylated Gc protein cannot be activated, leading to immunosuppression. Since Nagalase is the intrinsic component of the envelope protein gp120, serum Nagalase activity is the sum of enzyme activities carried by both HIV virions and envelope proteins. These Nagalase carriers were already complexed with anti-HIV immunoglobulin G (IgG) but retained Nagalase activity that is required for infectivity. Stepwise treatment of purified Gc protein with immobilized beta-galactosidase and sialidase generated the most potent macrophage activating factor (termed GcMAF), which produces no side effects in humans. Macrophages activated by administration of 100 ng GcMAF develop a large amount of Fc-receptors as well as an enormous variation of receptors that recognize IgG-bound and unbound HIV virions. Since latently HIV-infected cells are unstable and constantly release HIV virions, the activated macrophages rapidly intercept the released HIV virions to prevent reinfection resulting in exhaustion of infected cells. After less than 18 weekly administrations of 100 ng GcMAF for nonanemic patients, they exhibited low serum Nagalase activities equivalent to healthy controls, indicating eradication of HIV-infection, which was also confirmed by no infectious center formation by provirus inducing agent-treated patient PBMCs. No recurrence occurred and their healthy CD + cell counts were maintained for 7 years.
- PMID:
- 19031451
- [PubMed - indexed for MEDLINE]
Wat is er verder bekend over Gc-Maf:
Ene Herman schrijft op ons forum dat hij contact heeft met artsen in Duitsland: Mijn reis voerde mij, in eerste instantie, naar Aken (RWTH), alwaar ik een gesprek heb gevoerd met éen der 'uitvinders' van Gc-MAF, Dokter Olav Gressner. en Denemarken maar dit gaat niet om Gc-MAF injecties maar om Gc-Globulin. Welke ook in Nederlandse academische ziekenhuizen worden gebruikt. Lees het octrooi op Gc-Maf van dr. Yamamoto en zie het verschil
Via internet kun je ook Gc-MAF injecties in druppelvorm c.q. capsules verkrijgen. Verder biedt de Canadese man van de DCA site Gc-Maf injecties aan. Er wordt ook gesuggereerd dat een arts werkzaam in Antwerpen hierbij betrokken zou zijn. Dit is zover wij weten niet waar. De man achter de DCA site lijkt ons iemand die op een handige manier gebruik c.q. misbruik maakt van beloftevolle ontwikkelingen bij kanker. Op mijn vraag aan dr. Yamamoto of hij aan anderen Gc-MAF injecties verstrekt kreeg ik dit antwoord:
Sent: Saturday, June 20, 2009 10:55 AM
Subject: Re: Re: Re: Gc-MAF questions
Dear Mr. Kees Braam,
We never release GcMAF anywhere. Could you find out who is making and distributing GcMAF, illegally? Moreover, GcMAF is a protein factor and cannot be administered via digestive system (you indicated in capsules).
Regards,
Dr. Yamamoto
25 november 2008: het blijkt dat Gc-MAF al tientallen jaren onderzocht wordt en gebruikt bij vormen van immuunziektes. Het Gc-MAF, een vitamine D bindend glyco-protein (een molecule met een glucose - suiker - en eiwit component) werkt 100% effectief in het volledig vernietigen van kankercellen binnen een jaar maximaal en de kanker komt jaren later zelfs niet meer terug als dit wekelijks wordt gegeven al of niet na operatieve ingreep bij verschillende vormen van kanker. Dat blijkt uit een aantal studies (zie abstracten hieronder) uitgevoerd door Japanse onderzoekers bij respectievelijk prostaatkanker, borstkanker en darmkanker.
Maar ook andere studies wijzen uit volgens de Japanse onderzoekers dat Gc-MAF werkt bij zo goed als alle vormen van kanker, zelfs bij bloedkankersoorten als leukemie. De kosten van deze aanpak bedragen gemiddeld $ 150,-- per injectie en gemiddeld heeft iemand zeg 35 wekelijkse inejcties nodig. Daarbij komen dan uiteraard nog wel de kosten van de artsen, ziekenhuisbezoek en het maken van scans enz. Maar lijkt o.i. een betaalbare aanpak, zeker als je bedenkt dat er geen bjkomende kosten zijn voor bestrijden van infecties en
andere bijwerkingen. En de kwaliteit van leven blijkt uitstekend van alle deelnemende kankerpatiënten.
Uit de borstkankerstudie (the January 15 issue of the International Journal of Cancer. [International Journal Cancer.2008 January15; 122(2):461-7] ):
Na 16-22 weken van injecties met Gc-MAF vielen de hoeveelheid NAGALASE enzymen (alpha-N-acetylgalactosaminidase) terug tot het niveau van een gezond mens, welke erop duidt dat de tumoren volledig zijn geëlimineerd, aldus de onderzoekers. De behandeling was volledig succesvol...het werkte in 100% bij de 16 kankerpatiënten uit de studie en er waren geen recidieven noch bijwerkingen over een periode van 4 jaar.
Uit de darmkankerstudie: [Cancer Immunology, Immunotherapy Volume 57, Number 7 / July 2008]:
Gc-MAF therapie vernietigde volledig alle tumorcellen bij 8 darmkankerpatienten die al een operatie hadden ondergaan maar nog steeds tumor activiteit toonden door uitgezaaide kankercellen. Na 32 tot 50 wekelijkse injecties, "toonden alle 8 darmkankerpatienten een gezond niveau van Nagalase enzymen (alpha-N-acetylgalactosaminidase), daarmee aantonend dat de uitzaaiingen ook waren geëlimineerd " zeggen de onderzoekers, een effect dat minimaal 7 jaar duurde aangetoond door Nagalase enzym activiteit en scans.
Uit de prostaatkankerstudie: ( Transl Oncol. 2008 Jul;1(2):65-72)Na 14 tot 25 weken van wekelijkse injecties hadden alle 16 prostaatkankerpatienten het niveau van hun NAGALASE enzymen (alpha-N-acetylgalactosaminidase) terug tot het niveau van een gezond mens, welke erop duidt dat de tumoren volledig zijn geëlimineerd, aldus de onderzoekers. Geen enkele patient kreeg een recidief binnen minimaal 7 jaar.
Achtereenvolgens de abstracten van de drie genoemde studies en daaronder nog enkele studies met Gc-MAF van Nobuto Yamamoto, director of the Division of Cancer Immunology and Molecular Biology, Socrates Institute for Therapeutic Immunology, Philadelphia, Pennsylvania, welke zegt in een recent Amerikaans artikel "dit is waarschijnlijk de meest effectieve macrophage activerende factor welke ooit is ontdekt". Zou het dan toch waar kunnen zijn en een genezing van kanker binnen de mogelijkheden gaan behoren?.
Immunotherapy of metastatic colorectal cancer with vitamin D-binding protein-derived macrophage-activating factor, GcMAF
Immunotherapy of metastatic colorectal cancer with vitamin D-binding protein-derived macrophage-activating factor, GcMAF.
Source
Division of Cancer Immunology and Molecular Immunology, Socrates Institute for Therapeutic Immunology, 1040, 66th Ave, Philadelphia, PA 19126-3305, USA. nobutoyama@verizon.net
Abstract
Serum vitamin D binding protein (Gc protein) is the precursor for the principal macrophage-activating factor (MAF). The MAF precursor activity of serum Gc protein of colorectal cancer patients was lost or reduced because Gc protein is deglycosylated by serum alpha-N-acetylgalactosaminidase (Nagalase) secreted from cancerous cells. Deglycosylated Gc protein cannot be converted to MAF, leading to immunosuppression. Stepwise treatment of purified Gc protein with immobilized beta-galactosidase and sialidase generated the most potent macrophage-activating factor (GcMAF) ever discovered, but it produces no side effect in humans. Macrophages treated with GcMAF (100 microg/ml) develop an enormous variation of receptors and are highly tumoricidal to a variety of cancers indiscriminately. Administration of 100 nanogram (ng)/ human maximally activates systemic macrophages that can kill cancerous cells. Since the half-life of the activated macrophages is approximately 6 days, 100 ng GcMAF was administered weekly to eight nonanemic colorectal cancer patients who had previously received tumor-resection but still carried significant amounts of metastatic tumor cells. As GcMAF therapy progressed, the MAF precursor activities of all patients increased and conversely their serum Nagalase activities decreased. Since serum Nagalase is proportional to tumor burden, serum Nagalase activity was used as a prognostic index for time course analysis of GcMAF therapy. After 32-50 weekly administrations of 100 ng GcMAF, all colorectal cancer patients exhibited healthy control levels of the serum Nagalase activity, indicating eradication of metastatic tumor cells. During 7 years after the completion of GcMAF therapy, their serum Nagalase activity did not increase, indicating no recurrence of cancer, which was also supported by the annual CT scans of these patients.
- PMID:
- 18058096
- [PubMed - indexed for MEDLINE]
Immunotherapy for Prostate Cancer with Gc Protein-Derived Macrophage-Activating Factor, GcMAF
Immunotherapy for Prostate Cancer with Gc Protein-Derived Macrophage-Activating Factor, GcMAF.
Source
Division of Cancer Immunology and Molecular Biology, Socrates Institute for Therapeutic Immunology, Philadelphia, PA 19126-3305, USA.
Abstract
Serum Gc protein (known as vitamin D(3)-binding protein) is the precursor for the principal macrophage-activating factor (MAF). The MAF precursor activity of serum Gc protein of prostate cancer patients was lost or reduced because Gc protein was deglycosylated by serum alpha-N-acetylgalactosaminidase (Nagalase) secreted from cancerous cells. Therefore, macrophages of prostate cancer patients having deglycosylated Gc protein cannot be activated, leading to immunosuppression. Stepwise treatment of purified Gc protein with immobilized beta-galactosidase and sialidase generated the most potent MAF (termed GcMAF) ever discovered, which produces no adverse effect in humans. Macrophages activated by GcMAF develop a considerable variation of receptors that recognize the abnormality in malignant cell surface and are highly tumoricidal. Sixteen nonanemic prostate cancer patients received weekly administration of 100 ng of GcMAF. As the MAF precursor activity increased, their serum Nagalase activity decreased. Because serum Nagalase activity is proportional to tumor burden, the entire time course analysis for GcMAF therapy was monitored by measuring the serum Nagalase activity. After 14 to 25 weekly administrations of GcMAF (100 ng/week), all 16 patients had very low serum Nagalase levels equivalent to those of healthy control values, indicating that these patients are tumor-free. No recurrence occurred for 7 years.
- PMID:
- 18633461
-
- PMCID:
- PMC2510818
Immunotherapy of metastatic breast cancer patients with vitamin D-binding protein-derived macrophage activating factor (GcMAF).
Immunotherapy of metastatic breast cancer patients with vitamin D-binding protein-derived macrophage activating factor (GcMAF).
Source
Division of Cancer Immunology and Molecular Biology, Socrates Institute for Therapeutic Immunology, Philadelphia, PA 19126-3305, USA. nobutoyama@verizon.net
Abstract
Serum vitamin D3-binding protein (Gc protein) is the precursor for the principal macrophage activating factor (MAF). The MAF precursor activity of serum Gc protein of breast cancer patients was lost or reduced because Gc protein was deglycosylated by serum alpha-N-acetylgalactosaminidase (Nagalase) secreted from cancerous cells. Patient serum Nagalase activity is proportional to tumor burden. The deglycosylated Gc protein cannot be converted to MAF, resulting in no macrophage activation and immunosuppression. Stepwise incubation of purified Gc protein with immobilized beta-galactosidase and sialidase generated probably the most potent macrophage activating factor (termed GcMAF) ever discovered, which produces no adverse effect in humans. Macrophages treated in vitro with GcMAF (100 pg/ml) are highly tumoricidal to mammary adenocarcinomas. Efficacy of GcMAF for treatment of metastatic breast cancer was investigated with 16 nonanemic patients who received weekly administration of GcMAF (100 ng). As GcMAF therapy progresses, the MAF precursor activity of patient Gc protein increased with a concomitant decrease in serum Nagalase. Because of proportionality of serum Nagalase activity to tumor burden, the time course progress of GcMAF therapy was assessed by serum Nagalase activity as a prognostic index. These patients had the initial Nagalase activities ranging from 2.32 to 6.28 nmole/min/mg protein. After about 16-22 administrations (approximately 3.5-5 months) of GcMAF, these patients had insignificantly low serum enzyme levels equivalent to healthy control enzyme levels, ranging from 0.38 to 0.63 nmole/min/mg protein, indicating eradication of the tumors. This therapeutic procedure resulted in no recurrence for more than 4 years.
Copyright 2007 Wiley-Liss, Inc.
- PMID:
- 17935130
- [PubMed - indexed for MEDLINE]
Nog enkele citaten uit artikelen en studies die dr. Yamamoto heeft gedaan:
Division of Cancer Immunology and Molecular Immunology, Socrates Institute for Therapeutic Immunology, 1040, 66th Ave, Philadelphia, PA 19126-3305, USA. nobutoyama@verizon.net
Serum vitamin D binding protein (Gc protein) is the precursor for the principal macrophage-activating factor (MAF). The MAF precursor activity of serum Gc protein of colorectal cancer patients was lost or reduced because Gc protein is deglycosylated by serum alpha N-acetylgalactosaminidase (Nagalase) secreted from cancerous cells. Deglycosylated Gc protein cannot be converted to MAF, leading to immunosuppression. Stepwise treatment of purified Gc protein with immobilized beta-galactosidase and sialidase generated the most potent macrophage-activating factor (GcMAF) ever discovered, but it produces no side effect in humans. Macrophages treated with GcMAF (100 microg/ml) develop an enormous variation of receptors and are highly tumoricidal to a variety of cancers indiscriminately. Administration of 100 nanogram (ng)/ human maximally activates systemic macrophages that can kill cancerous cells. Since the half-life of the activated macrophages is approximately 6 days, 100 ng GcMAF was administered weekly to eight nonanemic colorectal cancer patients who had previously received tumor-resection but still carried significant amounts of metastatic tumor cells. As GcMAF therapy progressed, the MAF precursor activities of all patients increased and conversely their serum Nagalase activities decreased.
Since serum Nagalase is proportional to tumor burden, serum Nagalase activity was used as a prognostic index for time course analysis of GcMAF therapy. After 32-50 weekly administrations of 100 ng GcMAF, all colorectal cancer patients exhibited healthy control levels of the serum Nagalase activity, indicating eradication of metastatic tumor cells. During 7 years after the completion of GcMAF therapy, their serum Nagalase activity did not increase, indicating no recurrence of cancer, which was also supported by the annual CT scans of these patients.
PMID: 18058096 [PubMed - indexed for MEDLINE]Gc-MAF treatment for cancer has been agonizingly slow to develop. Dr. Yamamoto first described this immuno-therapy in 1993. [The Journal of Immunology, 1993 151 (5); 2794-2802]
In a similar animal experiment published in 2003, researchers in Germany, Japan and the United States collaborated to successfully demonstrate that after they had injected macrophage activating factor (Gc-MAF) into tumor-bearing mice, it totally eradicated tumors. [Neoplasia 2003 January; 5(1): 32–40]
In 1997 Dr. Yamamoto injected GcMAF protein into tumor-bearing mice, with the same startling results. A single enzyme injection doubled the survival of these mice and just four enzyme injections increased survival by 6-fold. [Cancer Research 1997 Jun 1; 57(11):2187-92]
In 1996 Dr. Yamamoto reported that all 52 cancer patients he had studied carried elevated blood plasma levels of the immune inactivating alpha-N-acetylgalactosaminidase enzyme (Nagalase), whereas healthy humans had very low levels of this enzyme. [Cancer Research 1996 Jun 15; 56(12):2827-31]
In the early 1990s, Dr. Yamamoto first described how the human immune system is disengaged by enzymes secreted from cancer cells, even filing a patent on the proposed therapy. [US Patent 5326749, July 1994; Cancer Research 1996 June 15; 56: 2827-31]
References
Plaats een reactie ...
3 Reacties op "Gc-MAF een vitamine D verbindend eiwit werkt ook effectief (100% genezing) bij HIV positieve patienten naast vormen van kanker. Originele Gc-Maf nu beschikbaar in Nederland"
Gerelateerde artikelen
- Gc-Maf studie publicatie bij borstkanker van dr. Yamamoto officieel teruggetrokken wegens onvoldoende bewijs en tegenstrijdige bevindingen. Via internet verkrijgbare Gc-Maf en Nagalasetest blijken geen enkel bewijs te leveren van werkzaamheid
- Gc-MAF een vitamine D verbindend eiwit werkt ook effectief (100% genezing) bij HIV positieve patienten naast vormen van kanker. Originele Gc-Maf nu beschikbaar in Nederland
- Gc-Maf van dr. Yamamoto nu in Nederland beschikbaar



Vriendelijke groet, Bert Albronda
Vriendelijke groet, Bert Albronda