Mocht u kanker-actueel de moeite waard vinden en ons willen ondersteunen om kanker-actueel online te houden dan kunt u ons machtigen voor een periodieke donatie via donaties: https://kanker-actueel.nl/NL/donaties.html of doneer al of niet anoniem op - rekeningnummer NL79 RABO 0372931138 t.n.v. Stichting Gezondheid Actueel in Amersfoort. Onze IBANcode is NL79 RABO 0372 9311 38
Elk bedrag is welkom. En we zijn een ANBI instelling dus uw donatie of gift is in principe aftrekbaar voor de belasting.
En als donateur kunt u ook korting krijgen bij verschillende bedrijven:
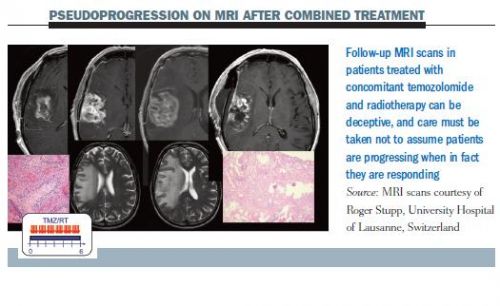
15 april 2016: Afgelopen week werd een interessante studie gepubliceerd die aantoont dat via een MRI en vooral hoe zo'n MRI dan te lezen en te interpreteren pseudoprogressie bij gebruik van temodal - temozolomide bij hersentumoren kan worden aangetoond.
In this review, we discuss the recent applications of advanced MR imaging such as diffusion-weighted and perfusion-weighted imaging in the evaluation of treatment response in high-grade glioma patients and highlight their potential role in differentiating pseudoprogression from true progression.
Is van groot belang denk ik voor mensen die temodal krijgen. Klik op de volgende PDF voor het volledige studierapport: Recent Application of Advanced MR Imaging to Predict Pseudoprogression in High-grade Glioma Patients
https://www.jstage.jst.go.jp/article/mrms/15/2/15_rev.2015-0053/_pdf
18 oktober 2009: Uit een retropostpectieve studie blijkt dat Temozolomide - Temodal bij bijna de helft van de patienten die Temodal krijgen op de eerste scan na toediening een pseudoprogressie laat zien. Dit betekent dat er beter niet gestopt kan worden met de Temodal maar gewoon moet worden doorgegaan aldus de onderzoekers van deze studie. (zie op deze pagina onder chemo bij hersentumoren het volledige studieabstract van deze studie). Dan blijkt de mediane overleving ca. 5 maanden langer te bedragen.
16 maart 2009: Bron: 1: Lancet Oncol. 2009 Mar 6. [Epub ahead of print]![]()
Combinatiebehandeling van Temozolomide = Temodal en radiotherapie - bestraling bij hersentumoren Glioblastomen, na operatie geeft meer 2, 3, 4, en 5 jaars overlevingen ten opzichte van alleen radiotherapie - bestraling. Temozolomide = Temodal had echter geen effect op het wel of niet ontstaan van een recidief ten opzichte van alleen bestraling. De onderzoekers merken op dat Temozolomide = Temodal de tumor blijkbaar minder agressief maakt maar stopt niet het proces van groei van de tumor. Onder het abstract een artikel uit Medscape over genoemde studie. Opvallend ook dat in het abstract met geen woord gesproken wordt over het feit dat Temozolomide = Temodal voor de echte overall overleving, dus kankervrij worden, geen enkel verschil maakt terwijl Medscape dat impliciet wel noemt.
"Many patients with glioblastoma survive for several years," they add. "However, true long-term survival and cure are not possible." Zij schrijven dus dat een hersentumor waarbij niet alles weggehaald kan worden of een recidief ontstaat nooit te genezen is. Ook blijkt Temozolomide = Temodal geen effect te hebben op het wel of niet ontstaan van een recidief ten opzichte van alleen bestraling na operatie.
Toch wel opmerkelijk dat dr. Robert Gorter met zijn aanpak van hyperthermie en dendritische celtherapie en infusen met immuunstimulerende middelen wel succes heeft. Zie de video's van Teun van Vliet en van Dirk van den Boogaard die beiden vanuit een totaal ongeneeslijke situatie volledig klinisch kankervrij werden door aanpak bij dr. Gorter. Ook kennen we een jonge vrouw met een recidief en inoperabele hersentumor in 2005 die via arts-bioloog drs. E. Valstar een aantal speciale voedingsupplementen krijgt en nu al vier jaar klinisch kankervrij is, ook door het strikt volgen van een gezonde leefwijze. En niets wijst op een recidief. Terwijl zij als onbehandelbaar en ongeneeslijk werd gekwalificeerd in 2005.
Uit abstract van fase III studie met Temodal:
Resultaten: Tussen Aug 17, 2000, en Maart 22, 2002, 573 patienten werden teogelaten tot de behandeling. 278 (97%) van de 286 patienten in de radiotherapie groep zonder Temodal en 254 (89%) van de 287 patienten in de combinatiegroep bestraling en Temodal stierf binnen de 5 jaar studiefollow-up. Overall overleving was 27.2% (95% CI 22.2-32.5) na 2 jaar, 16.0% (12.0-20.6) na 3 jaar, 12.1% (8.5-16.4) na 4 jaar, en 9.8% (6.4-14.0) na 5 jaar met temozolomide, versus 10.9% (7.6-14.8), 4.4% (2.4-7.2), 3.0% (1.4-5.7), and 1.9% (0.6-4.4) met radiotherapie alleen (hazard ratio 0.6, 95% CI 0.5-0.7; p<0.0001). Een positeif effect werd in de combinatiegroep bereikt in alle klinische prognostische subgroepen, inclusief patienten in de leeftijd van 60-70 jaar. Methylation van de MGMT promoter was de sterkste voorspeller voor een positieve uitkomst voor de temozolomide chemotherapie.
Hieronder het abstract van de fase III studie en daaronder het artikel uit Medscape over deze studie.
Effects of radiotherapy with concomitant and adjuvant temozolomide versus radiotherapy alone on survival in glioblastoma in a randomised phase III study: 5-year analysis of the EORTC-NCIC trial.
Centre Hospitalier Universitaire Vaudois and University of Lausanne, Lausanne, Switzerland.
BACKGROUND: In 2004, a randomised phase III trial by the European Organisation for Research and Treatment of Cancer (EORTC) and National Cancer Institute of Canada Clinical Trials Group (NCIC) reported improved median and 2-year survival for patients with glioblastoma treated with concomitant and adjuvant temozolomide and radiotherapy. We report the final results with a median follow-up of more than 5 years.
METHODS: Adult patients with newly diagnosed glioblastoma were randomly assigned to receive either standard radiotherapy or identical radiotherapy with concomitant temozolomide followed by up to six cycles of adjuvant temozolomide. The methylation status of the methyl-guanine methyl transferase gene, MGMT, was determined retrospectively from the tumour tissue of 206 patients. The primary endpoint was overall survival. Analyses were by intention to treat. This trial is registered with Clinicaltrials.gov, number NCT00006353.
FINDINGS: Between Aug 17, 2000, and March 22, 2002, 573 patients were assigned to treatment. 278 (97%) of 286 patients in the radiotherapy alone group and 254 (89%) of 287 in the combined-treatment group died during 5 years of follow-up. Overall survival was 27.2% (95% CI 22.2-32.5) at 2 years, 16.0% (12.0-20.6) at 3 years, 12.1% (8.5-16.4) at 4 years, and 9.8% (6.4-14.0) at 5 years with temozolomide, versus 10.9% (7.6-14.8), 4.4% (2.4-7.2), 3.0% (1.4-5.7), and 1.9% (0.6-4.4) with radiotherapy alone (hazard ratio 0.6, 95% CI 0.5-0.7; p<0.0001). A benefit of combined therapy was recorded in all clinical prognostic subgroups, including patients aged 60-70 years. Methylation of the MGMT promoter was the strongest predictor for outcome and benefit from temozolomide chemotherapy.
INTERPRETATION: Benefits of adjuvant temozolomide with radiotherapy lasted throughout 5 years of follow-up. A few patients in favourable prognostic categories survive longer than 5 years. MGMT methylation status identifies patients most likely to benefit from the addition of temozolomide.
FUNDING: EORTC, NCIC, Nélia and Amadeo Barletta Foundation, Schering-Plough.
PMID: 19269895 [PubMed - as supplied by publisher]
Bron: Medscape Medical News 2009. © 2009 Medscape
March 12, 2009 — The final results from a phase 3 study, with a median follow-up of more than 5 years, have confirmed the survival advantage of adding temozolomide (Temodar, Schering-Plough) to radiotherapy in adult patients with newly diagnosed glioblastoma.
"A benefit of combined therapy was recorded in all clinical prognostic subgroups, including patients 60 to 70 years," according to a report published online March 9 in the Lancet Oncology.
In addition, the long-term results confirm earlier findings that patients with a tumor containing a methylated promoter for the gene encoding 0-6-methylguanine-DNA methyltransferase were more likely to benefit from the addition of temozolomide. This has also been seen with temozolomide in other brain tumors, such as gliomatosis cerebri, as reported recently by Medscape Oncology.
"We have identified the first marker in brain tumors that allows selection of patients who will benefit most from treatment with temozolomide and radiotherapy," say the researchers, headed by Roger Stupp, MD, from the University of Lausanne, in Switzerland.
Survival Improved, But Did Not Plateau
When results from this trial were first reported in 2004, with a median follow-up of just over 2 years, they were described as "the most markedly positive" results in patients with glioblastoma in 20 years, and were predicted to change clinical practice (Nat Clin Pract Oncol. 2005;2:334-335).
Until that time, postoperative radiotherapy had been the standard treatment for glioblastoma. Since then, combined treatment with radiotherapy and temozolomide, given both concomitantly and after the radiotherapy, has become the standard.
The new results show that survival advantage was maintained over the long term. Overall survival was significantly improved at 2, 3, 4, and 5 years in patients who were treated with temozolomide plus radiotherapy, compared with those treated with radiotherapy alone.
Overall Survival With Combined Therapy (Temozolomide Plus Radiotherapy) or With Radiotherapy Alone
| Overall Survival | Combined Therapy | Radiotherapy Alone |
| 2 years, % | 27.2 | 10.9 |
| 3 years, % | 16.0 | 4.4 |
| 4 years, % | 12.1 | 3.0 |
| 5 years, % | 9.8 | 1.9 |
Despite this improvement, however, most of the patients died during the 5-year follow up — 254 of 287 patients (89%) in the combined-therapy group and 278 of 286 patients (97%) in the radiotherapy-alone group.
"Survival does not plateau, and combined treatment is unlikely to be curative for many patients," the researchers write.
They add that an analysis of recurrence showed no difference between initial radiotherapy alone and the combined treatment, which supports the hypothesis that combined therapy might effectively reduce tumor bulk and aggressiveness, but does not modify the disease course.
"Many patients with glioblastoma survive for several years," they add. "However, true long-term survival and cure are not possible."
Further research is needed and ongoing trials are investigating the addition of other treatments to the combination of temozolomide plus radiotherapy, the researchers note. These include studies with the angiogenesis inhibitor bevacizumab, inhibitors of integrins, such as cilengitide, and inhibitors of epidermal growth-factor receptor, such as erlotinib.
"Until better treatments are available, radiotherapy with concomitant and adjuvant chemotherapy is the current standard of care," Dr. Stupp and colleagues conclude.
The study was funded by Schering-Plough, manufacturer of temozolomide, and by the European Organisation for Research and Treatment of Cancer and the National Cancer Institute of Canada Clinical Trials Group. Dr. Stupp and several coauthors report having received research funding and honoraria from Schering-Plough and Merck AG.
Lancet Oncol. Published online before print March 9 2009. Abstract
Gerelateerde artikelen
- Temodal - temozolomide naast radiotherapie geeft geen enkel voordeel bij een hersentumor type astrocytoom graad 3 met geen IDH1/2 mutatie. Ook bij patienten met gemethyleerde MGMT-promotor was er geen effectiviteit
- Temodal - temozolomide naast bestraling maar ook solo vergroot 5-jaars overleving met 15 tot 20 procent bij laaggradige hersentumoren - anaplastische glioma
- Chemo bij hersentumoren: Temozolomide - Temodal samen met radiotherapie - bestraling geeft significant meer 2, 3, 4, en 5-jaars overlevingen t.o.v. alleen bestraling maar heeft geen effect op wel of geen recidief t.o.v. alleen bestraling. Ook kan Temodal
- Temozolomide - Temodal bij hersentumoren - Glioblastomen Multiforme geeft vaak een pseudo progressie te zien op eerste scan en wanneer doorgegaan met Temodal geeft dan 5x langere mediane levensduur. Studie toont nu aan hoe dit verschil te onderscheiden
- Temozolomide - temodal geeft gemiddeld slechts 2 maanden verschil in overlevingstijd voor hersentumoren - Glioblastoom - in vergelijking met periode voordat temodal werd ingezet
- Temodal - temozolomide verbetert zelfstandig functioneren en verlengt levensduur met enkele weken bij lichamelijk verzwakte bejaarden met een nieuw gediagnosteerde hersentumor, GMB.
- Chemo bij hersentumoren: wanneer temodal - temozolomide continue wordt gegeven levert dat de langste ziektevrije tijd op, al blijft de uiteindelijke overlevingstijd kort. Artikel geplaatst 3 april 2010
- Chemo bij hersentumoren: Enzastaurine, een specifiek gericht medicijn voor hersentumoren faalt bij hersentumoren Glioblastoom in fase III studie. Artikel geplaatst 27 februari 2010
- Chemo bij hersentumoren: Gliadel (R) Wafer, een ingeplante vorm van 'timerelease' chemo na operatie zorgt voor 27% meer kans op overleving bij een kwaadaardige hersentumor. Artikel geplaatst september 2002
- Chemo bij hersentumoren: Gliadel® wafer een chemo met ook carmustine (BCNU) toegediend tijdens operatie van kwaadaardige hersentumoren geeft een significant betere 2 en 3 jaars overleving (29%) blijkt uit gerandomiseerde fase III studie.
- Gliadel® wafer een chemo met ook carmustine (BCNU) toegediend tijdens operatie van kwaadaardige hersentumoren geeft een significant betere 2 en 3 jaars overleving (29%) blijkt uit gerandomiseerde fase III studie. Nieuwe studie meldt ernstige bijwerkingen
- Temozolomide - Temodal gebruik bij hersentumoren wordt aanbevolen na goede studieresultaten.
- Kinderen met medulloblastomen - hersentumoren - zouden na operatie alleen met chemo moeten worden behandeld en pas na recidief met ook bestraling aldus advies na studieresultaten over cognitieve beschadigingen na bestraling.
- Velcade - Bortezomib lijkt een veelbelovend middel als bestrijding van hersentumoren, glioblastoom multiforme
- Temozolomide - Temodal geeft kleine remming van recidief van Glioblastomen blijkt uit fase II studie
- Combinatiebehandeling van irinitocan en Avastin bij hersentumoren (Glioma's), aldus een fase II studie.
- Temozolomide - Temodal krijgt ook Europese toestemming om te gebruiken via infuus. Lees hier ook over de bijwerkingen en mogelijke gevaren van Temodal
- Chemo bij hersentumoren: een overzicht van recente ontwikkelingen en artikelen, met name over Temodal - Temolzolomide



Plaats een reactie ...
Reageer op "Chemo bij hersentumoren: Temozolomide - Temodal samen met radiotherapie - bestraling geeft significant meer 2, 3, 4, en 5-jaars overlevingen t.o.v. alleen bestraling maar heeft geen effect op wel of geen recidief t.o.v. alleen bestraling. Ook kan Temodal"