Helpt u ons aan 500 donateurs om kanker-actueel online te kunnen houden?
4 april 2018: zie ook dit artikel:
6 november 2016: Lees ook dit artikel:
en dit artikel:
Lees ook dit artikel:
Wanneer en hoe PARP-remmers zoals olaparib te gebruiken als medicijn bij eierstokkanker?
Parpremmers zoals olaparib zouden veel eerder ingezet moeten worden als medicijn bij eierstokkankerpatiënten, maar ook bij andere vormen van kanker, vooral die met een BRCA mutatie, want elke chemokuur vermindert risico op aanslaan van de behandeling. En er is ook wel bewijs dat niet persè een BRCA 1-2 positieve DNA mutatie aanwezig moet zijn om een behandeling aan te laten slaan. Dr. Elizabeth M. Swisher stelt dit bij de presentatie van studies met de PARP-remmer olaparib voor eierstokkankerpatiënten.
Ik heb het verslag van de persconferentie en vragen aan dr. Swisher dat de ASCO Post publiceerde in z’n geheel proberen te vertalen.
“PARP-remmers bieden een veelbelovend alternatief voor gerichte therapie bij eierstokkanker en geven duidelijk een therapeutisch voordeel voor patiënten met een BRCA-mutatie, maar er blijven genoeg vragen over wanneer het beste moment is om deze medicijnen te geven aan patiënten met eierstokkanker. Ook de kosteneffectiviteit van deze behandeling staat ter discussie,” aldus Elizabeth M. Swisher , MD, van de Universiteit van Washington in Seattle, op een bijeenkomst bij de Society of Gynecologic Oncology Annual Meeting on Women's Cancer in Chicago. Aanvullend gegeven kunnen parp-remmers (poly (ADP-ribose) polymerase (PARP) enzymen) in combinatie met andere gerichte therapieën, zoals met chemotherapie, deze behandelingen nog veel effectiever maken." Aldus dr. Swisher
Dr. Swisher haar reactie volgde op presentaties van studies met olaparib (Lynparza) monotherapie bij patiënten met gevorderde recidief van eierstokkanker en het gebruik van olaparib als onderhoudstherapie. Olaparib werd door de Amerikaanse Food and Drug Administration goedgekeurd in 2014 voor de behandeling van patiënten met gevorderde eierstokkanker en positieve BRCA1 / 2 mutaties die drie of meer voorafgaande kuren van chemotherapie hebben ontvangen.
In Europa is olaparib goedgekeurd als onderhoudsbehandeling voor patiënten met een recidief na een op platinum basis gebaseerde chemokuur in zowel DNA bepaalde BRCA mutaties (erfelijk bepaald) of somatische BRCA-mutaties (afwijkingen die ontstaan tijdens de ziekte bv door behandelingen) ," "Dus de indicaties verschillen nogal", aldus dr. Swisher.
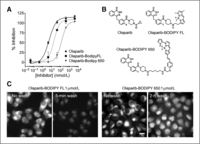
Studieresultaten:
Een samengevoegde analyse van zes fase I en II studies met olaparib vonden dat patiënten met een recidief van eierstokkanker en DNA afwijking van BRCA1 / 2 mutaties een profijt hadden van ongeveer 8 maanden durende progressievrije tijd en die duurzame respons was niet minder bij patiënten die eerder drie of meer chemokuren hadden ontvangen. De analyse bevestigde de werkzaamheid en veiligheid van olaparib in deze patiëntenpopulatie van een voltooide monotherapie, met inbegrip van de subgroep van patiënten die minstens drie voorafgaande chemokuren hadden gekregen", aldus Ursula A. Matulonis, MD, van het Dana-Farber Cancer Center, Boston, als reactie op de gepresenteerde resultaten.
Bij de patiënten met meetbare ziekte gaf RECIST (Response Beoordelingscriteria in solide tumoren) v1.1 criteria, dat de demografie en baseline kenmerken vergelijkbaar waren voor de totale populatie van 273 patiënten en de 205 patiënten die ten minste drie eerdere chemokuren hadden gekregen. Alle patiënten kregen tweemaal daags olaparib 400 mg capsules.
Reactie verminderd wel door meerdere chemokuren:
“De totale respons was 36% versus 31% voor de zwaarder behandelde patiënten”, zegt Dr. Matulonis . “Er was een geleidelijke afname van de totale respons in relatie tot het aantal chemokurren.”
"Zoals Dr Matulonis heeft aangetoond, neemt de respons af met een toenemend aantal eerdere therapieën," zegt ook Dr. Swisher . "Dus waarom zouden we willen wachten tot de vierde kuur om patiënten met een BRCA mutatie te behandelen?" zegt ook Dr Swisher, ” veel artsen zijn waarschijnlijk herhaaldelijk geconfronteerd met situaties waarin zij denken dat patiënten zouden kunnen profiteren van olaparib maar mogen olaparib nog niet geven omdat de patiënten eerst nog een paar chemokuren moeten volgen tot deze ook falen. '
“Daarnaast”, zei ze, "weten we allemaal dat later in het ziekteverloop, gastro-intestinale klachten vaker voorkomen en een oraal geneesmiddel wordt niet altijd meer getolereerd . Zo kunnen we de mogelijkheid verliezen om deze patiënten te behandelen met deze geneesmiddelen. "
In de samengevoegde analyse kwamen graad 3 bijwerkingen voor bij 50% van de totale patiëntengroep en bij 54% van de subgroep. Ernstige bijwerkingen traden op bij 30% van alle patiënten en bij 34% van de subgroepen. Alle acht de patiënten (3%) die overleden tijdens de studie aan ernstige bijwerkingen hadden minstens drie chemokuren vooraf gehad. Maar geen van deze bijwerkingen (sepsis, intestinale perforatie, breuk hechtdraad , acute leukemie, beroerte, chronische obstructieve longziekte en longembolie) werden beschouwd als oorzakelijk verband door het gebruik van olaparib. De meest voorkomende bijwerkingen van alle gradaties door olaparib waren misselijkheid (65%), vermoeidheid (61%), en braken (39%).
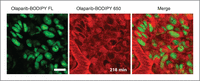
Onderhoudtherapie met PARP-remmers:
"Onderhoudstherapie voor eierstokkanker is erg spannend geweest," zegt Dr. Swisher. Bedrijven hebben met vier PARP-remmers zwaar geïnvesteerd in studies met PARP-remmers als onderhoudsbehandeling. Naast olaparib, worden veliparib, rucaparib en niraparib als onderhoudsbehandeling in fase III studies voor eierstokkanker onderzocht.
In deze studies, krijgt de patiënt ofwel een PARP-remmer of een placebo. De tijd tot de volgende progressie van de ziekte zich aandient is doel van deze studies." zei Dr Swisher. In een eerdere studie met die opzet bleek dat een onderhoudsbehandeling met olaparib progressievrije overleving bij patiënten met gevorderde eierstokkanker en BRCA-mutaties significant werd verlengd.
Studies met Olaparib concentreren zich alleen op patiënten met BRCA-mutaties, ofwel als DNA mutatie ofwel als somatische mutatie, terwijl de andere drie medicijnen studies hebben lopen die open zijn, zowel in de primaire en recidiverende stadia voor patiënten met het type hooggradige sereuze eierstokkanker of endometriose kanker, en patiënten die BRCA-mutaties hebben, "aldus Dr Swisher. "Voorspelbare factoren / kenmerken van een respons (en resistentie) anders dan BRCA-mutaties zijn nodig ," aldus Dr. Swisher.
Wat patiënten werkelijk willen?
"Patiënten willen verlenging van de levensduur en ook tijd van leven zonder een behandeling, vooral wanneer dat de behandeling gepaard gaat met ernstige bijwerkingen," zegt Dr Swisher. “Zo zou een onderhoudsbehandeling kunnen worden gebruikt om de tijd uit te stellen tot een latere chemotherapie weer nodig is. Dat is een zeer belangrijk einddoel," zegt Dr Swisher. "Ik denk dat we het er allemaal over eens zijn dat het uitstellen van een chemokuur een belangrijke klinische stimulans is."
Echter, er is enige bezorgdheid dat het gebruik van een PARP-remmer als onderhoudstherapie zou kunnen leiden tot chemoresistentie en enkele studies zijn op zoek naar de effecten van een tweede daaropvolgende chemotherapie. "Die tijd naar die tweede daaropvolgende chemokuur kunnen reflecteren of een onderhoudsbehandeling met een PARP-remmer resistentie tegen chemo genereert ," aldus Dr Swisher.
Bijvoorbeeld, als een patiënt die een PARP-remmer gebruikt toch progressie van de ziekte krijgt en daarop vervolgens een chemokuur krijgt, maar dan blijkt dat de chemokuur niet zo goed werkt, zal de patiënt een andere chemokuur eerder nodig hebben dan wanneer de patiënt na een PARP remmer een recideif krijgt en toch ook een goede respons laat zien op een daaropvolgende chemokuur. In nog een ander scenario, zou het starten van een PARP-remmer bij progressie van de ziekte uiteindelijk uitmonden in langere tijd tot zich progressie voordoet en langere tijd tot de volgende chemokuur nodig is, kunnen leiden tot een rendabelere aanpak.”, aldus dr. Swisher
Er blijven cruciale vragen over:
"Zoals: is het beter om een PARP-remmer te gebruiken in onderhoudsbehandleing of zelfs ten tijde van een terugval? Als we het gebruiken als onderhoudsbehandeling doen we dat dan in eerste lijns of als tweede lijns bij een recidief? "Dit zijn twee cruciale vragen die we nog moeten beantwoorden over het inzetten van PARP-remmers bij eierstokkanker," zegt Dr Swisher.
Andere vragen houden verband kosteneffectiviteit, bepalen van een synergistische combinatie van PARP remmers met biologische middelen of chemokuren, het ontwikkelen van testen die het beste BRCA-achtige vormen van kanker bepalen en die mogelijk zouden kunnen reageren op PARP-remmers, en het combineren PARP-remmers met andere therapieën die zich op DNA herstel richten. Dit zou de potentie van PARP-remmers uit kunnen breiden tot vormen van kanker die gedreven worden door homologe recombinaties of vormen van kanker waarbij een DNA-reparatie nodig is," zei Dr Swisher.
"We weten dat eierstokkanker die gedreven zijn door homologe recombinaties niet gevoelig zijn voor PARP-remmers," zegt Dr. Swisher . "Zelfs BRCA-mutaties eierstokkanker uiteindelijk resistentie tegen PARP remmers ontwikkelen, en veel daarvan is door middel van herstel van DNA en toename van homologe recombinatie. Zodat nieuwe geneesmiddelen die een homologe recombinatie remmen kan worden gecombineerd met PARP-remmers. "In dat scenario, kan een middel dat homologe recombinatie remt gebruikt om eierstokkanker bedreven in homologe recombinatie deficiënte in homologe recombinatie, die het mogelijk maken een PARP-remmer te maken synthetisch dodelijk voor die kanker. "Er is zeker een veel potentieel om PARP-remmers nog effectiever te maken," besluit Dr. Swisher .
Hierna is er nog discussie over de kosten van de nieuwe medicijnen enz. maar dat heb ik niet vertaald en kunt u lezen in dit artikel: PARP Inhibitors Have ‘Clear Benefit’ for Patients With Ovarian Cancer and BRCA Mutations, but When and at What Cost? op de website van ASCO Post.
Disclosure: Dr. Matulonis heeft financiering van het onderzoek van AstraZeneca ontvangen, is lid van adviesraden voor ImmunoGen en Genentech, en is lid van het sprekers bureau voor AstraZeneca. Drs. Swisher en Smith hebben geen potentiële belangenconflicten.
Abstracten van de genoemde studies met olaparib: 2 bij baarmoederhalskanker en baarmoederkanker, 4 studies bij eierstokkanker en 1 studie bij borstkanker zijn allemaal vermeld in deze reviewstudie in de referentielijst die onderaan dit artikel staat: Major clinical research advances in gynecologic cancer in 2015.
Table 1
| Site of cancer | Topic | Reference |
|---|---|---|
| Uterine cervix | 1. Treatment of advanced or metastatic cervical cancer | |
| 1) Antiangiogenic targeted therapy: bevacizumab (GOG 240) and cediranib (CIRCCa trial) | [1,2] | |
| 2) Immunotherapy: HPV-tumor-infiltrating lymphocytes and Z-100 | [3,4] | |
| 2. HPV test as a primary screening tool of cervical cancer | ||
| 1) FDA approval of Cobas HPV test | [7] | |
| 2) Efficacy of HPV-based screening test: follow-up results of 4 RCTs in Europe | [12,13,14,15,16] | |
| 3) Meta-analysis of self-collection versus clinician collection | [17] | |
| Uterine corpus | 3. Update of adjuvant radiation therapy in endometrial cancer | |
| 1) A phase III study of early stage endometrial cancer with high-intermediate risk factors (GOG 249) | [19] | |
| 2) ASTRO new guidelines | [7] | |
| 4. Uterine power morcellation: a hot potato in minimally invasive gynecologic surgery | [24,25,28,29,30] | |
| Ovary | 5. Update of PARP inhibitors in ovarian cancer | |
| 1) Olaparib maintenance therapy in PSROC | [33,34] | |
| 2) Olaparib combined with chemotherapy in PSROC | [35] | |
| 3) Combination of cediranib and olaparib in PSROC | [36] | |
| 4) Other PARP inhibitors | [32] | |
| 6. Pazopanib maintenance therapy for an effective survival prolongation in advanced ovarian cancer | [42] | |
| 7. Tailored treatment according to the molecular subtype of high-grade serous ovarian cancer | [45,46] | |
| 8. Opportunistic bilateral salpingectomy for ovarian cancer risk-reducing procedure in the general population | [52,54] | |
| Female breast | 9. Unveiled efficacy of ovarian suppression in premenopausal breast cancer | |
| 1) Adjuvant ovarian suppression in premenopausal early breast cancer | [56] | |
| 2) Adjuvant aromatase inhibitor exemestane with ovarian suppression in premenopausal early breast cancer | [57] |
ASTRO, American Society for Radiation Oncology; FDA, the US Food and Drug Administration; GOG, Gynecologic Oncology Group; HPV, human papillomavirus; PARP, poly (ADP-ribose) polymerase; PSROC, platinum-sensitive recurrent ovarian cancer; RCT, randomized controlled trial.
Hier het abstract van deze studie:
Following the FDA approval of bevacizumab as the first targeted agent for ovarian cancer, olaparib has emerged as a promising secondary targeted agent for the treatment of ovarian cancer, particularly for platinum-sensitive recurrent ovarian cancer in daily practice. Promising phase III study results for PARP inhibitors including olaparib are highly anticipated in the near future.
Major clinical research advances in gynecologic cancer in 2014
Abstract
In 2014, 9 topics were selected as major advances in clinical research for gynecologic oncology: 2 each in cervical and corpus cancer, 4 in ovarian cancer, and 1 in breast cancer. For cervical cancer, several therapeutic agents showed viable antitumor clinical response in recurrent and metastatic disease: bevacizumab, cediranib, and immunotherapies including human papillomavirus (HPV)-tumor infiltrating lymphocytes and Z-100. The HPV test received FDA approval as the primary screening tool of cervical cancer in women aged 25 and older, based on the results of the ATHENA trial, which suggested that the HPV test was a more sensitive and efficient strategy for cervical cancer screening than methods based solely on cytology. For corpus cancers, results of a phase III Gynecologic Oncology Group (GOG) 249 study of early-stage endometrial cancer with high-intermediate risk factors are followed by the controversial topic of uterine power morcellation in minimally invasive gynecologic surgery. Promising results of phase II studies regarding the effectiveness of olaparib in various ovarian cancer settings are summarized. After a brief review of results from a phase III study on pazopanib maintenance therapy in advanced ovarian cancer, 2 outstanding 2014 ASCO presentations cover the topic of using molecular subtypes in predicting response to bevacizumab. A review of the use of opportunistic bilateral salpingectomy as an ovarian cancer preventive strategy in the general population is presented. Two remarkable studies that discussed the effectiveness of adjuvant ovarian suppression in premenopausal early breast cancer have been selected as the last topics covered in this review.
Referentielijst
Gerelateerde artikelen
- Parpremmers bij eierstokkanker: een meta analyse biedt een overzicht welke vorm van eierstokkanker gevoelig blijkt en welke niet. En hoe resistentie optreedt bespreekt een andere studie
- Parpremmers olaparib (Lynparza®) of niraparib (Zejula®) voor eierstokkanker en borstkanker worden gedeeltelijk uit basisverzekering gehaald door Zorginstituut Nederland copy 1
- Olaparib herhalen bij patienten met gevorderde eierstokkanker die al eerder olaparib en chemo hebben gehad blijkt alsnog effectief in vergelijking met placebo
- Niraparib als eerstelijns onderhoudsbehandeling bij patiënten met nieuw gediagnosticeerde gevorderde operabele eierstokkanker verdubbelt op 5 jaar ziektevrije overleving in vergelijking met placebo
- Niraparib - Zejula als onderhoudsbehandeling bij gevorderde eierstokkanker geeft een veel langere progressievrije overleving bij zowel patiënten met BRCA-gemuteerde eierstokkanker als bij niet BRCA-gemuteerd
- niraparib plus bevacizumab (Avastin) zonder chemo of gegeven in chemovrije periode verdubbelt bij eierstokkanker ziektevrije tijd en ziektevrije overleving steeg met 26 procent (79 vs 53 procent)
- Niraparib geeft zeer goede resultaten bij recidief van gevorderde eierstokkanker die eerder gevoelig bleek voor op platinum gebaseerde chemo copy 1
- Parpremmers Olaparib en niraparib gegeven als onderhoudsbehandeling bij gevorderde chemo gevoelige eierstokkanker heeft geen negatief effect op kwaliteit van leven en geeft wel betere overall overleving
- PARP remmers zoals olaparib zouden in vroeger stadium van eierstokkanker en andere vormen van kanker met BRCA mutaties moeten worden ingezet want teveel chemokuren verminderen kans op aanslaan van de behandeling, stellen oncologen n.a.v. diverse studies
- Talazoparib, een PARP remmer, wordt in veel studies bij veel verschillende vormen van kanker en in combinatie met andere medicijnen onderzocht en geeft veelbelovende resultaten copy 1
- Olaparib plus Bevacizumab als eerstelijns onderhoudsbehandeling voor eierstokkanker geeft betere progressievrije ziekte dan placebo ongeacht BRCA status.
- Olaparib als onderhoudsbehandeling voor BRCA 1/2 uitgezaaide platinum gevoelige eierstokkanker geeft 70 procent minder kans op overlijden in vergelijking met placebo
- Olaparib, een PARP remmer, verlengt ziektevrije en overall overleving in vergelijking met placebo bij eierstokkanker met BRCA 1 en 2
- Olaparib plus cedinarib lijkt doorbraak bij controle van vergevorderde eierstokkanker en verdubbelt progressievrije overleving van 9,2 maanden naar 17,7 maanden
- Parpremmer niraparib naast chemo en daarna als onderhoudsbehandeling verdubbelt mediane overall overleving in vergelijking met placebo
- Parpremmer Veliparib naast chemo gevolgd door veliparib alleen als onderhoudsbehandeling geeft betere overall overleving voor patienten met eierstokkanker stadium III en IV.
- Patienten met gevorderde eierstokkanker met een PARP-7 mutatie / expressie blijken veel betere mediane overall overleving te hebben (45 vs 16 maanden) dan zonder PARP-7 mutatie / expressie. copy 1
- Parpremmer rucaparib verdubbelt ziektevrije overleving (5 vs 11 en 13 maanden) bij chemo gevoelige eierstokkanker. Ook bij patienten zonder BRCA mutatie is rucaparib effectief
- PARP remmers zoals olaparib zouden in vroeger stadium van eierstokkanker en andere vormen van kanker met BRCA mutaties moeten worden ingezet
- BRCA - erfelijkheid: Combinatie van sapacitabine en seliciclib geeft een hoopvol therapeutisch effect bij zwaar voorbehandelde kankerpatienten met solide tumoren met onderliggende afwijkende erfelijke BCRA gen mutaties. copy 1
- PARP remmers zoals olaparib, niraparib en rucaparib zijn effectief zowel met als zonder BRCA mutaties, een overzicht



 4
4
Plaats een reactie ...
Reageer op "PARP remmers zoals olaparib zouden in vroeger stadium van eierstokkanker en andere vormen van kanker met BRCA mutaties moeten worden ingezet"