Wanneer patiënten met de ziekte van Kahler - multiple myeloma die nog geen behandeling hebben gehad naast de standaard behandeling van lenalidomide en dexamethason ook vanaf het begin van de behandeling bortezomib erbij krijgen dan blijkt de progressievrije ziektetijd langer te duren (plus 12 maanden) en de overall overleving sterk te verbeteren (minimaal 15 maanden maar eindpunt was nog niet bereikt voor bortezomib) in vergelijking met aanpak zonder bortezomib. Dit blijkt uit een update van een fase III studie SWOG S0777 .
SWOG S0777, een gerandomiseerde fase III-studie, vergeleek bortezomib, lenalidomide en dexamethason (VRd) met lenalidomide en dexamethason (Rd).
Deze bijgewerkte analyse omvat 460 patiënten die evalueerbaar zijn voor overlevingseindpunten: 225 in aanmerking komende en analyseerbare patiënten werden gerandomiseerd naar Rd en 235 naar VRd. De inductie van 6 maanden bestond uit zes cycli van 28 dagen met Rd en acht cycli van 21 dagen van VRd gevolgd door Rd-onderhoud voor alle patiënten.
- De mediane follow-up is 84 maanden.
- De mediane PFS is 41 maanden voor VRd en 29 maanden voor Rd: gestratificeerde hazard ratio (96% Wald-betrouwbaarheidsinterval) was 0,742 (0,594; 0,928) en eenzijdig gestratificeerde log-rank P-waarde 0,003.
- De mediane OS voor VRd is nog steeds niet bereikt met een mediane OS voor Rd van 69 maanden: gestratificeerde hazard ratio (96% Wald-betrouwbaarheidsinterval) was 0,709 (0,543; 0,926) en de gestratificeerde tweezijdige P-waarde was 0,0114.
- Zowel PFS als OS waren verbeterd met VRd versus Rd-correctie voor leeftijd (P-waarden: 0,013 ; 0,033 )). De mediane duur van Rd-onderhoud was 17,1 maanden.
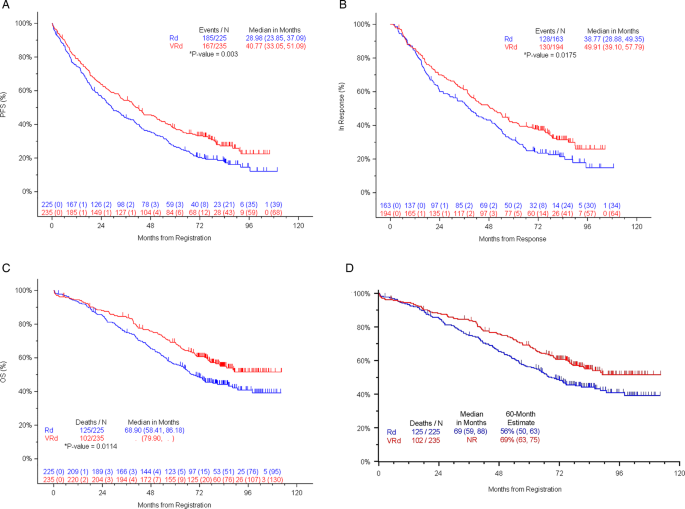
Conclusie: De toevoeging van bortezomib aan lenalidomide dexamethason voor inductietherapie resulteert in een statistisch significante en klinisch relevante verbetering van de PFS en een betere OS. VRd blijft een passende zorgstandaard vertegenwoordigen, ongeacht de leeftijd.
Het studierapport is gratis in te zien. Klik op de titel van het abstract.
- Article
- Open Access
- Published:
Longer term follow-up of the randomized phase III trial SWOG S0777: bortezomib, lenalidomide and dexamethasone vs. lenalidomide and dexamethasone in patients (Pts) with previously untreated multiple myeloma without an intent for immediate autologous stem cell transplant (ASCT)
Blood Cancer Journal volume 10, Article number: 53 (2020)
Abstract
SWOG S0777, a randomized phase III trial, compared bortezomib, lenalidomide and dexamethasone (VRd) with lenalidomide and dexamethasone (Rd). This updated analysis includes 460 patients evaluable for survival endpoints: 225 eligible and analyzable patients were randomized to Rd and 235 to VRd. The 6-month induction was six 28-day cycles of Rd and eight 21-day cycles of VRd followed by Rd maintenance for all patients. Median follow up is 84 months. Median PFS is 41 months for VRd and 29 months for Rd: stratified hazard ratio (96% Wald Confidence Interval) was 0.742 (0.594, 0.928) and one-sided stratified log-rank P-value 0.003. Median OS for VRd is still not reached with median OS for Rd being 69 months: stratified hazard ratio (96% Wald Confidence Interval) was 0.709 (0.543, 0.926) and stratified two-sided P-value was 0.0114. Both PFS and OS were improved with VRd versus Rd adjusting for age (P-values: 0.013 ; 0.033 )). Median duration of Rd maintenance was 17.1 months. The addition of bortezomib to lenalidomide dexamethasone for induction therapy results in a statistically significant and clinically meaningful improvement in PFS as well as better OS. VRd continues to represent an appropriate standard of care irrespective of age.
References
- 1.
Anonymous Revlimid® (lenalidomide) [prescribing information]. (Celgene Corporation, Summit, 2017).
- 2.
Lu, G. et al. The myeloma drug lenalidomide promotes the cereblon-dependent destruction of Ikaros proteins. Science 343, 305–309 (2014).
- 3.
Lopez-Girona, A. et al. Cereblon is a direct protein target for immunomodulatory and antiproliferative activities of lenalidomide and pomalidomide. Leukemia 26, 2326–2335 (2012).
- 4.
Richardson, P. et al. Lenalidomide in multiple myeloma: an evidence-based review of its role in therapy. Core Evid. 4, 215–245 (2010).
- 5.
Anonymous Velcade [package insert]. (Millenium Pharmaceuticals, Cambridge, MA, 2017).
- 6.
Hideshima, T. et al. Molecular mechanisms mediating antimyeloma activity of proteasome inhibitor PS-341. Blood 101, 1530–1534 (2003).
- 7.
Kotla, V. et al. Mechanism of action of lenalidomide in hematological malignancies. J. Hematol. Oncol. 2, 36 (2009).
- 8.
Mitsiades, N. et al. Apoptotic signaling induced by immunomodulatory thalidomide analogs in human multiple myeloma cells: therapeutic implications. Blood 99, 4525–4530 (2002).
- 9.
Hideshima, T. et al. The proteasome inhibitor PS-341 inhibits growth, induces apoptosis, and overcomes drug resistance in human multiple myeloma cells. Cancer Res. 61, 3071–3076 (2001).
- 10.
Rajkumar, S. V. et al. Combination therapy with lenalidomide plus dexamethasone (Rev/Dex) for newly diagnosed myeloma. Blood 106, 4050–4053 (2005).
- 11.
Dimopoulos, M. A. et al. Long-term follow-up on overall survival from the MM-009 and MM-010 phase III trials of lenalidomide plus dexamethasone in patients with relapsed or refractory multiple myeloma. Leukemia 23, 2147–2152 (2009).
- 12.
Dimopoulos, M. A. et al. Retrospective matched-pairs analysis of bortezomib plus dexamethasone versus bortezomib monotherapy in relapsed multiple myeloma. Haematologica 100, 100–106 (2015).
- 13.
Richardson, P. G. et al. A phase 2 trial of lenalidomide, bortezomib, and dexamethasone in patients with relapsed and relapsed/refractory myeloma. Blood 123, 1461–1469 (2014).
- 14.
Richardson, P. G. et al. Lenalidomide, bortezomib, and dexamethasone combination therapy in patients with newly diagnosed multiple myeloma. Blood 116, 679–686 (2010).
- 15.
Durie, B. G. et al. Bortezomib with lenalidomide and dexamethasone versus lenalidomide and dexamethasone alone in patients with newly diagnosed myeloma without intent for immediate autologous stem-cell transplant (SWOG S0777): a randomised, open-label, phase 3 trial. Lancet 389, 519–527 (2017).
- 16.
Durie, B. G. et al. Myeloma management guidelines: a consensus report from the Scientific Advisors of the International Myeloma Foundation. Hemtatol. J. 4, 379–398 (2003).
- 17.
Oken, M. M. et al. Toxicity and response criteria of the Eastern Cooperative Oncology Group. Am. J. Clin. Oncol. 5, 649–655 (1982).
- 18.
Griepp, P. R. et al. International staging system for multiple myeloma. J. Clin. Oncol. 23, 3412–3420 (2005).
- 19.
Durie, B. G. et al. International uniform response criteria for multiple myeloma. Leukemia 20, 1467–1473 (2006).
- 20.
Peto, R. et al. Design and analysis of randomised clinical trials requiring prolonged observation of each patient: I. Introduction and design. Br. J. Cancer 34, 585–612 (1976).
- 21.
Haybittle, J. L. Repeated assessment of results in clinical trials of cancer treatment. Br. J. Radiol. 44, 793–797 (1971).
- 22.
Mantel, N. Evaluation of survival data and two new rank order statistics arising in its consideration. Cancer Chemother. Rep. 50, 163–170 (1966).
- 23.
Cox, D. R. Regression models and life tables (with discussion). J. R. Stat. Soc. B34, 187–220 (1972).
- 24.
Kaplan, E. L. & Meier, P. Nonparametric estimation from incomplete observations. J. Am. Stat. Assoc. 53, 457–481 (1958).
- 25.
Agresti, Alan. Categorical Data Analysis, 2nd edn (John Wiley & Sons, New York, 2002).
- 26.
Cochran, W. G. Some methods for strengthening the common tests. Biometrics 10, 417–451 (1954).
- 27.
Mantel, N. & Haenszel, W. Statistical aspects of analysis of data from retrospective studies of disease. J. Natl. Cancer Inst. 22, 719–748 (1959).
- 28.
Cavo, M. et al. GIMEMA Italian Myeloma Network. Bortezomib with thalidomide plus dexamethasone compared with thalidomide plus dexamethasone as induction therapy before, and consolidation therapy after, double autologous stem-cell transplantation in newly diagnosed multiple myeloma: a randomised phase 3 study. Lancet 376, 2075–2085 (2010).
- 29.
Moreau, P. et al. Bortezomib, thalidomide and dexamethasone (VTD) is superior to bortezomib, cyclophosphamide and dexamethasone (VCD) prior to autologous stem cell transplantation for patients with de novo multiple myeloma: results of the prospective IFM 2013-2014 [ASH Annual Meeting Abstracts 2015, abstract 393]. American Society of Hematology website. https://ash.confex.com/ash/2015/webprogram/Paper81103.html. Accessed 10 Nov 2015.
- 30.
Jakubowiak, A. J. et al. A phase ½ study of carfilzomib in combination with lenalidomide and low-dose dexamethasone as frontline treatment for multiple myeloma. Blood 116, 679–686 (2010).
- 31.
McCarthy, P. L. et al. Lenalidomide maintenance after autologous stem-cell transplantation in newly diagnosed multiple myeloma: a meta-analysis. J. Clin. Oncol. 35, 3279–3289 (2017).
- 32.
Attal, M. et al. Lenalidomide, bortezomib, and dexamethasone with transplantation for myeloma. New Engl. J. Med. 376, 1311–1320 (2017).
- 33.
Facon, T. et al. Phase 3 Randomized study of daratumumab plus lenalidomide and dexamethasone (D-Rd) versus lenalidomide and dexamethasone (Rd) in patients with Newly Diagnosed Multiple Myeloma (NDMM) Ineligible for Transplant (MAIA); ASH 2018. Abstract LBA-2.
- 34.
Facon, T. et al. Daratumumab plus lenalidomide and dexamethasone for untreated myeloma. N. Engl. J. Med. 380, 2104–2115 (2019).
- 35.
Kapoor, P. & Rajkumar, V. MAIA under the microscope—bringing trial design into focus. Nat. Rev.: Clin. Oncol. 16, 339–340 (2019).
- 36.
Rosiñol, L. et al. Bortezomib, lenalidomide, and dexamethasone as induction therapy prior to autologous transplant in multiple myeloma. Blood 134, 1337–1345 (2019).
Gerelateerde artikelen
- ASCO 2021: aanbevolen abstracten voor vormen van bloedkanker, zoals vormen van leukemie en kanker van het beenmerg zoals Multiple Myeloma
- Belantamab mafodotin, pomalidomide en dexamethasone geeft betere ziekteprogressievrije tijd in vergelijking met pomalidomide, bortezomib en dexamethasone bij gevorderde multiple myeloma (ziekte van Kahler, botkanker)
- Bortezomib toegevoegd aan lenalidomide plus dexamethason bij niet eerder behandelde multiple myeloma geeft verbetering van progressievrije ziekte (plus en mediane overall overleving
- CAR-T cel behandeling met Ciltacabtagene autoleucel (cilta-cel-infusie) geeft lager risico op ziekteprogressie of overlijden en meer complete remissies dan standaardzorg bij patiënten met multiple myeloma met lenalidomide resistentie
- Cryotherapie tijdens toediening van Melphalan bij Kahler zorgt voor hoog significante verbetering van minder optreden van mucositis en andere bijwerkingen behorend bij chemo en beenmergtransplantatie.
- Daratumumab alleen gegeven geeft uitstekende resultaten bij patienten met actieve sluimerende Multiple Myeloma in vergelijking met actief monitoren
- Elotuzumab - een immuuntherapeutisch middel - aanvullend op lenalidomide en dexamethason geeft 30% betere overall overleving en progressievrije ziekte dan alleen lenalidomide en dexamethason bij gevorderde Multiple Myeloma - Kahler
- Genentest blijkt voorspellende waarde te hebben bij het verloop van Multiple Myeloma - ziekte van Kahler. Ook bij eerste diagnose.
- Hoewel overall overleving sterk verbetert met nieuwe medicijnen bij Multiple Myeloma / ziekte van Kahler blijven patienten met de del17p mutatie een veel slechtere prognose op overleving te hebben.
- Idecabtagene vicleucel (Abecma) geeft als immuuntherapie via CAR-T cellen bij patienten met zwaarvoorbehandelde vergevorderde multiple myeloma uitstekende resultaten copy 1
- intraveneus immunoglobuline voorkomt voor 90 procent ernstige infecties bij patienten met multiple myeloma die met op BCMA gerichte bispecifieke antilichamen worden behandeld
- Immuuntherapie met gepersonaliseerde dendritische celtherapie plus onderhoudsdosis lenalidomide na autologe stamceltransplantatie verbetert bij multiple myeloma complete remissies met ruim 7 procent na 1 jaar.
- Isatuximab aanvullend op lenalidomide, bortezomib en dexamethason vooraf aan stamceltransplantatie geeft betere meetbare restziekte - MRD (50 vs 36 procent) bij patiënten met nieuw gediagnosticeerde multiple myeloma die stamceltransplantatie ondergaan
- Isatuximab naast pomalidomide + dexamethason geeft betere overall overleving (Mediaan + 6,9 maanden) dan alleen pomalidomide + dexamethason bij patienten met multiple myeoloma (Kahler - botkanker) die zwaar voorbehandeld waren
- Jongere volwassenen met nieuw gediagnosticeerde multiple myeloma - botkanker die een autologe stamceltransplantatie ondergaan hebben een veel betere progressievrije overleving en een veel betere mediane overleving in vergelijking met 13 jaar geleden
- lenalidomide na autologe stamceltransplantatie bij multiple myeloma - ziekte van Kahler geeft superieure overall overleving en ziektevrije tijd
- Multiple Myeloma patienten met hoog risico vastgesteld door genentest hebben betere overleving bij behandeling met daratumumab, cyclofosfamide, bortezomib, lenalidomide en dexamethason zowel voor als na autologe stamceltransplantatie
- Meta-analysis Shows Association of Minimal Residual Disease–Negative Status With Improved Survival in Multiple Myeloma
- Nederlandse studie geeft overzicht van overall overleving bij Multiple Myeloma (Kahler) in alle stadia in periode 2008 tot 2013.
- Nelfinavir, een HIV remmer, plus bortezomib (velcade) geeft uitstekende resultaten - 65 procent bereikte PR - bij zwaar voorbehandelde patienten met vergevorderde multiple myeloma, Kahler
- Pembrolizumab plus lenalidomide en dexamethasone als eerstelijns behandeling voor patienten met nog onbehandelde multiple myeloma (Kahler) geeft geen betere resultaten en veel meer ernstige bijwerkingen
- Talquetamab, een nieuw bispecifiek antilichaam gericht op het antigen GPRC5D geeft veelbelovende resultaten bij zwaar voorbehandelde patienten met myeloma - botkanker (Kahler)
- Thalidomide naast dexamethason geeft bij Kahler - Multiple Myeloma een significant positief effect op aanslaan van behandeling, aldus Fase III studie. Artikel geplaatst juni 2004
- Teclistamab en daratumumab samen geeft bij gevorderde botkanker - multiple Myeloma betere progressievrije overleving en algehele overleving vergeleken met de standaardbehandeling
- Teclistamab geeft hele goede resultaten met 50 procent meer gedeeltelijke remissies en 20 procent complete remissies bij zwaar voorbehandelde patiënten met botkanker - multiple myeloma
- Vaccin gebaseerd op MUC1 lijkt veelbelovende ontwikkeling melden Israelische onderzoekers
- Velcade - Bortezomib: wat is dit voor middel en bij welke kankersoorten wordt het gebruikt: een overzicht van recente ontwikkelingen
- Venetoclax, een kleine molecuulremmer uit de BCL-2 groep, geeft veelbelovende resultaten bij vergevorderde zwaar voorbehandelde multiple myeloma (Kahler)
- Reguliere oncologie: Kahler - Multiple Myeloma - botkanker: een overzicht van recente ontwikkelingen binnen de reguliere oncologie bij elkaar gezet



Plaats een reactie ...
Reageer op "Bortezomib toegevoegd aan lenalidomide plus dexamethason bij niet eerder behandelde multiple myeloma geeft verbetering van progressievrije ziekte (plus en mediane overall overleving"