Aan dit artikel is enkele uren gewerkt. Opzoeken, vertalen, plaatsen enz. Als u ons wilt ondersteunen dan kan dat via een al of niet anonieme donatie. Elk bedrag is welkom hoe klein ook. Klik hier als u ons wilt helpen kanker-actueel online te houden Wij zijn een ANBI organisatie en dus is uw donatie aftrekbaar voor de belasting.
Raadpleeg ook literatuurlijsten niet-toxische middelen en behandelingen specifiek bij borstkanker van arts-bioloog drs. Engelbert Valstar
13 augustus 2021: Aanvullend op onderstaand artikel werden op ASCO 2021 de resultaten van de MINDACT trial gepresenteerd die onderzocht wat de effecten waren van het gebruik van de 70 genentest voor hoog risico groepen, laag risico groepen en heel laag risico groepen op overall overleving en kansen op een recidief bij borstkankerpatiënten.
De 70-genentest (Mammaprint) is namelijk een uitstekend voorspellend hulpmiddel voor het bepalen van hoog risico versus laag risico door het meten van genomische kenmerken van recidief bij vroege borstkanker. De laagrisicogroep kan eigenlijk in twee groepen worden verdeeld, een ultralaagrisicogroep en de laagrisicogroep. En de onderzoekers analyseerden eerdere resultaten uit de MINDACT-studie, die aantoonde dat patiënten met klinisch hoge en genomische lage scores over het algemeen geen chemotherapie nodig hebben, maar als ze keken naar de subgroep van patiënten die ultralaag waren, vertegenwoordigt dat ongeveer 15% van de de MINDACT-patiënten in de HR-positieve, HER2-subgroep. En wat ze vonden waren uitstekende resultaten voor patiënten zonder uitzaaiingen en uitzaaiingen op afstand voor genomische lage en ultralage patiënten.
In feite was bij de ultralage patiënten het interval van 8 jaar zonder metastasen op afstand 97% en was het nog steeds goed in het lage risico met 94,5% en niet zo goed in de hoge risicogroep. Deze patiënten hebben dus een extreem goede prognose. Er was een klein verschil naar klinisch risico.
Degenen met een klinisch hoog risico hadden een 95% 8-jarige DMFI [uitzaaiingsvrije ziekte], terwijl het percentage voor de klinische lage en de ultralage groep 97,6% was. Dus deze patiënten doen het wonderbaarlijk goed.
Een zeer interessant aspect van de MINDACT-studie was dat sommige patiënten uit eigen beweging geen hormoontherapie wilden. Dat was een kleine groep, maar als ze keken naar degenen die geen hormoontherapie kregen in de ultralage subgroep, was hun 8-jarige DMFI 97,8%. En degenen die wel hormoontherapie kregen was 97,4%, wat suggereert dat voor die groep patiënten hormoontherapie niet nodig is.
Klik op de titel voor het studierapport zoals dat in The Lancet is gepubliceerd. Onderaan staat abstract zoals gepresenteerd op ASCO 2021:
21 augustus 2015: Bron: Jama oncology:
80 procent van patiënten met borstkanker met DCIS – ductaal carcinoma in situ - zouden kunnen volstaan met alleen een operatie, maar zonder bestraling post operatief of zelfs met een wait-and-see beleid zonder welke behandeling dan ook. Weinig vrouwen ontwikkelen namelijk een recidief van invasieve borstkanker vanuit DICS of krijgen een vorm van uitgezaaide borstkanker en slechts 3,8% van patiënten met borstkanker overlijden binnen 20 jaar aan hun borstkanker.
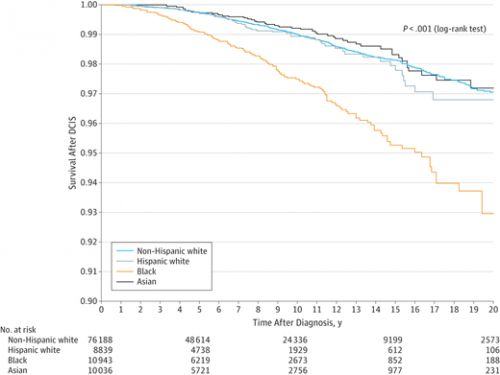
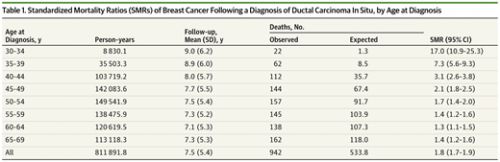
Alleen vrouwen jonger dan 35 jaar en zwarte vrouwen hebben een groter risico op overlijden binnen 20 jaar: voor vrouwen jonger dan 35 jaar is dat risico: (7.8% vs 3.2%; hazard ratio , 2.58; P < .001), voor zwarte vrouwen in vergelijking met blanke vrouwen is het risico: (7.0% vs 3.0%; HR, 2.55; P < .001). ook werd een groter risico op overlijden aan borstkanker gevonden bij DCIS met bepaalde eigenschappen, zoals bv. estrogeen-receptor status, gradatie, comedo necrosis (dode cellen blokkeren de melkgangen) en grootte (>5 cm). Deze bevestigden al eerder gevonden resultaten dat DCIS met hooggradige tumoren grotere kans hebben op overlijden aan borstkanker dan vrouwen met laaggradige tumoren. (1,88 keer grotere kans op overlijden = P < .001).
Dit alles blijkt uit nieuwe resultaten van een observatie studie van meer dan 100.000 vrouwen met een ductaal carcinoma in situ (DCIS). “Dit geeft een dwingende reden dat het tijd is voor een verandering in het behandelen van deze ziekte”, volgens een paar experts.
Wat is DUCTAAL CARCINOMA IN-SITU (DCIS)
Ductaal carcinoma in-situ (ook intraductaal carcinoom genoemd) is de abnormale groei van cellen die de melkgangen bekleden, die wordt begrensd door het basaalmembraan en niet doordringt in het omliggende borstweefsel. DCIS wordt beschouwd als een precancereuze aandoening omdat deze niet-invasief is. DCIS kan worden onderverdeeld in het comedo-type en non-comedo-type (of soms gemengd). Comedo-type DCIS is het agressiefste en snelst groeiende type met de hoogste kans op progressie tot invasieve borstkanker. De term 'comedo' verwijst naar het midden van de melkgang die wordt afgesloten door dode cellen, of necrose. Non-comedo-type DCIS omvat solide, micropapillaire en cribriforme DCIS. DCIS wordt meestal ontdekt met mammografie en kan worden bevestigd door een biopsie of FNA van de borst. DCIS wordt gewoonlijk ontdekt bij patiënten in de leeftijd van 50 tot 60 jaar. Ongeveer 20% van alle nieuwe gevallen van borstkanker betreft ductaal carcinoma in-situ.
“De studie geeft verdere informatie aan een groeiende bezorgdheid dat we onze strategie voor de opsporing en behandeling van DCIS - ductaal carcinoma in situ - moeten heroverwegen," schrijven Laura Esserman, MD, MBA, en Christina Yau, PhD, van de Universiteit van California, San Francisco, in een begeleidend schrijven naast de studie die online gepubliceerd is in JAMA Oncology.
Gezien de kleine kans om aan deze vorm van borstkanker te overlijden (3,3% binnen 20 jaar) bij vrouwen in de studie - die een scala aan behandelingen ondergingen voor hun DCIS – zeggen de commentatoren: "We moeten stoppen met te vertellen vrouwen dat DCIS is een noodsituatie verkeren en dat zij definitief een operatie moeten plannen binnen 2 weken na de diagnose."
Behandeling met "de huidige agressieve normen" is passend bij ongeveer 20% van de gevallen; bepaald met name door jonge leeftijd bij diagnose, Afrikaans / Amerikaanse afkomst en / of specifieke kenmerken van de tumor, maar voor de overige grote meerderheid, moeten andere benaderingen worden overwogen, aldus schrijft de commentatoren in het begeleidend schrijven. Bv. alleen endocriene therapie – hormoonremmers zou voldoende kunnen zijn en voor vrouwen met het laagste risico zou een wait-and-see beleid verdedigbaar zijn.
Hoofdonderzoeker Steven Narod, MD, van de Women's College Hospital in Toronto, stelde ook dat veranderingen in een behandelingsaanpak verdedigbaar zijn:
Dr. Narod zegt: “een behandeling kan twee doelen hebben: een recidief voorkomen of het overlijden aan de ziekte voorkomen.”
"Als het doel is om te voorkomen dat in de borst een recidief optreedt dan zijn bestraling - radiotherapie en mastectomie (operatie van hele borst) goede behandelingsopties,"
"maar als het doel is om overlijden aan borstkanker te voorkomen, zou de beste optie zijn een wait-and-see beleid. Op het moment dat er een recidief optreed of er sprake wordt van invasieve kanker of er zijn uitzaaiingen, kan direct gestart worden met chemotherapie en/of hormoonbehandelingen," aldus Dr. Narod
Beide benaderingen zijn echter wel in strijd met de gangbare praktijk en de richtlijnen, die al of niet borstbesparende operatie - gevolgd door bestraling voorschrijft.
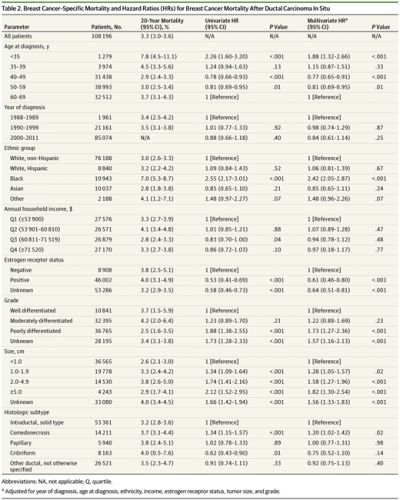
Studieresultaten:
In hun studie beoordeelden Dr Narod en zijn collega's 108.000 gevallen van DCIS die werden gediagnosticeerd in de periode van 1988-2011 zoals geregistreerd in de Epidemiologie,and End Results (SEER) database. De gemiddelde follow-up was 7,5 jaar.
De onderzoekers haalden een scala aan informatie uit de database, waaronder de doodsoorzaak. Zij vergeleken het risico op sterven aan borstkanker bij vrouwen met DCIS en bij vrouwen in de algemene bevolking, en de geschatte hazard ratio voor sterfte van DCIS met behulp van een verscheidenheid van factoren, zoals leeftijd en behandeling.
Op 20 jaar, borstkanker mortaliteit – de kans aan borstkanker te overlijden - was 3,3%, wat lager is dan eerdere bevindingen, hoewel niet veel lager. Dit cijfer is niet statistisch significant anders dan de statistiek die de American Cancer Society hanteert en de kans dat de gemiddelde vrouw zal sterven aan borstkanker," aldus het begeleidend schrijven bij de studie.
Het risico van overlijden aan borstkanker bij 20 jaar is wel veel hoger bij vrouwen met bepaalde eigenschappen. Bijvoorbeeld, de mortaliteit is hoger bij vrouwen jonger dan 35 jaar bij diagnose dan bij vrouwen ouder dan 35 jaar (7,8% vs 3,2%; hazard ratio , 2,58; p <0,001) en was hoger bij zwarte vrouwen dan bij blanke vrouwen (7,0% versus 3,0%; HR, 2.55; p <0,001).
Een hoger percentage van borstkanker sterfte werd ook gezien voor DICS – ductaal carcinoma in situ met bepaalde kenmerken, zoals oestrogeen-receptor status, gradatie, grootte (> 5 cm) en comedo necrosis.
In totaal, ongeveer 20% van de vrouwen gediagnosticeerd met DCIS had één of meer van deze kenmerken en was geassocieerd met een hoger risico op overlijden aan borstkanker.
De studie toonde ook aan, zoals verwacht, dat wanneer invasieve ziekte optreedt, de dood veel waarschijnlijker zal volgen. Specifiek, het risico van overlijden aan borstkanker is sterk verhoogd na de ontwikkeling van een ipsilaterale invasieve borstkanker (HR, 18,1; p <0,001).
Maar van het grootste klinisch belang was dat de preventie van een ipsilateral invasieve recidief d.m.v. daarop gerichte behandelingen de kans op overlijden aan borstkanker niet is te voorkomen, aldus de onderzoekers.
Een intuïtieve verwachting is dat als je kunt voorkomen dat een DCIS recidief ontstaat en/of uitgroeit tot invasieve ziekte met een specifieke behandeling, dan zal je naar verwachting het risico aan borstkanker te overlijden minder maken.
Maar dat is niet wat er gebeurd is, zo onderstrepen de onderzoekers hun bevindingen.
In plaats daarvan, voor patiënten die een borstbesparende operatie ondergingen werd de toevoeging van bestraling geassocieerd met een vermindering van het risico op een ipsilaterale invasief recidief binnen 10 jaar (2,5% versus 4,9%, gecorrigeerd HR, 0,47; p <0,001), maar niet van borstkanker-specifieke sterfte op 10 jaar (0,8% versus 0,9%; HR, 0,86; p = 0,22).
Dus een zwaardere behandeling voor DCIS (borstbesparende operatie plus bestraling) in vergelijking met de minder zwaardere therapie (borstbesparende operatie alleen) was wel goed om het risico op een invasieve ziekte te voorkomen, maar niet om het risico van overlijden aan borstkanker te verminderen.
Er waren ook vrouwen in de studie die een borstamputatie ondergingen. Ook hierbij vonden de onderzoekers hetzelfde patroon - de intensievere behandeling was goed voor het verminderen van risico op een recideif en invasieve ziekte, maar gaf geen verschil te zien in kans op overlijden aan borstkanker.
Hoewel de risico’s voor een ipsilateraal invasief recidief op 10 jaar lager was bij patiënten die een eenzijdige mastectomie – volledige borstamputatie hadden gehad dan bij degenen die een borstbesparende operatie hadden gehad (1,3% versus 3,3%), was het risico op overlijden aan borstkanker bij mastectomiepatiënten hoger dan in lumpectomie patiënten ( 1,3% versus 0,8%). Deze bevinding is verrassend, maar omdat de mastectomiepatiënten grotere en hogere graad tumoren hadden gemiddeld was in feite, wanneer deze factoren gecorrigeerd werden, het verschil in 10-jaars overleving statistisch niet significant tussen beide groepen.
Meest verrassende bevinding
Dr. Narod: “De meest verrassende bevinding van de studie is dat de meerderheid van de vrouwen die aan borstkanker stierven na een diagnose van DICS – ductaal carcinoma in situ in de Verenigde Staten [tijdens de onderzoeksperiode] nooit een recidief van DCIS in invasieve borstkanker hebben ervaren voorafgaand aan het ontwikkelen van uitgezaaide borstkanker. "
Uit het onderzoek blijkt dat 517 patiënten stierf aan borstkanker na de diagnose DICS – ductaal carcinoma in situ zonder het ervaren van een invasieve borstkanker vóór de dood. Dit blijkt bij 54% van alle sterfgevallen borstkanker in de studie wel zo te zijn, maar bedraagt slechts 0,48% van de 108.000 deelnemers oorspronkelijk gediagnosticeerd met DICS – ductaal carcinoma in situ.
Deze vaststelling is in strijd met de veronderstelling dat DCIS een voorloper van kanker is en de dood kan veroorzaken, indien het zich ontwikkelt tot een invasieve ziekte, zeggen de onderzoekers.
Drs Esserman en Yau wijzen in hun begeleidend schrijven erop dat DCIS als het gaat om aan borstkanker te overlijden zonder zich eerst te ontwikkelen tot een invasieve kanker niet gebruikelijk is (<1%), maar ze benadrukken ook dit als een belangrijk inzicht uit de studie: "Er zijn soms gevallen waarin DCIS een hoger risico op overlijden geeft dan nu wordt verondersteld."
Maar ze benadrukken dat 80% van patiënten met DICS – ductaal carcinoma in situ - hebben een laag risico tot overlijden aan borstkanker.
In sommige gevallen zouden patiënten kunnen volstaan met bv. hormoontherapie met tamoxifen / raloxifene of aromataseremmers, terwijl vrouwen met het laagste risico in het geheel niet hoeven worden behandeld, maar kunnen vanuit een wait-and-see beleid gevolgd worden met observatie en preventie aanpak, aldus de commentatoren. Dit zou onder andere voeding, lichaamsbeweging en alcohol matiging kunnen zijn, en het vermijden van postmenopauzale hormoontherapie met progesteron bevattende medicijnen. Misschien handig ook eens deze lijst te lezen want in het voorkomen van een recideif van ook borstkanker is al veel onderzoek naar verricht:
https://kanker-actueel.nl/NL/studiepublicaties-van-niet-toxische-middelen-en-behandelingen-uit-literatuurlijst-van-arts-bioloog-drs-engelbert-valstar-gerelateerd-aan-borstkanker.html
Het begeleidend schrijven: Rethinking the Standard for Ductal Carcinoma In Situ Treatment is gratis te lezen:
zoals ook het volledige studierapport: Breast Cancer Mortality After a Diagnosis of Ductal Carcinoma In Situ gratis is in te zien.
Hier het abstract van de studie:
The risk of death increases after a diagnosis of an ipsilateral second primary invasive breast cancer, but prevention of these recurrences by radiotherapy does not diminish breast cancer mortality at 10 years.
At a Glance
-
The purpose of this study was to estimate the mortality from breast cancer following a diagnosis of ductal carcinoma in situ (DCIS) and to identify risk factors for death from breast cancer.
-
The 20-year breast cancer–specific mortality rate following a diagnosis of DCIS was 3.3%.
-
Young age at diagnosis and black ethnicity were significant predictors of breast cancer mortality.
-
Prevention of invasive in-breast recurrence with either radiotherapy or mastectomy did not prevent death from breast cancer.
-
The clinical course of women with DCIS is similar to that of women with small invasive breast cancers.
Breast Cancer Mortality After a Diagnosis of Ductal Carcinoma In Situ FREE ONLINE FIRST
Steven A. Narod, MD, FRCPC1,2; Javaid Iqbal, MD1; Vasily Giannakeas, MPH1,2; Victoria Sopik, MSc1; Ping Sun, PhD1
JAMA Oncol. Published online August 20, 2015. doi:10.1001/jamaoncol.2015.2510
Importance Women with ductal carcinoma in situ (DCIS), or stage 0 breast cancer, often experience a second primary breast cancer (DCIS or invasive), and some ultimately die of breast cancer.
Objective To estimate the 10- and 20-year mortality from breast cancer following a diagnosis of DCIS and to establish whether the mortality rate is influenced by age at diagnosis, ethnicity, and initial treatment received.
Design, Setting, and Participants Observational study of women who received a diagnosis of DCIS from 1988 to 2011 in the Surveillance, Epidemiology, and End Results (SEER) 18 registries database. Age at diagnosis, race/ethnicity, pathologic features, date of second primary breast cancer, cause of death, and survival were abstracted for 108 196 women. Their risk of dying of breast cancer was compared with that of women in the general population. Cox proportional hazards analysis was performed to estimate the hazard ratio (HR) for death from DCIS by age at diagnosis, clinical features, ethnicity, and treatment.
Main Outcomes and Measures Ten- and 20-year breast cancer–specific mortality.
Results Among the 108 196 women with DCIS, the mean (range) age at diagnosis of DCIS was 53.8 (15-69) years and the mean (range) duration of follow-up was 7.5 (0-23.9) years. At 20 years, the breast cancer–specific mortality was 3.3% (95% CI, 3.0%-3.6%) overall and was higher for women who received a diagnosis before age 35 years compared with older women (7.8% vs 3.2%; HR, 2.58 [95% CI, 1.85-3.60]; P < .001) and for blacks compared with non-Hispanic whites (7.0% vs 3.0%; HR, 2.55 [95% CI, 2.17-3.01]; P < .001). The risk of dying of breast cancer increased after experience of an ipsilateral invasive breast cancer (HR, 18.1 [95% CI, 14.0-23.6]; P < .001). A total of 517 patients died of breast cancer following a DCIS diagnosis (mean follow-up, 7.5 [range, 0-23.9] years) without experiencing an in-breast invasive cancer prior to death. Among patients who received lumpectomy, radiotherapy was associated with a reduction in the risk of ipsilateral invasive recurrence at 10 years (2.5% vs 4.9%; adjusted HR, 0.47 [95% CI, 0.42-0.53]; P < .001) but not of breast cancer–specific mortality at 10 years (0.8% vs 0.9%; HR, 0.86 [95% CI, 0.67-1.10]; P = .22).
Conclusions and Relevance Important risk factors for death from breast cancer following a DCIS diagnosis include age at diagnosis and black ethnicity. The risk of death increases after a diagnosis of an ipsilateral second primary invasive breast cancer, but prevention of these recurrences by radiotherapy does not diminish breast cancer mortality at 10 years.
The 70-gene signature shows an intact ability of identifying among women with high clinical risk, a subgroup, namely patients with a low genomic risk, with an excellent distant metastasis-free survival when treated with endocrine therapy alone
ASCO 2021:
Outcome of patients with an ultralow risk 70-gene signature in the MINDACT trial.
Authors:
Josephine Lopes Cardozo, Caroline Drukker, Marjanka Schmidt, Laura van 't Veer, Annuska Glas, Anke Witteveen, Fatima Cardoso, Martine J. Piccart-Gebhart, Coralie Poncet, Emiel J. Rutgers
Research Funding:
This research was supported by a grant from the EORTC Breast Group and from the Netherlands Cancer Institute.
Background:Gene signatures have proven successful in identifying patients with a low risk of distant recurrence who could forego chemotherapy (CT) and are currently included in international treatment guidelines for breast cancer. For the 70-gene signature (MammaPrint) an additional threshold was established within the low risk category to identify patients with an ultralow risk of distant recurrence. In independent cohorts, these patients had excellent breast cancer specific survival at 15 years, suggesting that ultralow risk cancers represent indolent disease (Esserman, JAMA Oncol 2017, Delahaye, BC Res Treat 2017). Here we evaluate survival of patients with an ultralow risk 70-gene signature who participated in the randomized phase 3 MINDACT trial (Piccart, Lancet Oncol 2021).Methods:Of the 6,693 patients enrolled in the MINDACT trial (EORTC 10041/BIG 3-04) between 2007-2011, profiling revealed an ultralow risk 70-gene signature in 1,000 patients (15%). We assessed 5- and 8-year distant metastasis free interval (DMFI) and breast cancer specific survival (BCSS) in patients stratified by 70-gene signature result (high, low, ultralow), and within the ultralow risk group stratified by clinical risk. For these exploratory analyses, we used Kaplan-Meier estimates for time to event endpoints and Cox-regression models to calculate hazard ratio’s (HR).Results:Median follow-up was 8.7 years. Among the ultralow risk patients (n = 1,000), 67% were ≥50 years, 81% had tumors < 2cm, 80% were lymph node negative, 96% had grade 1 or 2 tumors and 99% were ER-positive. Systemic therapy was received by 83% of patients (69% endocrine therapy (ET), 14% ET + CT) and 16% received no adjuvant systemic treatment (AST). Survival estimates for all endpoints are shown in the table; 8-year DMFI was 97.0% (95% CI 95.8-98.1) for ultralow risk. The 8-year DMFI in ultralow risk patients who received no AST or ET only was 97.8% (95% CI 95.3-100) and 97.4% (95% CI 96.1-98.7), respectively. The HR for DMFI was 0.66 (95% CI 0.46-0.95) for ultralow vs low risk, after adjusting for tumor and treatment characteristics (preliminary results).Conclusions:In this prospective study, patients with an ultralow risk 70-gene signature have an excellent prognosis with 8-year BCSS above 99% regardless of clinical risk status, and with an 8-year DMFI of 95-98%.
| 70-gene signature | Events
(N) | 5-year DMFI
(95% CI) | 8-year DMFI
(95% CI) | 8-year BCSS
(95% CI) |
|---|
| Ultralow risk (n = 1000) |
36 |
98.1% (97.2-99.0) |
97.0% (95.8-98.1) |
99.6% (99.1-100) |
| Low risk* (n = 3295) |
192 |
97.5% (97.0-98.1) |
94.5% (93.6-95.3) |
98.2% (97.7-98.7) |
| High risk (n = 2398) |
273 |
92.5% (91.4-93.6) |
89.2% (87.9-90.5) |
93.7% (92.6-94.7) |
| Ultralow risk |
|
|
|
|
| Clinical low risk (n = 741) |
21 |
98.7% (97.8-99.5) |
97.6% (96.4-98.8) |
99.7% (99.3-100) |
| Clinical high risk (n = 259) |
15 |
96.3% (94.0-98.7) |
95.0% (92.3-97.8) |
99.2% (98.0-100) |
*Low risk excludes ultralow risk.
This material on this page is ©2021 American Society of Clinical Oncology, all rights reserved. Licensing available upon request. For more information, please contact licensing@asco.org.
References
- 1.
- Early Breast Cancer Trialists' Collaborative Group (EBCTCG)
Effects of chemotherapy and hormonal therapy for early breast cancer on recurrence and 15-year survival: an overview of the randomised trials.
Lancet. 2005; 365: 1687-1717
- 2.
- Dowsett M
- Goldhirsch A
- Hayes DF
- Senn HJ
- Wood W
- Viale G
International web-based consultation on priorities for translational breast cancer research.
Breast Cancer Res. 2007; 9: R81
- 3.
- Azim Jr, HA
- de Azambuja E
- Colozza M
- Bines J
- Piccart MJ
Long-term toxic effects of adjuvant chemotherapy in breast cancer.
Ann Oncol. 2011; 22: 1939-1947
- 4.
- Ferreira AR
- Di Meglio A
- Pistilli B
- et al.
Differential impact of endocrine therapy and chemotherapy on quality of life of breast cancer survivors: a prospective patient-reported outcomes analysis.
Ann Oncol. 2019; 30: 1784-1795
- 5.
- Sparano JA
- Gray RJ
- Makower DF
- et al.
Adjuvant chemotherapy guided by a 21-gene expression assay in breast cancer.
N Engl J Med. 2018; 379: 111-121
- 6.
- Cardoso F
- van't Veer LJ
- Bogaerts J
- et al.
70-gene signature as an aid to treatment decisions in early-stage breast cancer.
N Engl J Med. 2016; 375: 717-729
- 7.
- Bogaerts J
- Cardoso F
- Buyse M
- et al.
Gene signature evaluation as a prognostic tool: challenges in the design of the MINDACT trial.
Nat Clin Pract Oncol. 2006; 3: 540-551
- 8.
- Mook S
- Schmidt MK
- Viale G
- et al.
The 70-gene prognosis-signature predicts disease outcome in breast cancer patients with 1-3 positive lymph nodes in an independent validation study.
Breast Cancer Res Treat. 2009; 116: 295-302
- 9.
- van 't Veer LJ
- Dai H
- van de Vijver MJ
- et al.
Gene expression profiling predicts clinical outcome of breast cancer.
Nature. 2002; 415: 530-536
- 10.
- Ravdin PM
- Siminoff LA
- Davis GJ
- et al.
Computer program to assist in making decisions about adjuvant therapy for women with early breast cancer.
J Clin Oncol. 2001; 19: 980-991
- 11.
- Delaloge S
- Piccart M
- Rutgers E
- et al.
Standard anthracycline based versus docetaxel-capecitabine in early high clinical and/or genomic risk breast cancer in the EORTC 10041/BIG 3-04 MINDACT phase III trial.
J Clin Oncol. 2020; 38: 1186-1197
- 12.
- Krop I
- Ismaila N
- Andre F
- et al.
Use of biomarkers to guide decisions on adjuvant systemic therapy for women with early-stage invasive breast cancer: American Society of Clinical Oncology clinical practice guideline focused update.
J Clin Oncol. 2017; 35: 2838-2847
- 13.
- Sparano JA
- Gray RJ
- Ravdin PM
- et al.
Clinical and genomic risk to guide the use of adjuvant therapy for breast cancer.
N Engl J Med. 2019; 380: 2395-2405
- 14.
- Francis PA
- Pagani O
- Fleming GF
- et al.
Tailoring adjuvant endocrine therapy for premenopausal breast cancer.
N Engl J Med. 2018; 379: 122-137
- 15.
- Puhalla S
- Brufsky A
- Davidson N
Adjuvant endocrine therapy for premenopausal women with breast cancer.
Breast. 2009; 18: S122-S130
- 16.
- Goldhirsch A
- Ingle JN
- Gelber RD
- Coates AS
- Thürlimann B
- Senn HJ
Thresholds for therapies: highlights of the St Gallen International Expert Consensus on the primary therapy of early breast cancer 2009.
Ann Oncol. 2009; 20: 1319-1329
- 17.
- Coates AS
- Winer EP
- Goldhirsch A
- et al.
Tailoring therapies—improving the management of early breast cancer: St Gallen International Expert Consensus on the Primary Therapy of Early Breast Cancer 2015.
Ann Oncol. 2015; 26: 1533-1546
- 18.
Estimating risk of recurrence for early breast cancer: Integrating clinical and genomic risk.
J Clin Oncol. 2019; 37: 689-692
- 19.
- Jacob L
- Witteveen A
- Beumer I
- et al.
Controlling technical variation amongst 6693 patient microarrays of the randomized MINDACT trial.
Commun Biol. 2020; 3: 397
Article Info
Publication History
Published: March 12, 2021
Copyright
© 2021 Elsevier Ltd. All rights reserved.
DCIS - ductaal carcinoma in situ, borstkanker, kans op ovelrijden, kans op recideif van invasieve borstkanker, voeding, wait-and-see beleid, niet-toxische middelen en behandelingen, complementair
Gerelateerde artikelen
- Bloedtest via ctDNA meting op in bloed circulerend DNA geeft al na een maand aan of behandelingen bij borstkanker effectief zijn of niet.
- Doelgerichte studie vergelijkingen van observatiestudies voor 8 belangrijke medicijnen voor uitgezaaide borstkanker in de klinische praktijk komen 7 van de 8 overeen met resultaten uit fase III studies
- Richtlijnen hoe uitgezaaide borstkanker met lage HER2 expressie (+1 of +2) te behandelen met of Sacituzumab govitecan of trastuzumab deruxtecan is door een team van deskundigen in een officieel rapport vastgelegd
- Richtlijnen in Amerika hoe borstkanker te behandelen met Her2 positieve receptoren op basis van recente wetenschappelijke studies
- Niet alle borstkankerpatienten hebben chemo of bestraling nodig omdat zij meer en krachtigere immuuncellen (TIL) hebben die de borstkanker automatisch opruimt.
- Leverresectie voor aan borstkanker gerelateerde levermetastasen geeft een mediane ziektevrije overleving van 50 maanden en een 5-jaars overleving van 65 procent
- 80 procent van patiënten met borstkanker met DCIS – ductaal carcinoma in situ - zouden kunnen volstaan met alleen een operatie, maar zonder bestraling post operatief of zelfs met een wait-and-see beleid
- Regelmatig uitvoeren van FDG-PET / CT scan voor monitoring van effecten van behandelingen bij uitgezaaide borstkanker signaleert eerder resistentie en kan sneller verandering van behandelingen bewerkstelligen.
- Maagzuurremmers tijdens en na de behandeling van kanker lijkt gerelateerd aan een verminderd geheugen en concentratie bij overlevenden van borstkanker
- Koud kussen - cool pad pillow topper - vermindert opvliegers en sterk transpireren met meer dan de helft in de nacht bij borstkankerpatienten die hormoontherapie gebruiken en verbetert daardoor het slapen copy 1
- Melkzuurbacterien - probiotica aanwezig in gezond borstweefsel beschermt vrouwen tegen borstkanker blijkt uit kleinschalige studie copy 1
- Verschil in status en afwijkende mutaties tussen primaire tumor en uitzaaiingen bij borstkanker komt vaker voor - ca. 20 procent - dan gedacht blijkt uit biomoleculaire profile studie
- Borsttumoren vergen vaak andere behandeling dan eerste behandelplan na second opinion aldus het Alexander Monro Ziekenhuis in Bilthoven in de Telegraaf
- Borstkanker kliniek Alexander Mono ziekenhuis in Bilthoven opent volgende maand de deuren. Ziektekosten verzekeraars erkennen en betalen specialistische zorg in prive kliniek
- Borstbesparende ingreep gevolgd door bestraling geeft betere kans op overleving - 13 procent - dan borstamputatie, vooral bij hormoongevoelige borstkanker blijkt uit grote langjarige studie
- Algemeen - Wetenschappelijk onderzoek bij borstkanker: Overzicht van lopende fase I, II, III studies bij borstkanker in Nederland en Europa.
- Algemeen: Borstkankerpatienten met DICS (ductaal in situ) - overleven steeds langer zonder recidief door adekwate behandelingen, blijkt uit grote langjarige gerandomiseerde studie.
- Algemeen:screening via periodieke mammografie geeft weinig tot geen invloed op cijfers van sterfte aan borstkanker, blijkt uit groot onderzoek van WHO in landen die vroeger en later bevolkings screening toe gingen passen, zoals bv. Nederland en Belgie.
- Algemeen: bij vrouwen met uitgezaaide borstkanker blijkt status van ER, PR en HER2-Neu vaak verschillend (bij 48,6%) en ook vaak te veranderen en vereist soms nieuwe behandelingsstrategie. Aldus gerandomiseerde studie. Artikel geplaatst 12 mei 2010
- Algemeen: Uitzaaiingen van primaire borstkanker of tumoren bij het ontstaan van een recidief van voormalig primaire borstkanker kunnen een andere receptor status hebben en hebben dus andere behandeling nodig
- Algemeen: Biopt uit schildwachtklier bij borstkanker veroorzaakt niet significant meer uitzaaiingen in lymfklieren of elders in lichaam dan zonder biopt, aldus gerandomiseerde studie bij 2502 vrouwen.
- Algemeen: ook minieme uitzaaiingen leiden vaker tot recidief van borstkanker, aldus Nederlands onderzoek
- Algemeen: Overgewicht vergroot risico op uitzaaiingen bij borstkanker en vergroot significant risico op overlijden aan borstkanker met 38%, blijkt uit groot bevolkingsonderzoek
- Algemeen: Borstkanker korte algemene informatie






Plaats een reactie ...
Reageer op "80 procent van patiënten met borstkanker met DCIS – ductaal carcinoma in situ - zouden kunnen volstaan met alleen een operatie, maar zonder bestraling post operatief of zelfs met een wait-and-see beleid"