14 september 2015:
Als capecitabine plus temodal ingezet wordt als eerstelijns behandeling voor uitgezaaide pancreasNET zijn de resultaten extreem goed in vergelijking met standaard behandeling. 92% van de patiënten leefde nog na 2 jaar: zie volledige studierapport: First-line chemotherapy with capecitabine and temozolomide in patients with metastatic pancreatic endocrine carcinomas.
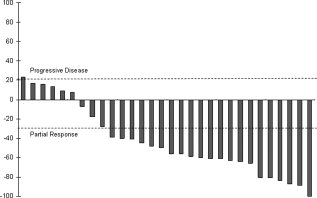
hier het volledige studierapport van onderstaande studie: Outcomes of patients treated with capecitabine and temozolamide for advanced pancreatic neuroendocrine tumors (PNETs) and non-PNETs dat gratis is in te zien. de studie is uitgebreid naar een fase II studie waarbij ook patiënten worden opgenomen met vormen van kanker niet vanuit endocriene afkomst. Er worden nng steeds patiënten aangenomen: zie studieprotocol: https://clinicaltrials.gov/ct2/show/NCT01824875?term=NCT01824875&rank=1
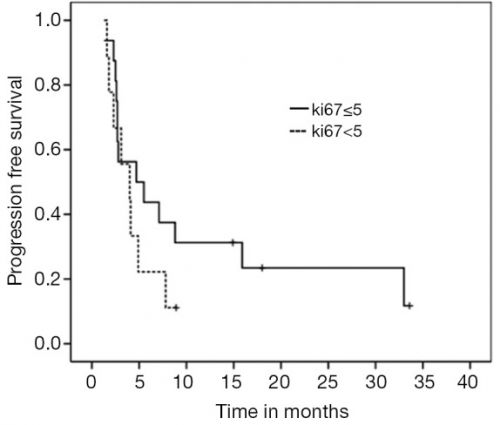
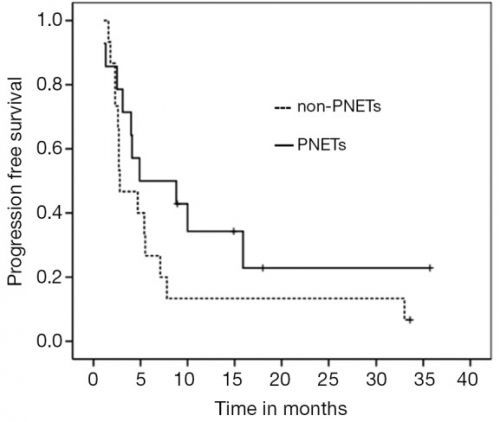
Bij de onderzoekers is er twijfel of capecitabine plus temodal ook werkt voor tumoren van niet neuro endocriene afkomst. Maar grafieken laten eigenlijk procentueel een zelfde effect zien op overall overleving.
Hier de twee grafieken, daaronder een uitgebreidere beschrijving van deze studie die zeer interessant is:
Overleving voor alle patienten
Overleving voor NET tumoren en niet NET tumoren
4 februari 2014: Bron: 2014 Gastrointestinal Cancers Symposium (GICS): Abstract 179. To be presented January 17, 2014
CAPTEM , een combinatie behandeling van Xeloda - capecitabine met temozolomide - temodal zorgt voor spectaculaire resultaten bij patiënten met alvleesklierkanker (NET tumoren), schildkliertumoren en hypofyse tumoren ontstaan vanuit neuro-endocriene afkomst.
Van de 28 deelnemende patiënten reageerde bijna iedereen (97%) positief op de behandeling met op z'n minst stabiele ziekte. 16 van de 28 deelnemers is nog steeds in leven waarvan de mediane progressievrije overlevingstijd inmiddels 29 maanden is maar deze kan nog langer worden omdat veel patiënten nog in leven zijn. Ook de bijwerkingen van deze aanpak blijken veel minder te zijn dan bij andere behandelingen van deze vorm van kanker.
Het bijzondere aan deze studie is ook dat alle patiënten vooraf de eerste lijnsbehandeling met octreotide(Sandostatine , Novartis) hebben gehad maar daaronder toch progressie van hun ziekte lieten zien. In feite waren deze patiënten dus uitbehandeld. En zoals verschillende oncologen lieten weten op de persconferentie, chemo bij deze vorm van kanker heeft weinig tot geen effect aangetoond tot nu toe. De reacties op het Gastrointestinal Cancers Symposium waren dan ook bijzonder positief omdat bij deze vorm van kanker er weinig andere opties tot behandelen zijn.
Dr. Fine van de Columbia University in New York staat aan de basis van deze studie. Hij onderzoekt al vanaf 2005 deze CAPTEM combinatie behandeling van capecitabine - xeloda plus temozolomide - temodal bij neuro endocriene tumoren.
Dr. Fine: "Temozolomide, bekend onder de merknaam Temodar, is een zogeheten cytotoxisch alkyleermiddel geïndiceerd voor gebruik bij patiënten met hersentumoren en uitgezaaide melanoom. Capecitabine - xeloda is een medicijn in tabeltvorm, wordt omgezet in het lichaam tot 5 - fluorouracil ( 5 - FU )en heeft bewezen de tumorgroei te vertragen en wordt gebruikt in een verscheidenheid van soorten kanker, zoals borstkanker en darmkanker.".
Volgens dr. Fine heeft deze combinatie zo'n grote kans van slagen omdat 5 - FU chemotherapie de "thymidine opslag" in de kankercel uitput (red: sorry maar weet niet goed wat dit precies is in het Nederlands) waardoor het celdodende aspect van temozolomide wordt versterkt.
Studieresultaten:
De studie is een zogeheten retrospectieve studie, uitgevoerd bij 28 patiënten. De studie begon al in 2005. De onderzoekers testten vooraf verschillende combinaties van medicijnen in het laboratorium voordat ze het protocol schreven dat wordt gebruikt in deze studie.
De patiënten kregen dagelijks capecitabine 1500 mg/m² gedurende 2 weken en dagelijkse temozolomide 150 tot 200 mg op dag 10 tot 14, met de volgende 2 weken geen medicijnen in een cyclus van 28 dagen. Alle deelnemende patiënten hadden goed of matig gedifferentieerde tumoren. Deze vertegenwoordigen de meeste gevallen van neuro-endocriene tumoren en staan bekend als resistent tegen een standaard eerstelijns en tweedelijns behandeling.
Overall 43 % van de deelnemende patienten reageerde positief op deze aanpak met capecitabine - xeloda en temolozomide - temodal (CAPTEM) en 54 % bereikten stabiele ziekte
CAPTEM bleek opvallend effectief bij de 3 patiënten met hypofyse tumoren, een moeilijk te behandelen neuro-endocriene tumor subtype en bekend staat als resistent te zijn tegen chemotherapie. Van de 3 patiënten met hypofyse tumoren - alle met toch progressie van de ziekte ondanks eerdere behandelingen met radiotherapie - bestraling, chemotherapie en chirurgie - bereikten 2 patiënten een volledige remissie met de behandeling (CAPTEM) en 1 patiënt bereikte een 75% reductie in tumorgrootte.
De twee complete remissies zijn heel bijzonder, aldus dr. Fine. Beide patienten waren in het eindstadium van hun ziekte en hadden al beademingsapparatuur nodig door de compressie van het ruggenmerg [veroorzaakt door de tumor]; Ze bereikten alle twee een volledige remissie, hadden de beademingsapparatuur niet meer nodig en zijn nu al bijna 4 jaar klinisch tumorvrij op een zogeheten onderhouds behandeling, aldus dr. Fine.
De combinatie behandeling bleek ook effectief bij de 11 patiënten met alvleesklierkanker vanuit neuro-endocriene oorsprong (NET tumoren). 55% bereikte stabiele ziekte, 36% een gedeeltelijke remissie (PR = 50% of meer vermindering van tumoromvang) .
De 2 patiënten met medullaire schildklier tumoren in deze studie bereikten beiden stabiele ziekte (100% respons).
Van de 12 patiënten met carcinoïde tumoren bereikten er 5 ( 41 % ) een vermindering van de tumoromvang van minstens 50% of meer. "Dit is heel ongebruikelijk ", aldus dr. Fine, omdat de respons op chemotherapie bij deze patiënten volgens de literatuur minder dan 3% is.
Voor de 28 studie patiënten was ten tijde van de analyse de mediane progressievrije overleving 22 maanden. De totale overlevingsgegevens zijn nog niet volledig te geven, maar mediane progressievrije overleving is meer dan 29 maanden op dit moment en 16 patiënten zijn nog steeds in leven en volgen nog steeds een zogeheten onderhoudsbehandeling.
Dr Fine zegt dat deze resultaten gunstig afsteken in vergelijking met octreotide, welke behandeling een respons geeft van ongeveer 6 % bij de verschillende typen van neuro-endocriene tumoren en ongeveer 30 % tot 40 % bereikt daarmee stabiele ziekte.
Tyrosine kinase remmers ( TKI's ), een klasse van geneesmiddelen voor neuro-endocriene tumoren waaronder sunitinib (Sutent , Pfizer), hebben volgens de literatuur een respons van minder dan 10 % en geven stabilisatie van de ziekte bij ongeveer 60 %. Met name klinische studies met TKI's zijn uitsluitend uitgevoerd bij patiënten met alvleesklierkanker vanuit neuro-endocriene oorsprong (NET tumoren).
Ongeveer 35% van de neuro-endocriene tumoren bestaat uit alvleeskliertumoren (NET tumoren) en deze zijn niet opgenomen in de lijst van patiënten met de meer behandelingsresistente carcinoide tumoren, welke ca. 55% deel uit maken van het totale aantal van neuro-endocriene tumoren, aldus dr. Fina op zijn persconferentie.
"De duur van de respons met CAPTEM is heel lang" aldus Dr Fine. "De langste overlevende patiënt in de CAPTEM studiegroep is nu al 8 jaar verder".
Bijwerkingen:
CAPTEM geeft in vergelijking met andere chemotherapieën voor deze groep van patiënten beduidend minder bijwerkingen. De meest voorkomende graad 3/4 bijwerkingen waren lymfopenie ( 35 % ) , hyperglycemie ( 6 % ) , thrombocytopenie ( 3 % ) , en diarree ( 3 % ) .
Conclusie:
"CAPTEM is de eerste behandeling met een bewezenwerkzaamheid in een breed scala van neuro-endocriene tumoren , waaronder carcinoïdtumoren, welke tot nu toe moeilijk te behandelen zijn." aldus dr. Fine.
Het behandelingsprotocol en fase II studie:
CAPTEM, de combinatie van capecitabine - xeloda en temozolomide - temodal wordt op dit moment onderzocht in een gerandomiseerde placebo gecontroleerde fase 2 studie. Klik hier voor het studieprotocol met e-mailadres en telefoonnummer van contactpersoon.
Er worden nog steeds patiënten aangenomen. Of zij ook patienten aannemen vanuit Europa durf ik niet te zeggen. Probleem is ook wel dat het een gerandomiseerde placebo gecontroleerde studie is (placebo is wel of niet xeloda, dus u kirjgt wel altijd temozolomide - temodal), waardoor als u wordt aangenomen u ook in de placebogroep kan terechtkomen.
Misschien beter uw behandelend arts vragen of u deze aanpak wellicht buiten studieverband kunt krijgen? Capecitabine en temozolomide zijn bekende reeds lang geregistreerde medicijnen, dus misschien wilt uw arts dit wel voorschrijven? Anders zou ik mytomorrows benaderen, misschien willen zij dit dan wel.
Dr Fine en Dr Krishnamurthi hebben verklaard geen relevante financiële belangen te hebben.
Het volledige studierapport: Capecitabine and temozolomide (CAPTEM) for metastatic, well-differentiated neuroendocrine cancers: The Pancreas Center at Columbia University experience opgemaakt maart 2013 is tegen in te zien. Het abstract van deze studie staat hieronder.
Van een andere studie met zelfde aanpak met alvleesklierkanker (NET tumoren) vanuit neuro-endocriene oorsprong en onderdeel van de hierboven beschreven studie is het volledige studierapport: A retrospective study of capecitabine/temozolomide (CAPTEM) regimen in the treatment of metastatic pancreatic neuroendocrine tumors (pNETs) after failing previous therapy wel gratis in te zien.
Het abstract daarvan staat ook hieronder. Referentielijst behorend bij CAPTEM studie staat onderaan dit artikel.
CAPTEM is highly active, well tolerated and may prolong survival in patients with well-differentiated, metastatic NET who have progressed on previous therapies
Capecitabine and temozolomide (CAPTEM) for metastatic, well-differentiated neuroendocrine cancers: The Pancreas Center at Columbia University experience.
Abstract
PURPOSE:
We evaluated the efficacy and safety of capecitabine and temozolomide (CAPTEM) in patients with metastatic neuroendocrine tumors (NETs) to the liver. This regimen was based on our studies with carcinoid cell lines that showed synergistic cytotoxicity with sequence-specific dosing of 5-fluorouracil preceding temozolomide (TMZ).
METHODS:
A retrospective review was conducted of 18 patients with NETs metastatic to the liver who had failed 60 mg/month of Sandostatin LAR™ (100%), chemotherapy (61%), and hepatic chemoembolization (50%). Patients received capecitabine at 600 mg/m(2) orally twice daily on days 1-14 (maximum 1,000 mg orally twice daily) and TMZ 150-200 mg/m(2) divided into two doses daily on days 10-14 of a 28-day cycle. Imaging was performed every 2 cycles, and serum tumor markers were measured every cycle.
RESULTS:
Using RECIST parameters, 1 patient (5.5%) with midgut carcinoid achieved a surgically proven complete pathological response (CR), 10 patients (55.5%) achieved a partial response (PR), and 4 patients (22.2%) had stable disease (SD). Total response rate was 61%, and clinical benefit (responders and SD) was 83.2%. Of four carcinoid cases treated with CAPTEM, there was 1 CR, 1 PR, 1 SD, and 1 progressive disease. Median progression-free survival was 14.0 months (11.3-18.0 months). Median overall survival from diagnosis of liver metastases was 83 months (28-140 months). The only grade 3 toxicity was thrombocytopenia (11%). There were no grade 4 toxicities, hospitalizations, opportunistic infections, febrile neutropenias, or deaths.
CONCLUSIONS:
CAPTEM is highly active, well tolerated and may prolong survival in patients with well-differentiated, metastatic NET who have progressed on previous therapies.
- PMID:
- 23370660
- [PubMed - indexed for MEDLINE]
A Retrospective Study of Capecitabine/Temozolomide (CAPTEM) Regimen in the Treatment of Metastatic Pancreatic Neuroendocrine Tumors (pNETs) after Failing Previous Therapy
JOP. J Pancreas (Online) 2013 Sep 10; 14(5):498-501.
Muhammad Wasif Saif1, Kristin Kaley2, Marianne Brennan2, Marie Carmel Garcon3, Gladys Rodriguez3, Teresa Rodriguez3
1Section of GI Cancers and Experimental Therapeutics, Tufts University School of Medicine. Boston, MA, USA. 2Yale School of Medicine. New Haven, CT, USA. 3Columbia University Medical Center. New York, NY, USA
ABSTRACT
Context Pancreatic neuroendocrine tumors (pNETs) are notoriously resistant to currently available chemotherapy agents. Preclinical data has suggested synergy between temozolomide and capecitabine.
Objective To report a retrospective data on the efficacy and safety of capecitabine and temozolomide (CAPTEM regimen) in patients with metastatic pancreatic neuroendocrine tumors (pNETs) who have failed prior therapies.
Methods We reviewed the medical records of 7 patients with metastatic pNETs who had had progressive cancer prior to treatment despite therapy, including long-acting release octreotide (60 mg/month), chemotherapy and hepatic chemoembolization. Capecitabine was administered at a flat dose of 1,000 mg orally twice daily on days 1-14 and temozolomide 200 mg/m2 was given in two divided doses daily on days 10-14 of a 28-day cycle. Tumor assessments were repeated every two cycles and serum tumor markers were measured every cycle. Response to treatment was assessed using Response Evaluation Criteria in Solid Tumors (RECIST) parameters, and toxicity was graded using the National Cancer Institute Common Terminology Criteria for Adverse Events (CTCAE), version 3.0.
Results Among 7 patients treated, three patients achieved a partial response, and two patients had stable disease. Total response rate was 43%, and clinical benefit (responders and stable disease) was 71%. Median duration of response was 8 months (range: 4-12 months). Grade 3 and 4 toxicities included grade 3 thrombocytopenia in one patient and grade 3 fatigue in one patient. The most common toxicities were grade 1 and 2 neutropenia, grade 1 fatigue, grade 1 and 2 hand-foot syndrome.
Conclusions Our retrospective study showed that modified CAPTEM regimen was well-tolerated and produced comparable response to historical data in neuroendocrine tumors, including pNETs. Our study is unique as it only included patients with pNETs. Further prospective studies are warranted to evaluate the combination of CAPTEM regimen with targeted therapies in pNETs.
References CAPTEM study
References
1. Dimou AT, Syrigos KN and Saif MW. Neuroendocrine tumors of the pancreas: what's new. Highlights from the "2010 ASCO Gastrointestinal Cancers Symposium". Orlando, FL, USA. January 22-24, 2010. JOP. J Pancreas (Online) 2010; 11:135-8. [PMID 20208321]
2. Yao JC, Hassan M, Phan A, Dagohoy C, Leary C, Mares JE, et al. One hundred years after "carcinoid": epidemiology of and prognostic factors for neuroendocrine tumors in 35,825 cases in the United States. J Clin Oncol 2008; 26:3063-72. [PMID 18565894]
3. Stevenson R, Libutti SK, Saif MW. Novel agents in gastroenteropancreatic neuroendocrine tumors. JOP. J Pancreas (Online) 2013; 14:152-4. [PMID 23474560]
4. Oberstein PE, Remotti H, Saif MW, Libutti SK. Pancreatic neuroendocrine tumors: entering a new era. JOP. J Pancreas (Online) 2012; 13:169-73. [PMID 22406593]
5. Cheng PN, Saltz LB. Failure to confirm major objective antitumor activity for streptozocin and doxorubicin in the treatment of patients with advanced islet cell carcinoma. Cancer 1999; 86:944-8. [PMID 10491519]
6. Kulke MH, Stuart K, Enzinger PC, Ryan DP, Clark JW, Muzikansky A, et al. Phase II study of temozolomide and thalidomide in patients with metastatic neuroendocrine tumors. J Clin Oncol 2006; 24: 401-6. [PMID 16421420]
7. Kulke MH, Stuart K, Earle CC, Bhargava P, Clark JW, Enzinger PC, et al. A phase II study of temozolomide and bevacizumab in patients with advanced neuroendocrine tumors. J Clin Oncol 2006; 24(18S): Abstract 4044.
8. Murakami J, Lee YJ, Kokeguchi S, Tsujigiwa H, Asaumi J, Nagatsuka H, et al. Depletion of O6-methylguanine -DNA methyltransferase by O6-benzylguanine enhances 5 -FU cytotoxicity in colon and oral cancer cell lines. Oncol Rep 2007; 17:1461-7. [PMID 17487405]
9. Isacoff WH, Moss RA, Pecora AL, Fine RL. Temozolomide/capecitabine therapy for metastatic neuroendocrine tumors of the pancreas. A retrospective review. J Clin Oncol 2006; 24(18S): Abstract 14023.
10. Strosberg JR, Fine RL, Choi J, Nasir A, Coppola D, Chen DT, et al. First-line chemotherapy with capecitabine and temozolomide in patients with metastatic pancreatic endocrine carcinomas. Cancer 2011; 117:268-75. [PMID 20824724]
11. Julka PK, Doval DC, Gupta S, Rath GK. Response assessment in solid tumours: a comparison of WHO, SWOG and RECIST guidelines. Br J Radiol 2008; 81:444-9. [PMID 18316345]
12. Cancer Therapy Evaluation Program. Common Terminology Criteria for Adverse Events (CTCAE) v4.0. National Cancer Institute at the National Institute of Health: Bethesda, MD, USA.
13. Rinke A, Müller HH, Schade-Brittinger C, Klose KJ, Barth P, Wied M, et al. Placebo-controlled, double-blind, prospective, randomized study on the effect of octreotide LAR in the control of tumor growth in patients with metastatic neuroendocrine midgut tumors: a report from the PROMID Study Group. J Clin Oncol 2009; 27:4656-63. [PMID 19704057]
14. Oberstein PE and Saif MW. Safety and efficacy of everolimus in adult patients with neuroendocrine tumors. Clin Med Insights Oncol 2012; 6:41-51. [PMID 22253554]
15. Yao JC, Shah MH, Ito T, Bohas CL, Wolin EM, Van Cutsem E, et al. Everolimus for advanced pancreatic neuroendocrine tumors. N Engl J Med 2011; 364:514-23. [PMID 21306238]
16. Raymond E, Dahan L, Raoul JL, Bang YJ, Borbath I, Lombard-Bohas C, et al. Sunitinib malate for the treatment of pancreatic neuroendocrine tumors. N Engl J Med 2011; 364:501-13. [PMID 21306237]
Gerelateerde artikelen
- FOLFIRINOX geeft betere overall overleving (9 1/2 vs 6 maanden) dan Gemcitabine plus Nab-Paclitaxel bij inoperabele gevorderde alvleesklierkanker blijkt uit grote studie
- Chemo (oxaliplatin plus gemcitabine) na operatie bij galwegkanker geeft 25 maanden extra overall overleving (50 vs 75 maanden ) maar wordt afgedaan als zou chemo zinloos zijn
- Chemo (irinotecan plus 5-FU/leucovorin ) liposomal - time released toegediend geeft betere overall overleving dan systemische chemo op 1 jaar bij gevorderde alvleesklierkanker
- Chemo met gemcitabine plus S-1 (tegafur/gimeracil/oteracil) vooraf aan operatie bij alvleesklierkanker verbetert overall overleving met 10 maanden (26 vs 36 maanden) in vergelijking met alleen operatie
- mFOLFIRINOX ( oxaliplatin leucovorin irinotecan en 5-fluorouracil - 5-FU) geeft langere mediane ziektevrije tijd en overall overleving (plus 20 maanden) bij alvleesklierkanker en post operatief chemo-bestraling geeft langere ziektevrije tijd
- Capecitabine plus gemcitabine geeft langere mediane overleving op 3,5 jaar in vergelijking met alleen gemcitabine, maar alleen bij patienten zonder uitzaaiingen
- S-1 een oraal in te nemen vorm van chemo zorgt voor spectaculaire verbetering van ziektevrije tijd en kleinere kans op overlijden - 44 procent - bij alvleesklierkanker in vergelijking met gemcitabine bij Japanese patiënten
- CAPTEM een combinatie van Xeloda - capecitabine met temozolomide - temodal zorgt voor spectaculaire resultaten (97% minimaal stabiele ziekte) bij patiënten met alvleesklierkanker (NET3), carcinoid, schildkliertumoren en hypofyse tumoren copy 1
- NAB-paclitaxel - Abraxane - in combinatie met gemcitabine verbetert significant mediane overleving voor uitgezaaide alvleesklierkanker en is nu door FDA goedgekeurd
- Lymfopenie - te lage waarden van de lymfocyten - veroorzaakt door chemo en bestraling geeft significant kortere overlevingstijd 14 vs 20 maanden voor mensen met operabele alvleesklierkanker
- Chemo plus bestraling vooraf en na operatie bij alvleesklierkanker na meta analyse van vijf grote gerandomiseerde studies geeft negatieve uitkomst voor operabele alvleesklierkankerpatiënten.
- Chemo plus bestraling - chemoradiation vooraf en na operatie bij alvleesklierkanker na meta analyse van vijf grote gerandomiseerde studies geeft negatieve uitkomst op overlevingscijfers voor operabele alvleesklierkanker
- Gemcitabine plus combinatie FOLFIRINOX (5-fluorouracil, leucovorin, irinotecan, en oxaliplatine) geeft significant mediaan langere overlevingstijd voor patienten met uitgezaaide alvleesklierkanker.
- Gemcitabine t.o. combinatie FOLFIRINOX (5-fluorouracil, leucovorin, irinotecan, en oxaliplatine) geeft geen enkele meerwaarde op ziektevrije tijd en overall overleving bij operabele alvleesklierkanker.
- Gemzar en Xeloda als combinatie behandeling zou mediane overlevingstijd van alvleesklierkankerpatiënten met 1,5 maand verlengen - van 6 maanden naar 7,4 maanden - jubelen de media na fase III studie resultaten.
- Gemzar verpakt en toegediend in speciaal geprepareerde vetbolletjes - cationic liposomen ( EndoTAG-1) verdubbelt bijna overlevingstijd (van 7,2 naar 13,6 maanden mediaan) van inoperabele alvleesklierkankerpatienten
- Chemo en effect bij alvleesklierkanker: Chemo (5-FU en cisplatin) vooraf aan bestraling bij alvleesklierkanker stadium I tot III geeft geen effect op overall overleving en slechts iets betere lokale controle.
- Chemo aangevuld met Cox-2 remmer zorgt voor geen enkel positief effect bij inoperabele alvleesklierkankerpatiënten. Mediane overall overleving bedroeg slechts 5,8 maanden plus ernstige bijwerkingen.
- Thalidomide zorgt voor tegengaan van gewichtsverlies bij vergevorderde alvleesklierkankerpatiënten blijkt uit gerandomiseerde placebo gecontroleerde studie.
- Chemo: een overzicht van recente ontwikkelingen en belangrijke studies over chemo en radiotherapie - bestraling



Plaats een reactie ...
Reageer op "CAPTEM een combinatie van Xeloda - capecitabine met temozolomide - temodal zorgt voor spectaculaire resultaten (97% minimaal stabiele ziekte) bij patiënten met alvleesklierkanker (NET3), carcinoid, schildkliertumoren en hypofyse tumoren copy 1"