Raadpleeg ook literatuurlijst niet-toxische middelen en behandelingen specifiek bij borstkanker van arts-bioloog drs. Engelbert Valstar
7 augustus 2019: Lees ook dit artikel:
31 oktober 2015: Bron: Immunotherapy. 2013 Nov;5(11):1177-82. doi: 10.2217/imt.13.126
Ook na 15 jaar follow-up is duidelijk dat immuuntherapie met het mannan-MCU1 veel betere overleving en langere ziektevrije tijd na operatie van beginnende borstkanker geeft. Zie ook onderstaand artikel.
Nu is na 12 tot 15 jaar follow-up geconstateerd dat bij een kleinschalige maar wel gerandomiseerde studie met totaal 31 patienten met beginnende borstkanker de verschillen in wel of geen recidief erg groot zijn: 60% (placebogroep) versus 12,5% (immuuntherapiegroep) kans op een recidief na 12 - 15 jaar follow-up.
Studieresultaten:
- Bij patiënten uit de placebogroep kregen er 9 van de 15 een recidief (60%). Uit de groep van 16 patiënten die de immuuntherapie volgden kregen er slechts 2 een recidief (12,5%)
- De tijd tot zich een recidief voordeed in de placebogroep na de operatie varieerde van 7 tot 180 maanden (gemiddeld: 65.8 maanden) en bij de twee patiënten uit de immuungroep was deze respectievelijk 95 maanden en 141 maanden (gemiddeld: 118 maanden) na operatie.
- Deze resutlaten zijn statistisch significant (p = 0.02 voor overleving en p = 0.009 voor patiënten die kankervrij waren.
- Alle patiënten geïnjecteerd met Mannan-FP vertoonden geen enkele vorm van toxiciteit, geen bijwerkingen dus, noch van auto immuunreacties tijdens de studieduur.
Het is toch eigenlijk ongelooflijk dat zo'n studie 15 jaar moet duren (20 jaar nadat de eerste studie met mannan-MUC1 startte en dat de onderzoekers nog steeds weer vragen om een grotere placebo gecontroleerde fase III studie. Ik vind dit echt schandalig.
Als u dit studierapport leest: Recent advances in the development of breast cancer vaccines. ziet u dat immuuntherapie met vaccins, inclusief herceptin enz. echt veel betere resultaten geeft bij borstkanker. Althans bij borstkanker in beginnend stadium en/of met kleine tumorload.
Onderaan staat het abstract van de studie evaluatie met de Mannan-MUC1 : Up to 15-year clinical follow-up of a pilot Phase III immunotherapy study in stage II breast cancer patients using oxidized mannan-MUC1. Voor het volledige studierapport moet worden betaald.
Zie ook hieronder meer over immuuntherapie met het mannan-MUC1
13 augustus 2011: zoekend naar vervolgstudies met mannan MUC1, een vorm van immuuntherapie bij o.a. borstkanker, maar ook bij andere vormen van kanker succesvol ingezet kom ik nog steeds alleen onderstaande Griekse gerandomiseerde fase III studie tegen bij patiënten. Onderaan heb ik een referentielijst toegevoegd van studies met mucins. als u op de volgende link klikt
kunt u vrij het volledige studierapport uit onderstaand artikel lezen.
Als u hier klikt kunt u een zeer uitgebreid artikel in Medscape lezen over deze aanpak met mannan MUC1. Ook in dit artikel zijn de meningen bijzonder positiief.
This study provides important justification for studies of immunotherapeutic studies in patients with early/minimal/no evidence of disease. It also suggests that M-FP confers some benefit. A larger trial is now in progress (multicentre trial to include >360 patients), which will yield further data
In het artikel van Medscape wordt ook geschreven dat er een grote fase III studie zou worden gestart maar ik kan die tot nu toe nergens vinden. Onderaan een referentielijst van andere studies.
27 september 2006: Bron: Breast Cancer Res. 2006; 8(3): R27. Published online 2006 June 15. doi: 10.1186/bcr1505. Copyright © 2006 Apostolopoulos et al.; licensee BioMed Central Ltd.
Met dank aan MB die ons deze studie opstuurde. Immuuntherapie tegen MUC1 met injecties van oxidized mannan-MUC1 geeft een 100% resultaat (statistisch significant = P = 0.0292) in het voorkomen van een recidief binnen vijf jaar bij vrouwen met borstkanker stadium II die daaraan eerder succesvol zijn behandeld. Hier een zo goed als letterlijke vertaling van het abstract van de dubbelblinde gerandomiseerde fase studie.
Methode
In een dubbelblinde gerandomiseerde studie, werden 31 patienten met stadium II borstkanker en met geen aanwijsbare ziekte op moment van start van de behandeling behandeld met ofwel een injectie met een placebo of een injectie met oxidized mannan-MUC1, om een immmuunreactie te bewerkstelligen tegen MUC1 en een recidief van kanker en/of uitzaaiingen te voorkomen. 28 patienten ontvingen ofwel de placebo of de volledige injectie met oxidized mannan-MUC1. Overleving en immunologische reactie werden onderzocht.
Resultaten
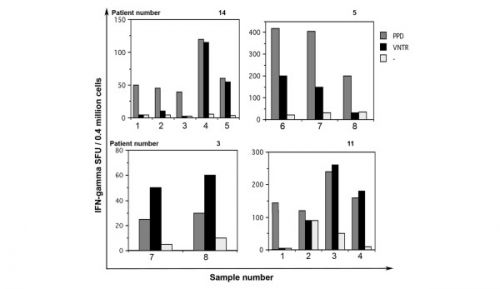
Na meer dan 5.5 jaar was verstreken sinds de laatste patiënt de behandeling was gestart (8.5 jaar nadat de eerste patient was gestart met de behandeling) het recidiefcijfer in de groep patienten welke een placebo hadden gekregen was 27% (4 uit 15 patiënten; is conform het verwachte cijfer op basis van statistische gegegens voor een recidief bij borstkanker stadium II); in de groep patiënten welke de immuuntherapie hadden gekregen kreeg geen enkele patiënt een recidief (0 uit 16 patiënten), en deze uitkomst is statistisch significant (P = 0.0292). Van de patiënten die oxidized mannan-MUC1 kregen hadden 9 ervan meetbare antibodies tegen MUC1 en vier van de tien hadden MUC1-specifieke T cell reacties; geen enkele patiënt uit de placebogroep toonde een immunologische reactie tegen MUC1.
Conclusie
De resultaten suggereren dat bij vroeg gediagnosteerde borstkanker (stadium I en II) MUC1 immunotherapie uitstekend werkt en een grotere Fase III studie zal moeten worden opgezet.
Pilot phase III immunotherapy study in early-stage breast cancer patients using oxidized mannan-MUC1 Vasso Apostolopoulos,1 Geoffrey A Pietersz,1 Anastasios Tsibanis,2 Annivas Tsikkinis,2 Heleni Drakaki,2 Bruce E Loveland,1 Sara J Piddlesden,1 Magdalena Plebanski,1 Dodie S Pouniotis,1 Michael N Alexis,3 Ian F McKenzie,1 and Stamatis Vassilaros2
1Immunology and Vaccine Laboratory, Burnet Institute at Austin, Heidelberg, Victoria, Australia 2Prolipsis Medical Center, Athens, Greece
3Institute of Biological Research and Biotechnology, The National Hellenic Research Foundation, Athens, Greece
Corresponding author.
Vasso Apostolopoulos: vasso@burnet.edu.au; Geoffrey A Pietersz: g.pietersz@burnet.edu.au; Anastasios Tsibanis: helaca@hol.gr; Annivas Tsikkinis: helaca@hol.gr; Heleni Drakaki: helaca@hol.gr; Bruce E Loveland: b.loveland@ari.unimelb.edu.au; Magdalena Plebanski: mplebans@ari.unimelb.edu.au; Dodie S Pouniotis: d.pouniotis@ari.unimelb.edu.au; Michael N Alexis: mnalexis@eie.gr; Ian F McKenzie: i.mckenzie@ari.unimelb.edu.au; Stamatis Vassilaros: helaca@hol.gr
Received March 24, 2006; Revisions requested May 11, 2006; Revised May 15, 2006; Accepted May 25, 2006.
This is an open access article distributed under the terms of the Creative Commons Attribution License (http://creativecommons.org/licenses/by/2.0), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Introduction
Mucin 1 (MUC1) is a high molecular weight glycoprotein overexpressed on adenocarcinoma cells and is a target for immunotherapy protocols. To date, clinical trials against MUC1 have included advanced cancer patients. Herein, we report a trial using early stage breast cancer patients and injection of oxidized mannan-MUC1.
Method
In a randomized, double-blind study, 31 patients with stage II breast cancer and with no evidence of disease received subcutaneous injections of either placebo or oxidized mannan-MUC1, to immunize against MUC1 and prevent cancer reoccurrence/metastases. Twenty-eight patients received the full course of injections of either oxidized mannan-MUC1 or placebo. Survival and immunological assays were assessed.
Results
After more than 5.5 years had elapsed since the last patient began treatment (8.5 years from the start of treatment of the first patient), the recurrence rate in patients receiving the placebo was 27% (4/15; the expected rate of recurrence in stage II breast cancer); those receiving immunotherapy had no recurrences (0/16), and this finding was statistically significant (P = 0.0292). Of the patients receiving oxidized mannan-MUC1, nine out of 13 had measurable antibodies to MUC1 and four out of 10 had MUC1-specific T cell responses; none of the placebo-treated patients exhibited an immune response to MUC1.
Conclusion
The results suggest that, in early breast cancer, MUC1 immunotherapy is beneficial, and that a larger phase III study should be undertaken.
References oxidized mannan MUC1
- Pietersz GA, Apostolopoulos V, McKenzie IF: Generation of cellular immune responses to antigenic tumor peptides. Cell Mol Life Sci 2000, 57:290-310
- Gendler S, Taylor-Papadimitriou J, Duhig T, Rothbard J, Burchell J: A highly immunogenic region of a human polymorphic epithelial mucin expressed by carcinomas is made up of tandem repeats. J Biol Chem 1988, 263:12820-12823
- Xing PX, Reynolds K, Tjandra JJ, Tang XL, McKenzie IF: Synthetic peptides reactive with anti-human milk fat globule membrane monoclonal antibodies. Cancer Res 1990, 50:89-96
- Xing PX, Tjandra JJ, Stacker SA, Teh JG, Thompson CH, McLaughlin PJ, McKenzie IF: Monoclonal antibodies reactive with mucin expressed in breast cancer. Immunol Cell Biol 1989, 67:183-195
- Barnd DL, Lan MS, Metzgar RS, Finn OJ: Specific, major histocompatibility complex-unrestricted recognition of tumorassociated mucins by human cytotoxic T cells. Proc Natl Acad Sci USA 1989, 86:7159-7163
- Ioannides CG, Fisk B, Jerome KR, Irimura T, Wharton JT, Finn OJ: Cytotoxic T cells from ovarian malignant tumors can recognize polymorphic epithelial mucin core peptides. J Immunol 1993, 151:3693-3703
- Jerome KR, Domenech N, Finn OJ: Tumor-specific cytotoxic T cell clones from patients with breast and pancreatic adenocarcinoma recognize EBV-immortalized B cells transfected with polymorphic epithelial mucin complementary DNA. J Immunol 1993, 151:1654-1662
- Agrawal B, Reddish MA, Longenecker BM: In vitro induction of MUC-1 peptide-specific type 1 T lymphocyte and cytotoxic T lymphocyte responses from healthy multiparous donors. J Immunol 1996, 157:2089-2095
- Apostolopoulos V, Loveland BE, Pietersz GA, McKenzie IF: CTL in mice immunized with human mucin 1 are MHC-restricted. J Immunol 1995, 155:5089-5094
- Domenech N, Henderson RA, Finn OJ: Identification of an HLAA11- restricted epitope from the tandem repeat domain of the epithelial tumor antigen mucin. J Immunol 1995, 155:4766-4774
- Kotera Y, Fontenot JD, Pecher G, Metzgar RS, Finn OJ: Humoral immunity against a tandem repeat epitope of human mucin MUC-1 in sera from breast, pancreatic, and colon cancer patients. Cancer Res 1994, 54:2856-2860
- Rughetti A, Turchi V, Ghetti CA, Scambia G, Panici PB, Roncucci G, Mancuso S, Frati L, Nuti M: Human B-cell immune response to the polymorphic epithelial mucin. Cancer Res 1993, 53:2457-2459
- von Mensdorff-Pouilly S, Gourevitch MM, Kenemans P, Verstraeten AA, Litvinov SV, van Kamp GJ, Meijer S, Vermorken J, Hilgers J: Humoral immune response to polymorphic epithelial mucin (MUC-1) in patients with benign and malignant breast tumours. Eur J Cancer 1996, 32A:1325-1331
- Gourevitch MM, von Mensdorff-Pouilly S, Litvinov SV, Kenemans P, van Kamp GJ, Verstraeten AA, Hilgers J: Polymorphic epithelial mucin (MUC-1)-containing circulating immune complexes in carcinoma patients. Br J Cancer 1995, 72:934-938
- Acres B, Apostolopoulos V, Balloul JM, Wreschner D, Xing PX, Ali- Hadji D, Bizouarne N, Kieny MP, McKenzie IF: MUC1-specific immune responses in human MUC1 transgenic mice immunized with various human MUC1 vaccines. Cancer Immunol Immunother 2000, 48:588-594
- Apostolopoulos V, Barnes N, Pietersz GA, McKenzie IF: Ex vivo targeting of the macrophage mannose receptor generates anti-tumor CTL responses. Vaccine 2000, 18:3174-3184
- Apostolopoulos V, Haurum JS, McKenzie IF: MUC1 peptide epitopes associated with five different H-2 class I molecules. Eur J Immunol 1997, 27:2579-2587
- Apostolopoulos V, Pietersz GA, Gordon S, Martinez-Pomares L, McKenzie IF: Aldehyde-mannan antigen complexes target the MHC class I antigen-presentation pathway. Eur J Immunol 2000, 30:1714-1723
- Apostolopoulos V, Pietersz GA, Loveland BE, Sandrin MS, McKenzie IF: Oxidative/reductive conjugation of mannan to antigen selects for T1 or T2 immune responses. Proc Natl Acad Sci USA 1995, 92:10128-10132
- Apostolopoulos V, Pietersz GA, McKenzie IF: Cell-mediated immune responses to MUC1 fusion protein coupled to mannan. Vaccine 1996, 14:930-938
- Apostolopoulos V, Yu M, Corper AL, Teyton L, Pietersz GA, McKenzie IF, Wilson IA, Plebanski M: Crystal structure of a noncanonical low-affinity peptide complexed with MHC class I: a new approach for vaccine design. J Mol Biol 2002, 318:1293-1305
- Apostolopoulos V, Yuriev E, Ramsland PA, Halton J, Osinski C, Li W, Plebanski M, Paulsen H, McKenzie IF: A glycopeptide in complex with MHC class I uses the GalNAc residue as an anchor. Proc Natl Acad Sci USA 2003, 100:15029-15034
- Apostolopoulos V, Karanikas V, Haurum JS, McKenzie IF: Induction of HLA-A2-restricted CTLs to the mucin 1 human breast cancer antigen. J Immunol 1997, 159:5211-5218
- Apostolopoulos V, McKenzie IF: Role of the mannose receptor in the immune response. Curr Mol Med 2001, 1:469-474
- Apostolopoulos V, McKenzie IF, Pietersz GA: Generation of MUC1 cytotoxic T-cells in mice and epitope mapping. Methods Mol Biol 2000, 125:455-462
- Apostolopoulos V, Pietersz GA, McKenzie IF: MUC1 and breast cancer. Curr Opin Mol Ther 1999, 1:98-103
- Apostolopoulos V, Popovski V, McKenzie IF: Cyclophosphamide enhances the CTL precursor frequency in mice immunized with MUC1-mannan fusion protein (M-FP). J Immunother 1998, 21:109-113
- Apostolopoulos V, Xing PX, McKenzie IF: Murine immune response to cells transfected with human MUC1: immunization with cellular and synthetic antigens. Cancer Res 1994, 54:5186-5193
- Lees CJ, Apostolopoulos V, Acres B, Ong CS, Popovski V, McKenzie IF: The effect of T1 and T2 cytokines on the cytotoxic T cell response to mannan-MUC1. Cancer Immunol Immunother 2000, 48:644-652
- Lees CJ, Apostolopoulos V, Acres B, Ramshaw I, Ramsay A, Ong CS, McKenzie IF: Immunotherapy with mannan-MUC1 and IL- 12 in MUC1 transgenic mice. Vaccine 2000, 19:158-162
- Lees CJ, Apostolopoulos V, McKenzie IF: Cytokine production from murine CD4 and CD8 cells after mannan-MUC1 immunization. J Interferon Cytokine Res 1999, 19:1373-1379
- Lofthouse SA, Apostolopoulos V, Pietersz GA, Li W, McKenzie IF: Induction of T1 (cytotoxic lymphocyte) and/or T2 (antibody) responses to a mucin-1 tumour antigen. Vaccine 1997, 15:1586-1593
- McKenzie IF, Apostolopoulos V, Lees C, Xing PX, Lofthouse S, Osinski C, Popovski V, Acres B, Pietersz G: Oxidised mannan antigen conjugates preferentially stimulate T1 type immune responses. Vet Immunol Immunopathol 1998, 63:185-190
- Pietersz GA, Li W, Osinski C, Apostolopoulos V, McKenzie IF: Definition of MHC-restricted CTL epitopes from non-variable number of tandem repeat sequence of MUC1. Vaccine 2000, 18:2059-2071
- Pietersz GA, Li W, Popovski V, Caruana JA, Apostolopoulos V, McKenzie IF: Parameters for using mannan-MUC1 fusion protein to induce cellular immunity. Cancer Immunol Immunother 1998, 45:321-326
- Karanikas V, Hwang LA, Pearson J, Ong CS, Apostolopoulos V, Vaughan H, Xing PX, Jamieson G, Pietersz G, Tait B, et al.: Antibody and T cell responses of patients with adenocarcinoma immunized with mannan-MUC1 fusion protein. J Clin Invest 1997, 100:2783-2792
- Karanikas V, Lodding J, Maino VC, McKenzie IF: Flow cytometric measurement of intracellular cytokines detects immune responses in MUC1 immunotherapy. Clin Cancer Res 2000, 6:829-837
- Karanikas V, Thynne G, Mitchell P, Ong CS, Gunawardana D, Blum R, Pearson J, Lodding J, Pietersz G, Broadbent R, et al.: Mannan mucin-1 peptide immunization: influence of cyclophosphamide and the route of injection. J Immunother 2001, 24:172-183
- Xing PX, Michael M, Apostolopoulos V, Prenzoska J, Marshall C, Bishop J, McKenzie IF: Phase I study of synthetic MUC1 peptides in breast cancer. Int J Oncol 1995, 6:1283-1289
- Apostolopoulos V, Xing PX, Trapani JA, McKenzie IF: Production of anti-breast cancer monoclonal antibodies using a glutathione-S-transferase-MUC1 bacterial fusion protein. Br J Cancer 1993, 67:713-720
- Loveland BE, Zhao A, White S, Gan H, Hamilton K, Xing PX, Pietersz GA, Apostolopoulos V, Vaughan H, Karanikas V, et al.: Mannan- MUC1 pulsed dendritic cell immunotherapy: a phase I trial in patients with adenocarcinoma. Clin Cancer Res 2006, 12:869-877
- Graphpad Software [http://www.graphpad.com/]
- Gruber R, van Haarlem LJ, Warnaar SO, Holz E, Riethmuller G: The human antimouse immunoglobulin response and the anti-idiotypic network have no influence on clinical outcome in patients with minimal residual colorectal cancer treated with monoclonal antibody CO17-1A. Cancer Res 2000, 60:1921-1926
- Davis ID, Chen W, Jackson H, Parente P, Shackleton M, Hopkins W, Chen Q, Dimopoulos N, Luke T, Murphy R, et al.: Recombinant NY-ESO-1 protein with ISCOMATRIX adjuvant induces broad integrated antibody and CD4+ and CD8+ T cell responses in humans. Proc Natl Acad Sci USA 2004, 101:10697-10702
- Rentzsch C, Kayser S, Stumm S, Watermann I, Walter S, Stevanovic S, Wallwiener D, Guckel B: Evaluation of pre-existent immunity in patients with primary breast cancer: molecular and cellular assays to quantify antigen-specific T lymphocytes in peripheral blood mononuclear cells. Clin Cancer Res 2003, 9:4376-4386
- Hirasawa Y, Kohno N, Yokoyama A, Kondo K, Hiwada K, Miyake M: Natural autoantibody to MUC1 is a prognostic indicator for non-small cell lung cancer. Am J Respir Crit Care Med 2000, 161:589-594
- von Mensdorff-Pouilly S, Verstraeten AA, Kenemans P, Snijdewint FG, Kok A, Van Kamp GJ, Paul MA, Van Diest PJ, Meijer S, Hilgers J: Survival in early breast cancer patients is favorably influenced by a natural humoral immune response to polymorphic epithelial mucin. J Clin Oncol 2000, 18:574-583.
Gerelateerde artikelen
- HER2-vaccinatie in combinatie met een anti-CD27 monoklonaal antilichaam + anti-PD-1 mAb-behandeling houdt alle patienten met uitgezaaide borstkanker in laatste stadium van hun leven al 18 jaar in leven
- Borstkankerpatiente en wetenschapster Beate Halassy maakte in haar eigen laboratorium twee oncolytische virussen en behandelde zichzelf daarmee succesvol in 2020.
- Pembrolizumab geeft betere overall overleving op 5 jaar voor patienten met beginnende niet uitgezaaide borstkanker in vergelijking met chemotherapie en placebo
- Pertuzumab plus trastuzumab geeft zelfde 2 jaars overall overleving met of zonder chemotherapie bij patienten met uitgezaaide borstkanker met Her2 positief
- Pertuzumab - Perjeta door FDA goedgekeurd als eerstelijns behandeling immuuntherapie bij operabele borstkanker HER-2 positief na uitstekende resultaten uit fase 3 APHINITY studie
- Stereotactische lichaamsbestraling plus plaatselijke injectie met valacyclovir een medicijn tegen herpesvirus plus pembrolizumab geeft verdubbeling van overall overleving bij zwaar voorbehandelde patienten met uitgezaaide triple negatieve borstkanker.
- Immuuntherapie met combinatiebehandeling van nivolumab en ipilimumab zou voor patienten met zogeheten metaplastische borstkanker een behandelingsoptie kunnen zijn blijkt uit kleinschalige studie
- Atezolizumab + nab-paclitaxel chemotherapie als eerstelijns behandeling voor triple negatieve borstkanker met PD-L1-positieve expressie geeft uitstekende resultaten op overall overleving met 10 maanden meer
- HER2-peptidevaccins, GP2 en AE37, lijken bij borstkankerpatiënten goede opties om een recidief te voorkomen.
- FDA verleent versnelde goedkeuring aan pembrolizumab voor lokaal terugkerende inoperabele of uitgezaaide triple-negatieve borstkanker
- Durvalumab met Olaparib en Paclitaxel geeft 17 procent betere complete remissies in vergelijking met alleen chemo bij vrouwen met borstkanker stadium II / III hoog risico, maar ook bij HER2 positief en triple negatief copy 1
- sTILs - tumor infiltrating lymphocytes aanwezig na chemo in beginnende borstkanker triple negatief voorspellen aanslaan van behandeling en geeft superieure overall overleving op drie jaar
- Vrouw met uitgezaaide hormoongevoelige borstkanker (HR-pos) komt in een duurzame complete remissie met immuuntherapie met anti-PD medicijn en TIL - tumor Infiltrating lymfocyten gericht op 4 specifieke mutaties copy 1
- ASCO 2017: I-SPY 2 Trial: Combination of Pembrolizumab Plus Standard Neoadjuvant Therapy in High-Risk Breast Cancer
- Immuuntherapie voor borstkanker in alle stadia maar ook als preventie in eerstelijns en tweede lijns voor borstkanker komt steeds dichterbij. Aldus Elizabeth A. Mittendorf, MD, PhD copy 1
- Immuuntherapie tegen borstkanker (MUC1) met injecties van oxidized mannan-MUC1 geeft een 100% resultaat in het voorkomen van een recidief binnen vijf jaar bij vrouwen met borstkanker stadium II
- Nivolumab: Immuuntherapie in fase II studie voor patienten met triple negatieve borstkanker met nivolumab gestart in Antoni van Leeuwenhoek ziekenhuis per 3 september 2015. copy 1
- Vaccin GP2 naast herceptin geeft significant betere resultaten na 3 jaar dan alleen herceptin bij Her2 positieve borstkanker
- Olaparib plus cedinarib lijkt doorbraak bij controle van vergevorderde eierstokkanker en verdubbelt progressievrije overleving van 9,2 maanden naar 17,7 maanden copy 1
- Gc-MAF een vitamine D verbindend eiwit werkt uiterst effectief (100% genezing bij totaal 8 borstkankerpatienten) als vernietiging en bescherming tegen terugkeer van borstkanker.
- Immuuntherapie: Nieuw vaccin - AE37 - gericht op HER2 expressie lijkt een recidief van borstkanker te kunnen voorkomen bij ruim de helft van de borstkankerpatiënten
- Immuuntherapie met donor natural T-killer cells doodt ook chemo resistente borstkankercellen - tumorstamcellen - en werkt volledig genezend toont een Nederlandse dierstudie aan
- Immuuntherapie met Her2-Neu peptides zorgt voor significant minder recidieven en beduidend minder overlijden bij borstkankerpatienten. 12,5% t.o. 41,7%.
- Immuuntherapie met injecties van MUC1 bij vrouwen met erfelijke BRCA1 of BRCA2 mutaties kan kans op ontwikkeling van borstkanker significant verkleinen. Aldus een gerandomiseerde studie uitgevoerd in de VU Amsterdam.
- Immuuntherapie bij borstkanker, een overzicht



Plaats een reactie ...
Reageer op "Immuuntherapie tegen borstkanker (MUC1) met injecties van oxidized mannan-MUC1 geeft een 100% resultaat in het voorkomen van een recidief binnen vijf jaar bij vrouwen met borstkanker stadium II"