Mocht u kanker-actueel de moeite waard vinden en ons willen ondersteunen om kanker-actueel online te houden dan kunt u ons machtigen voor een periodieke donatie via donaties: https://kanker-actueel.nl/NL/donaties.html of doneer al of niet anoniem op - rekeningnummer NL79 RABO 0372931138 t.n.v. Stichting Gezondheid Actueel in Amersfoort. Onze IBANcode is NL79 RABO 0372 9311 38
Elk bedrag is welkom. En we zijn een ANBI instelling dus uw donatie of gift is in principe aftrekbaar voor de belasting.
En als donateur kunt u ook korting krijgen bij verschillende bedrijven:
20 mei 2016: Lees ook dit artikel:
20 mei 2016: Bron: ASCO 2016
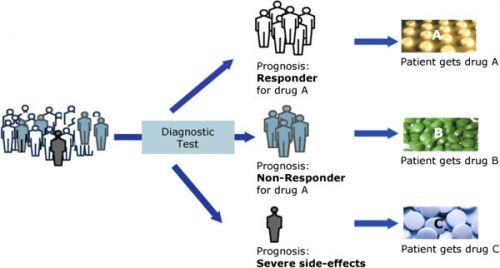
Wanneer bij kankerpatienten een biomoleculair onderzoek (receptoren- en mutatieonderzoek) wordt gedaan voor ze deelnemen aan een fase I onderzoek naar personalised medicine dan zijn de resultaten daarvan veel beter dan wanneer er geen biomoleculair onderzoek plaatsvindt vooraf aan de studiedeelname.
De response cijfers - vermindering van omvang en aantal van tumoren uit de twee vergeleken groepen (wel of geen biomoleculair onderzoek), blijkt gemiddeld 30.6% vs 4.9%, P < .0001 en de progressievrije tijd - PFS blijkt 5.7 maanden vs 2.95 maanden, P = .0002 respectievelijk.
Dr Schwaederle en collegas analyseerden en vergeleken de resultaten uit 346 fase 1 studies wereldwijd gepubliceerd tussen 1 januari 2011 en 31 december 2013. In 58 studies werden personalised medicine gebruikt aan de hand van een biomoleculair onderzoek tegenover 293 studies waarin geen biomoleculair onderzoek (biomarkers) werd gebruikt. Let wel in deze fase I studies worden voornamelijk kankerpatienten opgenomen die zwaar zijn voorbehandeld en met vergevorderde ziekte.
De onderzoekers vergeleken responsecijfers (n = 351 groepen; 13,203 patienten), progressie-vrije overleving (PFS) (n = 45 groepen; 1700 patienten), en overlijden gerelateerd aan de behandeling (n = 351 groepen, 13,203 patienten) tussen de twee studieopzetten (personalised medicine via biomoleculair onderzoek versus algemeen experimenteel onderzoek).
Overall overleving kon niet mee worden genomen in de analyse omdat er te weinig studies waren die dit ook als doel hadden - 27 studies waarvan er slechts 4 met een personalised medicine en een biomoleculair onderzoek.
In de meeste studies werd een vorm van targeted therapy gebruikt (98.3%), maar in de meeste studies daarvan werd geen personalised medicine aanpak of een biomoleculair onderzoek gebruikt (76%).
De studies met personalised medcine die ook een biomoleculair onderzoek (DNA mutatieonderzoek op basis van een eiwit) gebruikten, boekten duidelijk betere resultaten op respons (42% vs 22.4%, P = .001).
Mediaan behandelingsgerelateerd overlijden verschilde statistisch niet significant tussen de twee groepen: (1.89% vs 2.27%, P = 0.31).
"Een van de sterke punten van deze studie is dat het een meta analyse is van alle vormen van studies. En de onderzoekers hebben gekeken naar het gebruik van personalised medicine en biomoleculair onderzoek in een breed perspectief en naar meerdere indicaties, aldus Don S. Dizon, MD, FACP, woordvoerder van ASCO en moderator van de perscast op ASCO 2016.
"Dis is een belangrijke studie met een grote database aan gegevens van meer dan 13.000 patienten in fase I studies. "Personalised medicine is niet de toekomst maar het heden van de oncologische zorg, zegt dr. Dizon.
Het abstract van de studie: Impact of precision medicine in refractory malignancies: A meta-analysis of 13,203 patients in phase I clinical trials wordt op 6 juni 2016 gepresenteerd op ASCO 2016.
Hieronder dat abstract:
Analysis of phase I studies revealed that a personalized strategy was an independent predictor of improved outcomes (RR and PFS). In addition, studies that used targeted agents without a biomarker-based selection strategy had negligible response rates.
Impact of precision medicine in refractory malignancies: A meta-analysis of 13,203 patients in phase I clinical trials.
Sub-category:
Molecular Diagnostics and Imaging
Category:
Tumor Biology
Meeting:
2016 ASCO Annual Meeting
Abstract No:
11520
Poster Board Number:
Poster Discussion Session (Board #217)
Citation:
J Clin Oncol 34, 2016 (suppl; abstr 11520)
Author(s): Maria Clemence Schwaederle, Melissa M. Zhao, J. Jack Lee, Vladimir Lazar, Brian Leyland-Jones, Richard L. Schilsky, John Mendelsohn, Razelle Kurzrock; Center for Personalized Cancer Therapy and Division of Hematology and Oncology, University of California, San Diego, CA; Center for Personalized Cancer Therapy and Division of Hematology and Oncology, University of California, La Jolla, La Jolla, CA; Department of Biostatistics, University of Texas MD Anderson Cancer Center, Houston, TX; Worldwide Innovative Network for Personalized Cancer Therapy (WIN Consortium), Paris, France; Avera Cancer Institute, Sioux Falls, SD; American Society of Clinical Oncology, Alexandria, VA; Sheikh Khalifa Bin Zayed Al Nahyan Institute for Personalized Cancer Therapy, Department of Genomic Medicine, The University of Texas MD Anderson Cancer Center, Houston, TX; University of California, San Diego, La Jolla, CA
Background: Our goal was to compare patient outcomes between phase I studies of single agents that employed a personalized approach (defined as a biomarker-based selection strategy) versus those that did not.
Methods: This analysis included 346 published phase I trials (351 arms) (January 1, 2011 to December 31, 2013; PubMed search). Meta-analysis and weighted pooled analysis were performed. Response rate (RR) (N = 351 arms; 13,203 patients), progression-free survival (PFS) (N = 45 arms; 1,700 patients), and toxic death rate (N = 351 arms, 13,203 patients) were compared for treatment arms that used a personalized strategy versus those that did not. Survival could not be analyzed (data provided in only 27 of 346 studies (N = 4 were personalized studies)).
Results: Multivariable analysis (meta-regression and weighted multiple regression models) demonstrated that the personalized approach independently correlated with improved RR (30.6% vs 4.9%, P<0.0001) as well as prolonged median PFS (5.7 vs 2.95 months, P=0.0002). While most of the personalized arms (98.3%) used targeted agents, the majority of the arms employing targeted agents used a non-personalized approach, i.e., did not select patients using a cognate biomarker (76%). A sub-analysis within targeted arms (N = 234 arms) showed that those using a biomarker-based strategy had statistically improved RR compared to targeted arms that lacked a biomarker-based approach (31.1% vs 5.1%, P<0.0001). In addition, non-personalized targeted arms had comparable outcomes with arms that tested a cytotoxic agent: median RR 5.1% vs 4.7%, P = 0.63; respectively; median PFS 3.3 vs 2.5 months, P = 0.22. Personalized arms using a “genomic (DNA) biomarker” had higher RR than those using a “protein biomarker” (42% vs 22.4%, P = 0.001). Finally, the median treatment-related mortality was not statistically different for arms that employed a personalized strategy versus not (1.89% vs 2.27%, P=0.31).
Conclusions: Analysis of phase I studies revealed that a personalized strategy was an independent predictor of improved outcomes (RR and PFS). In addition, studies that used targeted agents without a biomarker-based selection strategy had negligible response rates.
Gerelateerde artikelen
- 6 nieuwe doorbraken in de strijd tegen kanker worden gepresenteerd door het World Economic Forum met bijbehorende video
- 90 procent van mensen met uitgezaaide kanker heeft meerdere DNA afwijkingen. Slechts 5 procent kreeg ook optimale behandeling daarvoor.
- Antibiotica binnen een maand vooraf aan immuuntherapie met anti-PD medicijnen geeft veel slechtere resultaten op overall overleving dan zonder antibiotica bij verschillende vormen van primaire kanker.
- Anti-PD medicijnen zoals nivolumab, Pembrolizumab en atezolizumab gegeven als immuuntherapie geven zeer goede resultaten bij verschillende vormen van kanker met solide tumoren, zelfs zonder Ligand-1 receptorstatus copy 1
- Bacterien in uitzaaiingen van kankerpatienten zijn door Nederlandse onderzoekers in beeld gebracht en in een gedetailleerde catalogus opgeslagen
- Behandelen van kanker verschuift steeds meer van chemotherapie naar biologische behandelingen, gerichte therapie waaronder immuuntherapie met gemoduleerde virussen die de minste bijwerkingen geven
- Biomarkers zoals PD-L1, CD163+ en NRAS mutaties en gegevens zoals uitzaaiingen later ontstaan bepalen kans van effectiviteit van immuuntherapie met anti PD medicijnen bij melanomen
- Bloedtesten, een overzicht van recent gepubliceerde resultaten van verschillende bloedtesten
- CRISPR-Cas kan veranderingen in bacterien bewerkstelligen en via bewerkte bacterien verspreiden om zo resistentie van antibiotica te veranderen in opnieuw werkende antibiotica.
- CHRISPR-CAS9 infuus blijkt genezende behandeling voor erfelijke aandoening angio-oedeem, aldus tussenresultaten van internationale studie met Nederlandse deelname.
- CLEVER studie: Waarom kanker jaren later kan terugkeren - en hoe dit te voorkomen. CLEVER studie bij borstkankerpatienten bewijst dat een recidief is te voorkomen door tumorcellen in beenmerg te behandelen.
- De biologische processen waarom en hoe kankercellen uitzaaien wordt beter begrepen, tumorcellen vroeger ontdekt en lijkt ook steeds beter te behandelen
- De huidige staat van moleculair testen in het behandelen van kankerpatienten met solide tumoren. Een uitstekend overzichtsartikel met de nieuwste ontwikkelingen over RNA, DNA en eiwitten anno 2019
- Diagnosetest PERCEPTION via AI - Kunstmatige Intelligentie ontwikkeld en met hulp van single-cell RNA-sequencing voorspelt nauwkeurig of een specifiek medicijn van de kankerpatient zal aanslaan of resistent zal zijn.
- DRUP studie geeft bij 37 procent van de patienten alsnog een therapeutisch effect met 6 procent CR en 14 procent PR en 17 procent stabiele ziekte
- EMA: Veel nieuwe kankermedicijnen in de EU hebben geen bewezen toegevoegde waarde blijkt uit Nederlandse studie naar goedgekeurde kankermedicijnen door het Europees Geneesmiddelenbureau (EMA).
- Erfelijkheid van kanker hangt vaak af van specifieke afwijkende genencombinaties in DNA onderzoek en eiwitexpressie blijkt uit groot Whole Exome Sequencing onderzoek via de Biobank van de UK.
- ESMO - European Society for Medical Oncology heeft een gids uitgegeven voor patienten over hoe personalised medicine werkt en stand van zaken
- FDA ondersteunt onderzoek naar personalised medicine op basis van mutaties ongeacht in welk lichaamsdeel de kanker zich het eerst openbaart.
- Genetisch onderzoek via Germline testen (kiembaan testen) werd in periode 2013 tot 2019 in Georgie en Californie bij slechts 7 procent gedaan onder 1 369 602 patienten met twee jaar kanker.
- Genetische mutatie ontdekt die kans van slagen van immuuntherapie bij alle vormen van kanker naar 100 procent zou kunnen brengen
- Geneesmiddel (ARS1620) verandert kankergen (KRAS mutatie) dat kwaadaardige tumoren beschermt tegen immuunsysteem in een doelwit voor immuunsysteem en helpt immuuntherapie kankercellen te elimineren
- Gentherapie zoals Chrispr-cas en base-editors zijn zeer succesvol bij erfelijke ziekten waaronder ook vormen van kanker zoals sikkelcelziekte
- Gerichte behandelingen met Aurora kinaseremmers geven soms uitstekende resultaten bij veel vormen van kanker. Een reviewstudie
- Immuunafwijkingen bij kankerpatienten gerelateerd aan infecties voortijdig ontdekken zouden in behandelingen van kanker sterven aan kanker met 25 procent of meer kunnen voorkomen
- Immuuntherapie met HER2-gerichte CT-0508 (CAR-Macrofaag therapie) geeft bij solide tumoren van verschillende vormen van kanker met HER2 positieve expressie hoopvolle resultaten
- Immuuntherapie met pembrolizumab bij patiënten met verschillende vormen van uitgezaaide kanker met hoge microsatellietinstabiliteit (MSI-H) en DNA-mismatch-reparatie-deficiënte (dMMR) geeft uitstekende en duurzame resultaten op overall overleving
- Immuuntherapie met nivolumab zorgt voor duurzame en sterk verbeterde overall overleving bij verschillende vormen van kanker, melanomen, longkanker en nierkanker copy 1
- Interleukin-15 speelt een cruciale rol wanneer gegeven samen met immuuntherapie voor verschillende vormen van kanker met solide tumoren en biedt veelbelovende mogelijkheden voor verbeterde behandelingen
- Internationale groep van 180 wetenschappers stelt rapport op hoe en met welke niet-toxische middelen - voedingsstoffen de effectiviteit te verbeteren, recidieven te voorkomen en de bijwerkingen te verminderen van personalised medicine
- Irina Kareva gebruikt wiskundige modellen die de dynamiek van kanker beschrijven, met het doel nieuwe geneesmiddelen te ontwikkelen die gericht zijn op tumoren.
- Kanker-actueel kan en wil helpen - begeleiden bij aanvragen van een volledig biomoleculair receptorenonderzoek en genenonderzoek
- Erfelijkheid: Kanker is vaak domme pech stelt prof. dr. Nicoline Hoogerbrugge van het Radboudumc en de Radboud Universiteit in een interview in de Stentor en Algemeen Dagblad
- Kankermedicijnen geven in de klinische praktijk veel minder effect dan uit de studies van farmaceutische bedrijven is aangetoond. Maar zijn wel ontzettend duur.
- Kankerremmende eiwitten kunnen bij mutatie die gen uitschakelt veranderen van kankerremmend in stimulerend, ontdekten Nederlandse onderzoekers
- Larotrectinib geeft bijzonder goede resultaten (76 procent respons met 12 procent complete remissies) bij alle vormen van solide tumoren met een positieve TRK Fusion mutatie
- Larotrectinib: Met de goedkeuring van Larotrectinib op basis van 1 specifieke afwijking en niet op basis van primaire tumor zorgt de FDA voor een doorbraak in het behandelen van kanker
- Lenvatinib Plus Pembrolizumab bij patiënten met inoperabele gevorderde nierkanker, buikvlieskanker, melanomen en andere gevorderde kanker met solide tumoren geeft uitstekende resultaten met meer dan de helft remissies van 50 procent of meer copy 1
- Medicijnen voorschrijven op basis van DNA profiel van de patient voorkomt 30 procent minder bijwerkingen blijkt uit internationale studie onder leiding van LUMC Leiden
- Moleculaire schakelaar verandert kankercellen in weer normale cellen en zou genezende aanpak van kanker kunnen betekenen
- MSC-1 een medicijn dat de groei van de kankerstamcellen afremt door LIF blokkade en immuunsysteem activeert laat spectaculair goede resultaten zien in fase I studie.
- Mytomorrows breidt aanbod aan experimentele medicijnen voor kankerpatienten uit met 11 nieuwe nog niet geregistreerde medicijnen en stelt deze beschikbaar voor uitbehandelde kankerpatienten
- Nederland betaalt veel meer voor kankermedicijnen, soms tot 50 procent of meer, dan andere landen blijkt uit vergelijkend onderzoek tussen 18 landen copy 1
- NCI-MATCH-studie toont aan dat een biomoleculaire analyse - DNA en receptorenonderzoek - belangrijk is in hoe een kankerpatient te behandelen.
- Nieuw medicijn - PD-0332991 - stopt groei hersentumoren Glioblastoom in dierproeven. Zodra gestopt werd met dit medicijn gingen de tumoren weer groeien. Fase I studie bij 33 patienten met nierkanker en lymfklierkanker bevestigt veiligheid van dit middel
- Nieuwe, dure kankermedicijnen zijn voortaan sneller beschikbaar door het Drug Access Protocol (DAP) dat is ontwikkeld door oncologen, verzekeraars en Zorginstituut Nederland
- Overzicht van alle wereldwijd geregistreerde medicijnen binnen immuuntherapie en lopende studies met immuuntherapie copy 1
- Overzicht van studies met medicijnen en behandelingen om tumoren met KRAS mutaties aan te pakken. Vooral combinatiebehandelingen zijn veelbelovend.
- PI3K/AKT/mTOR pathway speelt cruciale rol in apoptose proces, DNA herstel, metabolisme in de cel en angiogenese.
- Pembrolizumab - Keytruda geeft bij solide tumoren van verschillende oorsprong 21 procent complete remissies en 53 procent gedeeltelijke remissies.
- Personalised medicine door receptorenonderzoek geeft veel betere resultaten in fase 1 studies dan experimenteel onderzoek zonder receptorenonderzoek
- Prof. Bernards over de doorbraak bij darmkanker met Kras mutatie en bij melanomen met BRAF mutatie in DWDD van donderdag 27 maart 2014
- POLE mutatie: veel kankerpatienten met erfelijke vormen van kanker hebben naast een P1-ligand een POLE mutatie en reageren goed op immuuntherapie met anti-PD medicijnen - checkpointremmers als pembrolizumab en nivolumab
- Radiotherapeutisch stimulerend middel NBTXR3 geeft in combinatie met anti-PD-1 medicijnen alsnog uitstekende resultaten bij patiënten die ziekteprogressie lieten zien ongeacht eerdere behandeling met anti-PD-1 medicijnen
- Rezatapopt, een p53-reactivator gericht op de p53 Y220C-mutatie, geeft in veiligheidstudie hoopvolle resultaten bij zwaarvoorbehandelde kankerpatienten met solide tumoren
- Rozlytrek (entrectinib), een tyrosine kinase remmer, goedgekeurd door FDA als medicijn voor solide tumoren met NTRK (neurotrophic tyrosine receptor kinase) gene fusion. Dit is 3e goedgekeurde medicijn op basis van mutatie.
- Stamceltherapie succesvol toegepast bij vrouw met diabetes type 1. Zij hoeft nu al een jaar geen insuline meer te spuiten.
- Tweede primaire vorm van kanker bij een kankerpatient wordt steeds vaker bekend bij de diagnose (2 tot 17 procent) door betere diagnose technieken en verfijnder biomoleculair onderzoek
- Tumorindeling mede aan de hand van biomarkers - biomoleculaire profielen is nodig en zal behandelingen sterk veranderen voor veel kankerpatiënten. Van 10 procent nu tot 50 procent straks. Aldus grote studie van het TOGA
- Vaccin tegen KRAS positief gemuteerde vormen van kanker - darmkankers en longkanker o.a. - wordt gecombineerd met trametinib een anti-PD medicijn in fase I studie na hoopvolle resultaten.
- Voorbeeldrapporten van receptoren en DNA testen - biomoleculaire profielen uitgevoerd door Caris Lifesciences - van alvleesklierkanker, hersentumoren, melanomen en longkanker
- Vroege diagnose van kanker is de toekomst en is vaak al mogelijk: zie TED talk
- Xeloda (capecitabine) en fluorouracil (5-FU) kunnen levensbedreigende bijwerkingen veroorzaken bij kankerpatienten met een DPD-deficiëntie. FDA pleit voor testen op genmutaties vooraf aan behandelingen.
- Ziekte van Parkinson: prasinezumab, een monoklonaal antilichaam dat alfa-synucleïne bindt, vertraagt sterk de progressie van de ziekte van Parkinson in vergelijking met patienten die beste zorg kregen
- Algemeen: overzicht van artikelen waarin personal medicine een rol speelt.



Plaats een reactie ...
Reageer op "Personalised medicine door receptorenonderzoek geeft veel betere resultaten in fase 1 studies dan experimenteel onderzoek zonder receptorenonderzoek"